부처연구성과
세포분열을 끝내는 조절기전의 신규규명
- 등록일2012-01-17
- 조회수6509
-
성과명
세포분열을 끝내는 조절기전의 신규규명
-
연구자명
송기원 교수팀
-
연구기관
연세대학교 생명시스템대학
-
사업명
21세기프론티어 미생물유전체활용기술개발사업
-
지원기관
교육과학기술부
-
보도자료발간일
2012-01-17
- 원문링크
-
키워드
#유전체의 안정 #유사분열 #생화학적 조절
- 첨부파일
핵심내용
-유전학계 세계 최고 권위 저널 ‘PLoS Genetics'지 온라인판에 게재 -
□ 세포분열에서 복제된 염색체를 분배하는 과정인 “유사분열”을 종결시키는 생화학적 조절 절차가 국내 연구진에 의해 밝혀졌다.
○ 유사분열 종결기전은 체세포의 분열로 만들어진 딸세포가 추가적인 세포분열을 종결하고 유전체의 안정성을 유지하기 위한 핵심과정이다.
※ 유사분열 : 세포주기 중 복제된 염색체를 물리적으로 반반씩 똑같이 분리하여 두 개의 딸세포에 분배하는 과정
□ 교육과학기술부는 연세대학교 생화학과 송기원 교수팀이 효모를 이용하여 종결기전을 조절하는 세포 내 단백질의 상호작용을 규명해 냈다고 밝혔다.
□ 세포가 유전체의 손상을 받는 등 유전체의 안정성을 위협하는 작용이 있을 경우 세포는 유전체의 안정성을 유지하기 위해 유사분열의 종결을 억제한다.
○ 이때 유사분열의 종결이 그대로 진행되면 딸세포의 DNA가 손상되며 결과적으로 암과 같은 질병이 발생할 수 있다.
○ 그동안 유전체의 안정성이 위협받는 경우의 유사분열 종결 억제기전은 몇몇 연구그룹에 의해 보고되어 있었으나, 정상 분열에서 종결기전의 조절은 잘 알려져 있지 않았다.
□ 송 교수팀은 신호전달계의 스위치로 작용하는 단백질(Bfa1)의 4개의 아미노산기가 특정 인산화효소에 의해 인산화되고 이 때문에 세포내 위치변화가 유발되어 유사분열의 시기가 조절된다는 것을 확인하였다.
○ 결과적으로 세포에 유전체의 안정성이 위협받는 경우와 그렇지 않은 경우, 서로 다른 기전에 의해 유사분열의 종결과 시기가 섬세하게 조절될 수 있음을 제시하였다.
□ 송기원 교수는 “이번 연구 결과는 생명 유지의 핵심과정인 세포분열의 새로운 조절 기전을 규명한데의 의의가 있으며, 향후 세포분열 이상으로 야기되는 현상인 암 등을 제어할 수 있는 응용 기술 개발에 기여할 수 있다”고 말했다.
□ 이번 연구는 ‘21세기프론티어 미생물유전체활용기술개발사업단’(단장 오태광)의 지원을 받아 수행되었으며 연구결과는 유전학계의 세계 최고 권위 학술저널인 ‘PLoS Genetics'지 2012년 1월 12일자 온라인 판에 게재되었다.
상세내용
용 어 설 명
□ 유전체의 안정성 (genomic stability)
○ 세포가 가지고 있는 유전정보의 총체인 유전체가 세포주기 동안 복제하고 분리되는 과정에서 변이나 변화 없이 원래 정보를 그대로 유지 하는 것.
□ 인산화
○ 생체의 분자를 인산 유도체로 만드는 반응을 말함. 생체 내 대사조절(에너지 저장·공급·운반 중개 등)의 주요물질인 에이티피(ATP)에서부터 효소반응에 의하여 인산기를 전달하는 것으로 인산화는 주로 효소의 세린이나 트레오닌에서 이루어짐
□ Bfa1의 4개 아미노산기
○ 인산화는 주로 단백질의 세린이나 트레오닌에서 이루어지는데, 송교수팀은 Bfa1 위치를 조절하는 아미노산기 452, 453, 454, 559번의 세린(Serine)이 인산화되어 Bfa1 위치 변화를 일으킨다는 것을 세계 최초로 발견하였음. 한편, 아미노산은 자연계에 20개가 존재하며 세린은 그 중 하나임.
□ 유사분열 종결기전 (mitotic exit network)
○ 유사분열에서 복제된 유전체를 앞으로 딸세포가 될 영역으로 분리한 후 유사분열을 끝내기 위해 유사분열 진행을 위해 활성화 되었던 Cdk(cyclin-dependent kinase)를 불활성화 시키는 신호전달계로 small GTPase 및 그 조절단백질을 포함함. 세포의 유전체에 문제를 유발하여 유전체의 안정성이 저해(세포섭동) 되어있는 상태로 유사분열이 종결되면 세포주기로 생성된 두 딸세포의 유전체 안정성이 담보될 수 없으므로 DNA손상, 미세소관 형성 이상 등에 의해 그 활성화가 억제 됨. 유전체가 안정하며 세포분열을 진행하는데 문제가 없을 때의 유사분열 종결 시기 조절 기전은 잘 알려져 있지 않았고 본 연구가 그 기전을 최초로 제시함.
그 림 설 명
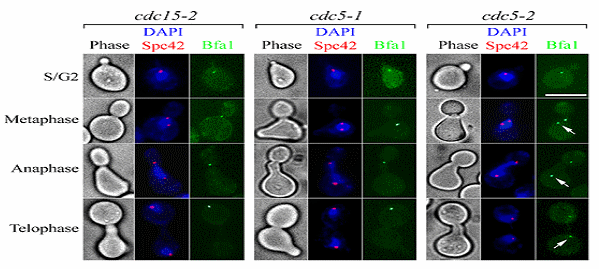
그림 1. 유사분열 종결의 주 조절자인 Bfa1의 위치가 인산화효소 Cdc5에 의존
Bfa1은 유사분열 종결 시점에서 딸세포 쪽 spindle pole body (SPB)에만 비대칭적으로 위치하나(왼쪽), kinase 활성이 없는 cdc5-2 변이체에서는 대칭적으로 양쪽 SPB에 위치함(오른쪽). kinase 활성이 있는 cdc5-1 변이체에서는 정상 경우처럼 비대칭적으로 위치함 (중간).
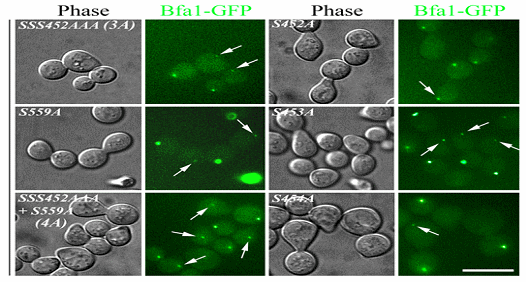
그림 2. Bfa1이 비대칭적으로 위치를 조절하기 위한 Cdc5 인산화효소로 매개되는 Bfa1 인산화 아미노산 잔기 확인
Bfa1의 비대칭적 위치 조절을 검증하기 위해 본 연구에서 밝힌 Cdc5 인산화효소에 의해 인산화 되는 4개의 serine 잔기를 인산화되지 못하도록 바꾼 Bfa1 변이체 (4A로 표기)는 정상과 달리 항상 비대칭적으로 위치함.
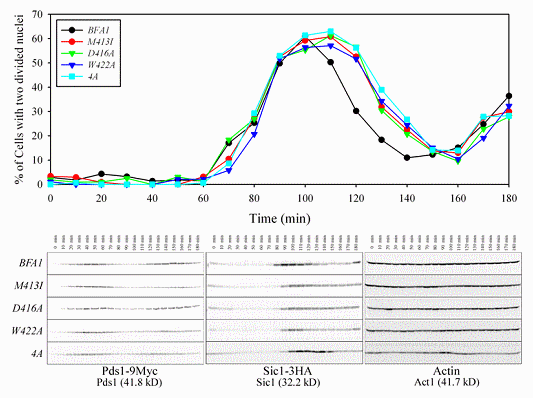
그림 3. Cdc5 인산화효소에 의한 Bfa1 인산화로 정확한 유사분열 종결 시기 조절
Cdc5에 의한 Bfa1 인산화와 비대칭적 위치는 정확하게 유사분열 종결시기를 조절하는 기능을 수행하며 인산화 되지 못하는 변이체(4A)는 유사분열 종결이 지연됨을 확인


 세포분열_끝내는_조절절차규명.hwp
세포분열_끝내는_조절절차규명.hwp