부처연구성과
우리 몸의‘아미노산 스위치’를 찾다 !
- 등록일2012-03-19
- 조회수7537
-
성과명
우리 몸의‘아미노산 스위치’를 찾다 !
-
연구자명
김성훈 교수, 한정민 교수, 류성호 교수 연구팀
-
연구기관
서울대, 포항공대
- 사업명
-
지원기관
교육과학기술부
-
보도자료발간일
2012-03-19
- 원문링크
-
키워드
#아미노산 #Leucyl-tRNA synthetase #mTORC1
- 첨부파일
핵심내용
-서울대 글로벌프론티어 김성훈 단장, 셀(Cell) 게재 -
교육과학기술부(장관 이주호)는 ‘서울대 글로벌프론티어 의약바이오컨버젼스연구단’(경기도 참여)의 김성훈 교수와 한정민 교수, 포항공대 류성호 교수 연구팀이 Leucyl-tRNA synthetase (이하 LRS)라는 효소가 단백질 합성을 조절하는 아미노산 스위치의 역할을 하고 있음을 세계 최초로 규명하였다고 밝혔다.
□ 아미노산은 단백질을 구성하는 기본 요소로 근육형성, 혈당, 수명, 암, 신경질환 등 거의 모든 신체 대사와 질병 발생에 관련되어 있지만 아직까지 세포에서 아미노산의 농도 변화를 감지하는 메커니즘이 발견되지 않았었다.
□ 최근 소위 “몸짱” 열풍으로 인해 각종 아미노산을 포함하는 다양한 기능성 식품들이 즐비하지만 이들이 어떻게 근육형성과 에너지 생성에 기여하는 지에 대한 지식은 매우 부족했다.
○ 특히 류신(Leucine)이라는 아미노산은 근육 형성에 가장 중요한 역할을 하는데 세포 내에서 류신을 감지하는 센서의 존재가 과거 20여 년간 학계의 초미의 관심사였다.
□ 김성훈 교수 연구팀은 이번 연구를 통해 LRS가 류신을 감지하여 단백질 합성을 조절하는 스위치 기능을 한다는 것을 규명했다.
○ LRS의 발현을 억제하거나 류신 결합 부위를 돌연변이 시키면 류신이 존재해도 단백질 합성이 활성화 되지 않았으며,
○ LRS와 류신이 결합하면 구조가 변형되어 mTOR이라는 단백질 합성 조절 신호전달체계에 결합하여 단백질 합성을 활성화함을 증명했다.
□ 김성훈 단장은 “단백질 합성 과정은 정상적일 경우 근육 형성 등 몸의 성장을 주관하지만 이번에 밝혀진 LRS와 같은 아미노산 스위치가 고장 났을 경우 암, 당뇨, 노화 등의 질병을 유발하는 것으로 알려져 있다”며 “실제로 암 조직에서 LRS가 과발현되는 경우도 보고가 되고 있다”고 설명했다.
□ 이어 “이러한 이유로 최근 단백질 합성 조절에 관여하는 여러가지 조절인자들을 중심으로 신약개발 연구가 활발히 이루어지고 있다”며 “LRS가 암, 당뇨, 수명조절 등의 신약개발에 새로운 타깃으로 활용될 수 있을 것으로 기대된다.”고 강조했다.
□ 연구 결과는 생명과학 분야 세계 최고 권위의 학술지인 ‘셀 (Cell)’ 3월 15일자 온라인판에 발표됐으며, 4월호에 정식 게재될 예정이다.
상세내용
연 구 결 과 개 요
Leucyl-tRNA Synthetase Is an Intracellular Leucine Sensor for the mTORC1-Signaling Pathway
J.M. Han et al. (Cell - 2012. 3.15 온라인 게재, 4월호 게재 예정)
20 여종의 아미노산 중 류신 (leucine)은 세포 내 단백질 합성을 증가시키는 능력이 있으며 특히 아미노산 음료나 고기류와 같은 음식에 포함된 류신이 근육세포에서 단백질합성을 촉진함으로써 근육생성에 중요한 영향을 미치는데 이 과정에 mTOR 신호전달 경로가 관련이 되어있다. 최근 연구 결과들로부터 mTOR 신호전달 경로는 암 생성 및 촉진, 당뇨, 노화와 같은 중요한 생리현상과 밀접한 연관성이 있다는 것이 밝혀졌다.
연구팀은 세포 내 LRS 단백질이 세포 내 류신 농도를 감지하는 아미노산 스위치로 작용함으로써 mTOR 신호전달 경로를 활성화시키는 일련의 과정들을 상세히 밝혀냈다. 특히 세포 내 LRS 유전자를 특이적으로 억제하였을 때 스위치 기능의 저하로 인해 류신 농도 감지가 제대로 되지 않아 mTOR 신호전달 경로를 통한 생리 현상 조절이 제대로 되지 않았다.
또한 mTOR 신호전달 경로는 암세포에서 비정상적으로 활성화되어 있어 암 치료제의 타겟으로 최근 각광받고 있는데 결국 아미노산의 많고 적음을 감지하는 LRS가 암을 포함하여 여러 질환에 관련되어 있는 mTOR 신호전달 경로와 연결되어 있음을 알 수 있었고 이는 대사-단백질합성조절-암이 연결이 되는 중요한 발견이다. 따라서 이러한 중요성이 인정되어 생명과학 분야 세계 최고의 권위를 자랑하는 Cell 지에 논문 게재가 수락이 되었다. 위 연구 결과는 암 치료제 개발에 있어서 신규 타겟을 발굴하는데 도움이 되고 이들 정보로부터 새로운 신약이 개발될 것이다.
용 어 설 명
□ 셀 (Cell) 지
○ Cell 지는 1974년에 창간된 이래 생명과학 분야 연구에서 가장 인용이 많이 되는 과학 저널로 26가지 생명과학 분야에서 중요한 발견을 우선 게재한다. 월간저널로 1년에 총 120편 정도의 논문만이 실린다. 참고로 Cell의 2010년 Impact Factor는 32.401입니다.
□ LRS (Leucyl-tRNA synthetase)
○ LRS는 단백질 합성에 필요한 ‘류신(leucine) 아미노산’(20가지 아미노산 중 하나)을 사용할 수 있도록 활성화 시켜주는 효소로 알려져 있습니다.
□ mTORC1 (mammalian target of rapamycin complex 1)
○ Rapamycin이라는 약의 타겟으로 발굴된 단백질로써 세포 성장, 세포 생존, 단백질 합성, 유전자 발현 등 세포 내 다양한 생리 현상을 조절하는 중요 인자로 최근에는 수명 연장과 밀접한 관련이 있다는 것이 밝혀져 있고 성장인자와 아미노산 농도에 따라 활성이 조절되는 인산화 효소로 알려져 있습니다.
그 림 설 명
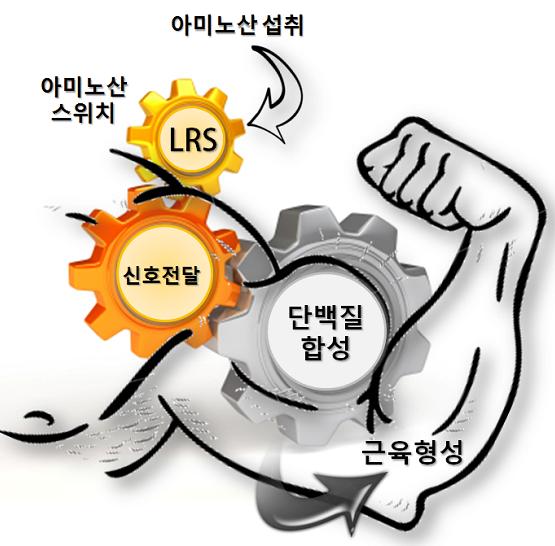
□ 섭취한 아미노산이 세포내로 유입되면 LRS가 아미노산을 감지하여 단백질 합성과정을 활성화하는 신호전달시스템을 가동함. 따라서 LRS 스위치가 작동하지 않으면 섭취한 아미노산이 단백질합성으로 이어지지 못함.
□ LRS를 포함하는 아미노산 신호전달체계가 고장이나 단백질합성과정에 이상이 오게되면 암, 당뇨, 노화 등의 난치 질환이 형성됨.


 우리몸의아미노산스위치를찾다.hwp
우리몸의아미노산스위치를찾다.hwp