제도동향
혁신성에 근거한 디지털헬스케어의 가치 평가 필요성
- 등록일2021-07-30
- 조회수4571
- 분류제도동향 > 종합 > 종합
-
자료발간일
2021-07-22
-
출처
한국보건산업진흥원
- 원문링크
-
키워드
#혁신성#디지털헬스케어#가치평가
- 첨부파일
혁신성에 근거한 디지털헬스케어의 가치 평가 필요성
◈목차
Ⅰ. 배경
Ⅱ. 미국 CMS의 신기술추가지불보상(NTAP) 제도
Ⅲ. 시사점
◈본문
Ⅰ 배경
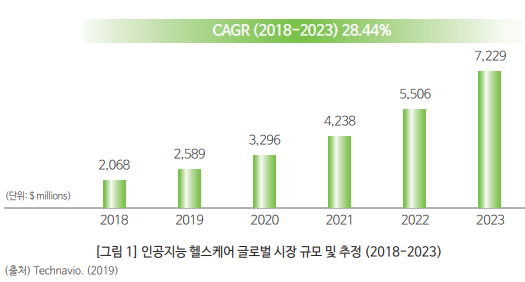
⊙ 대표적 디지털헬스케어 기술 중 하나인 인공지능(AI, Artificial Intelligence)은 난이도가 높고 복잡한 물리적 정신적 노동 과정을 자동화하는 것을 혁신 특성으로 하는 기술로써 특히 의료 부문에서는 인공지능 기술이 영상진단, 신약발견, 가상비서, 작업(Workflow)관리와 같은 다양한 영역에서 솔루션을 제공하고 있어, 의료 영역 글로벌 인공지능 시장의 규모는 크게 성장할 것으로 예상하고 있다1)
⊙ 우리나라는 최근 인공지능 기반 의료기기 등 혁신기술에 대하여 의료기기 허가·신의료기술평가 등을 통합 운영함으로써 시장진입 소요기간을 단축할 수 있는 규제 개선을 추진한 바 있고2) 의료서비스 내 혁신기술 도입을 촉진하기 위한 정책을 수립하고 있으나3) , 현재 의료 AI는 의료진의 판단을 보조하는 기기로써 포지셔닝 되어있어 비용 효과성을 평가하기 어려운 부분이 있고, 다양한 이해관계자가 존재하여 지불주체와 적정서비스 가격 결정과 관련한 논의가 좀처럼 진전되고 있지 못한 상황이다
⊙ 또한 의료서비스 내 신속한 신기술 도입을 위한 다양한 지원 제도가 추진되고 있으나 여전히 의료 현장까지 신기술이 전달되는 과정은 허가 후 급여까지 다양한 평가 단계와 기준을 충족하는 근거를 생산・보유해야 가능한 상황이고, 이는 기업이 해당 기술로 사업화하기까지 장기간 투자를 요하게 하므로 가격 결정에도 영향을 미치는 요인이 되고 있다
⊙ 미국, 영국, 독일 등 여러 국가에서는 의료서비스의 혁신을 위해 제도적 정책적으로 다양한 변화를 시도하고 있으며, 특히 의료 현장에 신기술 활용을 적극 지원하기 위해 신기술에 대한 별도 평가 트랙 및 추가 보상 체계에 대한 논의를 진척시키고 있다
⊙ 최근 미국 Centers for Medicare & Medicaid Services(CMS)에서 신기술추가지불 보상제도(NTAP, New Technology Add-on Payment)를 통해 Viz.ai사 ContaCT가 인공지능 의료기기로는 최초로 승인되어 해당 사례의 근거 수준을 살펴보고, 국내 신기술 의료서비스의 평가방법과 보상체계 구축에 참조할 시사점을 찾아보고자 하였다
Ⅱ 미국 CMS의 신기술추가지불보상(NTAP) 제도
1) NTAP 제도 특징 및 현황
⊙ 미국 CMS는 메디케어 포괄수가제(Medicare Severity Diagnosis-related Groups, MS-DRG) 시스템에 따라 수집된 자료(2~3년 동안 발생한 메디케어 청구 자료)를 기반으로 수가를 매년 갱신하는데, 이 시스템에서는 새롭고 고가인 기술을 활용한 혁신적 치료에 대해 산출근거를 생성하기 어려워 신기술 도입에 장벽이 되므로 이를 개선하기 위해 인센티브 제도로써 NTAP을 도입했다고 밝힌 바 있다4)
⊙ CMS의 NTAP 승인을 받기 위해서는 ①신규성(Newness) ②진료비용(Cost) ③상당한 임상개선 (Substantial clinical improvement)의 3가지 기준을 충족해야 하며5)6) , 제도와 관련한 안내에서 “신규성”은 보통 FDA 허가 및 시장 출시부터 3년 이내의 기술로(FDA 510(k) 승인 제외), 기존에 유사한서비스나 기술이 있을 경우 인정하지 않을 것임을 분명히 하고 있으며, 진료비용 부분은 신기술에 대한 지불대가로써 MS-DRG 수가가 부적절한 수준이라는 점을 설명할 수 있어야 한다는 것이고, 상당한 임상개선이라 함은 신기술이 다른 서비스 또는 기술에 비해 상당한 임상적 이점을 제공함을 입증해야 한다고 정리하고 있다

⊙ 미국 CMS는 기업이 제출한 자료를 바탕으로 전문가 타운홀(Town hall) 미팅 등을 통해 신규성, 진료비용, 상당한 임상 개선의 여부를 검토하고, 자료 검토 과정에서 전문가의 질의에 대하여 회사의 답변 및 추가 데이터를 요구하기도 하며, 최종적으로 승인/거절 여부를 판단한다
⊙ 혁신적인 치료를 위해 2001년에 도입된 NTAP 프로그램은 2003~2018년 동안 95개 제품이 신청되었고 그 중 30%만 NTAP 요건을 충족하여 승인되었다. 나머지는 ‘신규성의 기준(Newness criteria)’을 충족하지 못한 것이 주된 원인으로 철회(25%), 거부(45%) 등의 결정을 받은 것으로 보고되고 있다7)
⊙ 이런 이유로 CMS에서는 NTAP의 진입 장벽을 해소하고 혁신적인 치료의 도입을 장려하고자 제도개선을 추진하였는데, 개선사항은 지불보상금액을 인상하는 것과, 임상개선 입증기간을 연장해준 조치이다8)9)
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
-
다음글
- 코로나19 감염 동물모델 사례집
-
이전글
- [KBCH보고서] 일본 2021
관련정보
지식
동향


 보건산업브리프 328호(수정).pdf
보건산업브리프 328호(수정).pdf