부처보도자료
국내 개발 코로나19 혈장분획치료제 2상 임상 승인
- 등록일2020-08-20
- 조회수3068
-
발간일
2020-08-20
-
출처
식품의약품안전처
- 원문링크
-
키워드
#코로나19#국내#혈장분획치료제
- 첨부파일
국내 개발 코로나19 혈장분획치료제 2상 임상 승인
코로나19 치료제·백신 국내 임상시험 총 16건 진행
□ 식품의약품안전처(이의경 처장)은 국내 개발 코로나19 혈장분획치료제 ‘GC5131’에 대하여 2상 임상시험을 8월 20일 승인하였습니다.
○ 이로써 현재 국내에서 코로나19 관련하여 진행 중인 치료제 및 백신의 임상시험은 총 16건(치료제 14건, 백신 2건)이 되었습니다.
□ 이번에 승인한 ‘GC5131’은 ‘녹십자’에서 코로나19 완치자의 혈장을 이용해 개발 중인 ‘고면역글로불린(Hyper-immune Globulin)’ 성분 의약품으로, 코로나19 환자를 대상으로 안전성과 유효성을 평가하는 2상 임상시험을 진행하게 됩니다.
|
임상시험 단계 |
|
|
(임상 1상)최초로 사람에게 투여하여 안전성, 약동학등을 평가 (임상 2상)1상 종료 후, 대상 환자들에게 투여하여 치료효과를 탐색 (임상 3상)2상 종료 후, 많은 환자들에게 투여하여 안전성 및치료효과를확증 ※ ‘1상과 2상’(1/2상) 또는 ‘2상과 3상’(2/3상)을 동시 진행하는 경우도 있음 |
|
○ 해당 제품은 코로나19 완치자의 혈액 중 혈장을 대량으로 수집한 후 여러 공정을 거쳐 제품화한 것으로 코로나19 중화항체가 농축된 면역글로불린입니다.
* 중화항체 : 코로나19 바이러스를 중화(무력화)할 수 있는 항체
* 면역글로불린 : 혈장 성분 중 면역에 중요한 역할(항원-항체반응)을 하는 단백질
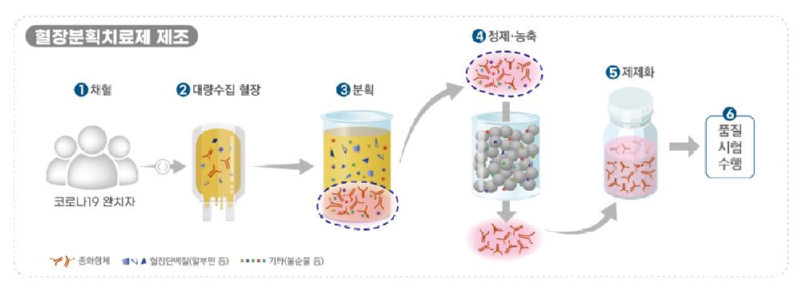
<혈장분획치료제 제조공정 개요>
|
➊코로나19 완치자로부터 혈장을 채혈 합니다
➋코로나19 완치자 혈장을 대량으로 모읍니다.
➌ 혈장 내 다른 성분(알부민, 혈액응고인자 등)과 중화항체가포함된
면역글로불린을 분리합니다. ➍ 분리된 면역글로불린을 정제‧농축하여 불순물을 제거합니다.
➎ 제제화하여 ‘혈장분획치료제’를 생산합니다.
➏ 품질시험을 실시하고 적합한 제품을 출하합니다.
|
○ 식약처는 지난 3월부터 혈장분획치료제 개발을 위해 사전상담을 진행해 왔으며,
- 원료물질인 혈장이 인체에서 유래하고 중화항체를 이용해 질병을 치료하는 동일 원리를 적용한 제품이 예전부터 개발되어 사용되고 있어 임상 1상 시험을 면제하였습니다.
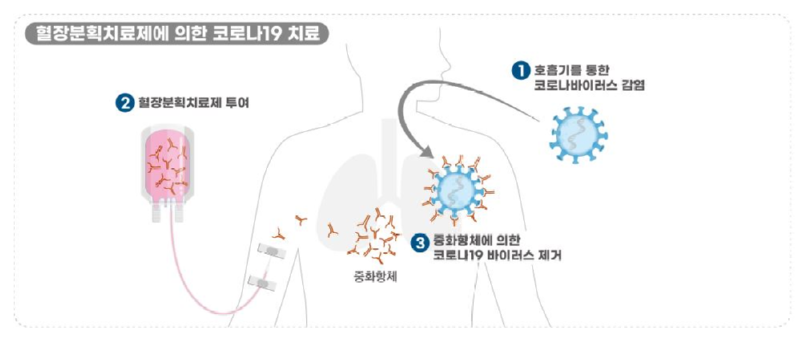
<혈장분획치료제 작용 원리>
|
➊ 코로나19 바이러스가 호흡기를 통해 침입하여 감염을 일으킵니다. ➋ 환자에게 혈장분획치료제를 투여합니다. ➌ 투여된 중화항체가 침입한 코로나19 바이러스를 제거합니다. |
○ 참고로 해외에서도 프랑스, 중국, 일본 및 이탈리아에서 혈장분획치료제를 개발 중이며, 현재 6개의 소규모 임상시험이 진행 중에 있습니다.
□ 식약처는 코로나19 치료제·백신 개발에 대한 국민적 관심이 큰 만큼 앞으로도 국내 개발 제품의 임상시험 현황에 대해서 신속하게 정보를 전달하도록 하겠습니다.
○ 또한, 안전하고 효과 있는 코로나19 치료제·백신이 신속히 개발될 수 있도록 최대한 지원할 계획입니다.
<첨부> 국내 코로나19 임상시험 승인 현황(2020.8.20 기준)
|
구분 |
연번 |
의뢰자 |
제품명 |
임상시험제목 |
단계 |
승인일 |
|
치료제 |
1 |
길리어드사이언스코리아 유한회사 |
렘데시비르 |
중증 COVID-19 시험대상자에서 렘데시비르(GS-5734™)의 안전성 및 항바이러스 활성을 평가하기 위한 제3상 무작위 배정 시험[종료] |
3상 |
2020-03-02 |
|
2 |
길리어드사이언스코리아 유한회사 |
렘데시비르 |
중등도 COVID-19 시험대상자에서 표준 치료 투여와 비교해 렘데시비르(GS-5734™)의 안전성 및 항바이러스 활성을 평가하기 위한 제3상 무작위 배정 시험 [종료] |
3상 |
2020-03-02 |
|
|
3 |
서울대학교병원 |
렘데시비르 |
COVID-19에 대한 remdesivir의 안전성과 유효성에 대한 다기관, 무작위배정, 이중눈가림, 위약대조 연구 [종료] |
연구자 임상 |
2020-03-05 |
|
|
4 |
재단법인아산사회복지재단서울아산병원 |
칼레트라정, 옥시크로린정 |
경증 코로나19 환자에서 lopinavir/ritonavir vs hydroxychloroquine vs 비투약군 간의 open labelled randomized controlled clinical trial [종료] |
연구자 임상 |
2020-03-20 |
|
|
5 |
강남세브란스병원 |
할록신정 |
SARS -CoV -2 에 대한 노출 후 예방으로서 하이드록시클로르퀸 연구 [종료] |
연구자 임상 |
2020-03-25 |
|
|
6 |
고려대학교의과대학 부속 구로병원 |
알베스코 흡입제 |
경증 코로나19 환자에서 Ciclesonide의 임상적 유효성 평가 |
연구자 임상 |
2020-03-27 |
|
|
7 |
부광약품㈜ |
레보비르캡슐30mg (클레부딘) |
중등증 코로나바이러스감염증-19(COVID-19) 환자에서 클레부딘 (Clevudine)의 안전성과 유효성을 평가하는 단일맹검, 무작위배정, 위약대조, 다기관 제2상 임상시험 |
2상 |
2020-04-14 |
|
|
8 |
경상대학교병원 |
후탄 (나파모스타트) |
: 코로나19 폐렴 환자에서 Nafamostat mesilate 의 치료효과 분석을 위한 open labelled randomized controlled clinical trial |
연구자 임상 |
2020-04-17 |
|
|
9 |
동아대학교병원 |
페로딜 정 |
COVID-19 감염 중증 폐렴 환자의 폐 기능에 관한 이펜프로딜의 28일 제2a상 공개, 연구자 주도 연구 |
연구자 임상 |
2020-04-21 |
|
|
10 |
엔지켐 생명과학 |
EC-18 |
신종 코로나바이러스로 인한 폐렴환자에서 EC-18의 안전성과 유효성을 평가하기 위한 다기관, 무작위 배정, 이중 눈가림 제 2상 임상시험 |
2상 |
2020-05-12 |
|
|
11 |
신풍제약㈜ |
피라맥스정 |
경증 또는 중등증 코로나바이러스감염증-19 (COVID-19) 환자를 대상으로 피라맥스정의 유효성 및 안전성을 비교 평가하기 위한 다기관, 무작위배정, 이중눈가림, 평행, 위약대조, 제 2상 임상시험 |
2상 |
2020-05-13 |
|
|
12 |
서울대학교병원 |
바르시티닙 |
COVID-19에 대한 새로운 약제들의 안전성과 유효성에 대한 다기관, 무작위배정, 이중눈가림, 위약대조 연구 |
연구자 임상 |
2020-05-18 |
|
|
13 |
㈜종근당 |
CKD-314 (나파모스타트) |
코로나 19 폐렴으로 진단받아 입원한 환자 대상으로 CKD-314의 유효성과 안전성을 평가하기 위한 공개, 다기관, 무작위배정, 치료적 탐색 제 2상 임상시험 |
2상 |
2020-06-17 |
|
|
14 |
크리스탈지노믹스㈜ |
CG-CAM20 (카모스타트) |
코로나19 바이러스 (SARS CoV 2) 감염이 확진된 COVID-19 환자에서의 카모스타트(Camostat) 치료의 유효성 및 안전성을 평가하기 위한 무작위 배정, 이중 눈가림, 위약대조, 평행 2상 임상 시험 |
2상 |
2020-07-01 |
|
|
15 |
㈜대웅제약 |
DW1248정 (카모스타트) |
경증 및 중등증 코로나19 환자를 대상으로 DWJ1248의 유효성 및 안전성을 평가하기 위한 이중눈가림, 무작위배정, 위약대조, 다기관 제2상 임상시험 |
2상 |
2020-07-06 |
|
|
16 |
㈜셀트리온 |
CT-P59 |
건강한 시험대상자를 대상으로 CT-P59의 안전성, 내약성 및 약동학을 평가하는 제1상, 무작위배정, 이중눈가림, 위약 대조군, 평행군, 단회 투여 용량 증량 임상시험 |
1상 |
2020-07-17 |
|
|
17 |
서울대학교병원 |
Rebif (인터페론) |
COVID-19에 대한 새로운 약제들의 안전성과 유효성에 대한 다기관, 무작위배정, 이중눈가림, 위약대조 연구 |
연구자 임상 |
2020-08-04 |
|
|
18 |
㈜제넥신 |
GX-I7 (인터루킨) |
코로나바이러스 (COVID-19) 감염된 환자에서 GX-I7의 안전성 및 예비 효과 탐색을 위한 제1b상 임상시험 |
1b상 |
2020-08-07 |
|
|
19 |
㈜녹십자 |
GC5131 (혈장분획치료제) |
COVID-19 환자에서 H-Ig(고면역글로불린) GC5131의 용량 설정 및 유효성, 안전성을 평가하기 위한 전향적, 공개, 무작위 배정, 다기관 제2상 임상시험 |
2상 |
2020-08-20 |
|
|
백신 |
1 |
국제백신연구소 |
INO-4800 |
건강한 성인을 대상으로 피내 (Intradermal, ID) 접종 후 전기천공법(Electroporation, EP)을 이용하는 SARS-CoV-2 예방백신INO-4800 의 안전성, 내약성 및 면역원성을 평가하기 위한 용량 증량, 제 I/IIa 임상시험 |
1/2a상 |
2020-06-02 |
|
2 |
(주)제넥신 |
GX-19 |
건강한 성인을 대상으로 COVID-19 예방 DNA 백신 GX-19의 안전성, 내약성 및 면역원성을 탐색하기 위한 다기관, 무작위 배정, 이중 눈가림, 위약대조, 제1/2a상 임상시험 |
1/2a상 |
2020-06-11 |
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.


 8.20+임상제도과.hwp
8.20+임상제도과.hwp