부처보도자료
코로나19 치료제·백신 허가·심사, 어떻게 진행되고 있나요 (2)
- 등록일2021-01-22
- 조회수2058
-
발간일
2021-01-22
-
출처
식품의약품안전처
- 원문링크
-
키워드
#코로나19 백신#코로나19 치료제
- 첨부파일
코로나19 치료제·백신 허가·심사,
어떻게 진행되고 있나요 (2)
□ 식품의약품안전처(김강립 처장)는 코로나19 치료제 ‘렉키로나주’와 코로나19 백신 ‘아스트라제네카코비드-19백신주’의 품목허가 진행 상황에 대해 다음과 같이 설명합니다.
1 치료제 허가·심사 진행 상황
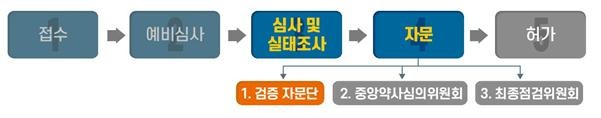
□ 식약처는 ㈜셀트리온이 허가 신청한 ‘렉키로나주’와 관련해 제조소 및 임상시험실시기관(의료기관)에 대한 실태조사를 마쳤으며, 현재 비임상·임상시험 자료에 대해 추가 검토와 품질자료에 대한 심사를 진행하고 있습니다.
<< 자료심사(품질) >>
□ 품질자료는 치료제의 제조공정관리, 품질의 적합성 등에 관한 자료로서, 원료의약품 및 완제의약품의 물리화학적·생물학적 성질, 제조방법, 기준 및 시험방법, 표준품, 용기·포장 등에 관한 자료를 심사하고 있습니다.
○ 또한 유전자재조합의약품의 특성을 고려한 원료관리 자료, 공정단계별 불순물 제거 검증 자료, 보관방법 및 사용기간 설정을 위한 안정성시험 자료를 검토하고 있습니다.
<< 임상시험실시기관(의료기관) 실태조사 >>
□ 임상시험 참여 환자의 안전과 시험결과의 신뢰성을 확인하기 위해 환자 동의서 작성, 임상시험용의약품 관리, 전자 자료 관리 등 임상시험 전반에 걸쳐 규정 준수 여부를 서류검토와 현장 점검(1.12.~15.)을 통해 확인했습니다.
○ 또한 해외 의료기관의 경우 임상시험의 신뢰성과 국제적 윤리기준에 따라 수행되었는지 서류상으로 중점검토했습니다.
2 백신 허가‧심사 진행 상황
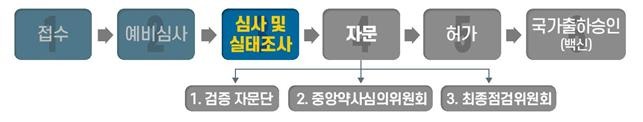
□ 식약처는 ㈜한국아스트라제네카가 허가 신청한 ‘아스트라제네카코비드-19백신주’와 관련해 제조소에 대한 실태조사를 마쳤으며, 현재 비임상·임상시험 자료와 품질자료에 대한 심사를 진행하고 있습니다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.


 1.21+첨단제품허가담당관.pdf
1.21+첨단제품허가담당관.pdf