산업동향
바이오제조 동향_세포유전자치료제 중심
- 등록일2021-07-26
- 조회수5060
- 분류산업동향 > 제품 > 바이오의약
-
자료발간일
2021-07-26
-
출처
한국바이오협회
- 원문링크
-
키워드
#바이오제조동향#세포유전자치료제
- 첨부파일
바이오제조 동향_세포유전자치료제 중심
◈본문
세포·유전자치료제의 성장이 바이오제조(biomanufacturing)의 변화를 추동하고 있다. 2020년 2월 기준 세포·유전자치료제는 전체 출시된 의약품에서 차지하는 비중이 1%로 나타나지만 임상 파이프라인의 12%를 차지하고 공개된 전임상 파이프라인의 16%를 차지하며 개발 중인 파이프라인에서 차지하는 비중은 훨씬 크게 나타난다.
첫 출시 후 초반 수년 안에 10~20개가량의 제품으로부터 연간 50억 달러의 매출이 발생하고 있다는 점에서 세포·유전자치료제는 지난 20 년간 의약품 산업에 큰 변화를 일으킨 단일클론항체(monoclonal antibodies) 의약품의 초기 개발 양상과 유사한 모습을 보인다.1) 항체치료제는 1997년 첫 출시 후 5년이 된 시점에서 15개 이상의 치료제로부터 51억 달러의 매출이 발생했다. 이후 생산수율 향상과 비용 감축을 위한 더 효율적인 제조 방법이 개발되면서 2018년에는 100개에 달하는 제품에서 발생하는 매출이 1,225억 달러에 이르고 있다.
세포·유전자치료제도 파이프라인의 개발과 함께 제조 방법의 개발이 성공적으로 이루어진다면 주요 치료 양식(modality)으로의 성장이 기대된다. 세포·유전자치료제의 개발이 가속화됨에 따라 세포‧ 유전자치료제의 위탁개발생산(Contract Development and Manufacturing Organization, 이하 CDMO) 시장의 가파른 성장이 전망되 고 있다.
약 20% 정도의 제조 공정이 아웃소싱으로 이뤄지는 다른 바이오의약품 분야와 달리 세포·유전자치료제 분야에서는 50% 혹은 그 이상의 제조 공정이 아웃소싱 되고 있다. 세포‧ 유전자치료제 개발 기업의 65%가 소규모 바이오기업이기도 하지만, 무엇보다 세포‧ 유전자치료제의생산과 공급에는 특화된 공정 기술과 설비가 필요하고 제조와 치료제 투여까지의 전 과정에 복잡
한 물류가 수반되어 CDMO에 대한 의존성이 더 큰 것으로 보인다.2)
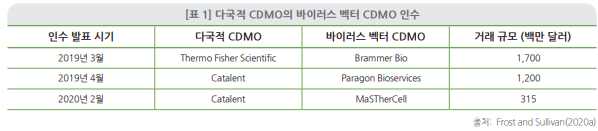
이에 발맞추어 세포·유전자치료제 제조 역량 강화를 위한 CDMO 기업 간 통합이 활발히 이뤄지고 있다. 우선 세포·유전자치료제의 end-to-end 서비스 제공 역량을 확보하기 위해 다국적 제약사들이 바이러스 벡터 개발 및 제조 전문 CDMO를 인수하고 있다. Thermo Fisher Scientific이 2019년 3월 Brammer Bio를 인수했으며 Catalent는 2019년 4월 Paragon Bioservices와
2020년 2월 MaSTherCell을 인수했다.
환자맞춤형인 세포·유전자치료제의 특성에 맞추어 치료장소에서 가까운 생산이 요구됨에 따라 Lonza는 유럽에서의 생산기반 구축을 위해 2017년 네덜란드 소재 세포·유전자치료제 CDMO PharmaCell을 인수했다.
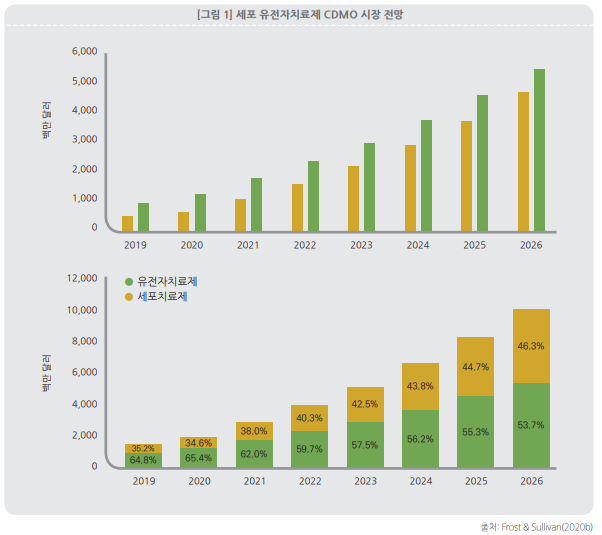
세포‧ 유전자치료제 CDMO 시장은 2019년 기준 15억 2,460만 달러에서 연평균 31.0% 성장해 2026년 101억 1,340만 달러에 이를 것으로 전망된다. 성장 속도는 세포치료제 시장이 더 빠를 것으로 보인다. 2019년에서 2026년 사이 세포치료제 시장의 5억 3,740만 달러에서 연평균36.2%로 성장해 46억 8,420만 달러에, 유전자치료제 시장은 9억 8,720만 달러에서 연평균27.6% 성장해 54억 2,920만 달러에 이를 것으로 기대된다.
2019년에서 2026년 사이 전체 세포‧ 유전자치료제 CDMO 시장 대비 유전자치료제가 차지하는 비중은 64.8%에서 53.7%로 줄
어들고 세포치료제가 차지하는 비중은 35.2%에서 46.3%로 증가할 전망이다.3)
세포·유전자치료제의 성장에 따라 바이오제조 시스템에 변화가 일어나고 있다. 재조합단백질이 나 단일클론항체와 같은 이전의 바이오의약품이 비교적 구조가 규정된 단백질을 재료로 했다면 세포·유전자치료제는 더 복잡하고 다변수(multivariate)의 역동적인 세포를 재료로 한다.4)
또한 대부분 환자 맞춤형으로 환자별 소규모 생산이 필요하다. 이런 특성으로 인해 세포·유전자치료제 의 생산은 기존 바이오제조 시스템에서 3가지 문제를 보인다.5) 품질(quality) 관점에서 기존 개방형 제조공정은 조작(manipulation) 단계가 많아질수록 오염의 위험성이 커지는데, 세포치료제 생산을 위한 세포 변형 과정은 증식과 여과, 정제, 동결보존 등 여러 단계로 이뤄지기 때문에 수동적 개입과 배양액 교체 등으로 인한 오염의 위험성이 높아진다.
양적(quantity) 관점에서 기 존 제조 공정은 생산량이 제한적인 소규모 단위 공정으로 유연성과 규모 가변성(scalability)이 부
족하다. 효율성 측면에서 기존의 개방형 수동식 생산 공정은 매우 노동집약적이고 개입이 많아 생산 비용을 높이고 그에 따라 전체적인 치료 비용을 높인다.
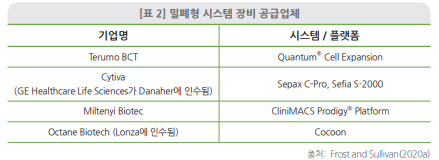
세포·유전자치료제 분야는 위와 같은 문제의 해결을 위해 장비(equipment) 간 연결성을 기반으로 확장 기술에 초점을 맞춘 자동화된 밀폐형(automated closed) 시스템을 도입하고있다. 우선 대부분의 단위 공정이 밀폐형 시스템으로 진행되면 감염에 의한 잠재적인 배치(batch) 손실을 줄일 수 있다.
또한 자동화된 밀폐형 시스템은 여러 장소에서 제조된 치료제 간의 동등성을 확립하고 유지할 수 있게 해준다. 특히 자가유래(autologous) 세포·유전자치료제의 경우 환자 특화된 요구사항과 투입 재료의 가변성으로 인해 공정의 유연성과 모듈화
가 핵심 동력이 될 것으로 보인다.

향후 자동화된 밀폐형 시스템을 기반으로 생산 설비의 모듈화가 확대되면 세포·유전자치료제 개발 기업이 여러 환자별 치료제를 혹은 세포·유전자치료제 CDMO가 여러 기업별 치료제를 효율적으로 생산할 수 있게 될 것으로 기대된다. 동시에 모듈화된 자동화 생산 시스템은 신속한 제조와 환자 투여가 가능한 시스템의 탈중앙화(decentralization), 즉 환자 치료 현장에서의 생산 시스템 실현도 뒷받침할 것으로 기대된다.
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보


 [bio economy brief] 123호_바이오제조 동향_세포유전자치료제 ...
[bio economy brief] 123호_바이오제조 동향_세포유전자치료제 ...