산업동향
재생의료 산업 및 임상동향
- 등록일2022-05-11
- 조회수5055
- 분류산업동향 > 제품 > 바이오의약
-
자료발간일
2022-05-01
-
출처
한국바이오협회
- 원문링크
-
키워드
#한국바이오협회#재생의료#첨단바이오의약품
- 첨부파일
재생의료 산업 및 임상동향
- 첨단바이오의약품을 중심으로
◈목차
글로벌 재생의료 임상 현황
글로벌 재생의료 신약개발 승인 현황
글로벌 재생의료 투자의 급증
국내 첨단바이오의약품 개발 현황
맺음말
◈본문
재생의료(Regenerative medicine)란 손상된 세포와 조직, 장기 등을 대체하거나 원래의 기능을 할 수 있도록 복원시키는 의학분야로서, 알츠하이머, 척추손상, 당뇨 등 적절한 치료방법이 없는 난치성 질환의 근본적 치료대안으로 부각되고 있다. 최근 재생의료 산업은 기존 세포, 조직을 기반으로 하는 ‘재생의료’ 개념에서 혁신적 치료기술을 융합하는 ‘첨단재생의료’라는 새로운 패러다임으로 전환되고 있으며, 세포치료, 유전자치료, 조직공학치료 및 융복합 치료 등을 포함하고 있다.
재생의료연합(Alliance for Regenerative Medicine) 2021년 기준 최근 자료에 따르면, 전 세계적으로 1,171건의 임상이 이루어지고 있으며, 이 중 142건이 임상 3상 진행 중에 있다. 특히, 미국식품의약국(FDA)과 유럽의약품청(EMA)에 따르면 2025년까지 각 기관별 연 10~20건의 세포 및 유전자 치료제가 승인 받을 것으로 예상되어, 재생의료 시장 규모는 2021년 기준 147억 달러에서 향후 2027년까지 504억 달러로 크게 성장하며 확대 될 것으로 보인다.
이처럼 재생의료 시장의 성장 가능성이 높은 이유는 미국, 유럽 등 선진국 규제기관에서 신속허가 절차 지원 ‘패스트트랙’ 제도 활성화를 통해 제품의 파이프라인 개발을 뒷받침하고 있기 때문이다. 국내에서도 치료법이 없는 난치질환 환자들을 위해 첨단바이오의약품의 합리적 허가·심사 체계를 마련함에 따라 신속허가 제도를 활성화 할 전망이다. 본 브리프에서는 첨단바이오의약품을 중심으로 한 재생의료 산업 및 임상 동향에 대해 살펴본다.

글로벌 재생의료 임상 현황
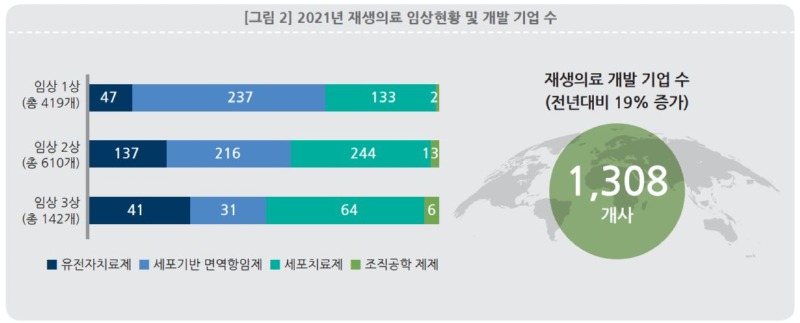
글로벌 재생의료 개발 기업 수는 유전자, 세포 및 조직 기반 치료제 기업을 모두 포함하여 2021년 기준 총 1,308개사로 파악된다. 현재 전세계적으로 1,171건의 임상이 이루어지고 있으며, 그 중 142건(12%)이 임상 3상 진행중에 있다. 치료제 기전별로 살펴보면, 유전자 치료제 225건, 세포기반 면역항암제 484건, 세포 치료제 441건, 조직 공학제제 21건이다.
전체적으로, 세포기반 면역항암제(Cell-based immuno-oncology)의 비중이 41%로 가장 큰 비중을 차지하는 것으로 나타났다. 이는 항암 면역 치료 요법으로 불리며, 최근 면역 관문 억제제(checkpoint inhibitor), CAR-T 세포 치료 등 몇몇 항암 면역치료 요법이 임상적으로 큰 효과가 있음이 알려지게 되었고, 기존 화학 요법이나 방사선 치료요법으로는 치료할 수 없는 암에도 적용가능하다는 큰 장점이 있어서 주목을 받게 되었다.
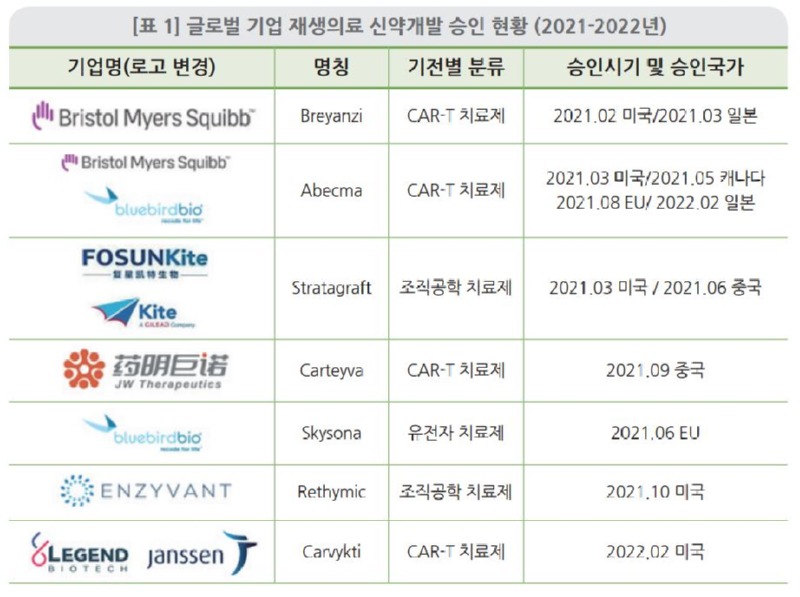
글로벌 재생의료 신약개발 승인 현황
2021년 기준 미국, 유럽, 중국 전역에서 6개의 재생의료 관련 신약이 승인되었으며, 2022년 2월에는 Legend Biotech & Janssen의 다발성 골수종 대상 CAR-T 치료제인 CARVYKTI™ (ciltacabtagene autoleucel)가 승인되었다. CAR-T 치료제 분야에서 2021년 기준으로는 Abecma, Breyanzi와 Carteyva 등 3개가 승인되었다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보
지식


 [브리프_issue 53] 재생의료 산업 및 임상 동향-첨단바이오의약품...
[브리프_issue 53] 재생의료 산업 및 임상 동향-첨단바이오의약품...