BioINwatch
(BioIN + Issue + watch) : 바이오 이슈를 빠르게 포착하여 정보 제공나노바디, 코로나19 치료제로서의 새로운 활용 가능성 및 전략 제시
- 등록일2021-02-18
- 조회수5424
- 분류레드바이오 > 의약기술, 플랫폼바이오 > 바이오기반기술
-
발간일
2021-02-18
-
키워드
#코로나19#나노바디#COVID-19# Nanobody
- 첨부파일
-
차트+
?
차트+ 도움말
BioINwatch(BioIN+Issue+Watch): 21-12
나노바디, 코로나19 치료제로서의 새로운 활용 가능성 및 전략 제시
◇ 국제 연구팀, 코로나19 바이러스의 돌기 단백질(spike protein)을 표적으로 항원 중화도가 100배 이상 향상된 4종의 중화 나노바디 단백질 연결체 개발에 성공. 향후 코로나19 치료제로서 가능성 기대
▸주요 출처 : Science, ‘Structure-guided multivalent nanobodies block SARS-CoV-2 infection and suppress mutational escape’, 2021.01.
□ 전 세계적으로 다양한 방식의 코로나19 대응을 위한 시도가 추진 중
○ 최근 mRNA·재조합 단백질·바이러스 벡터 등 다양한 종류의 코로나19 백신의 성공적인 개발 소식이 보고
○ 하지만 이와는 별도로 코로나19에 감염된 환자 치료 및 백신 효과가 제한적인 低면역력의 잠재적 위험군의 감염 및 증상 악화 차단을 위해서는 효과적인 코로나19 치료제 개발이 필수
- 이러한 목적에서 바이러스 병원성 단백질을 무력화시키는 ‘중화 항체’의 장점은 유지하면서 생산의 어려움, 비싼 가격 등의 단점을 극복할 수 있는 새로운 전략으로서 ‘나노바디(Nanobody)’ 주목
나노바디 개요
나노바디(Nanobody)는 낙타과 동물(낙타, 라마, 알파카)에서 발견되는 단일 사슬 항체의 항원 인식 가변 부위(variable region)를 분리하여 제조
나노바디(~14kDa, 단일 도메인)는 일반적인 항체(~150 kDa, 12개 도메인)에 비해 구조가 단순하고 크기가 작아서 구조적 안정성이 높고 정제와 생산이 용이
또한 온도, 산성도 등 환경 요인에 대하여 저항성이 강하며 단백질 엔지니어링을 통한 구조적, 기능적 변환 역시 상대적으로 용이하여 의학 및 산업적으로 높은 잠재적 활용성을 보유
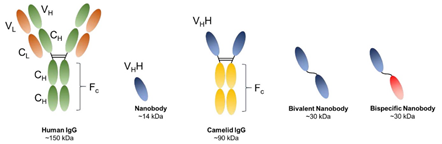
출처 :Progess in Biomedical Engineering, ‘The magic bullet as cancer therapeutic-has nanotechnology failed to find its mark?’ 2020.09
□ 이러한 장점을 활용하여 코로나19 바이러스 단백질을 표적으로 하는 ‘새로운 중화 나노바디’ 개발
○ 독일 본 대학, 스웨덴 카롤린스카 연구소, 미국 일리노이 대학 연구팀이 참여한 다국적 연구팀은 코로나19 바이러스의 스파이크 단백질을 표적으로 하는 4종*의 중화 나노바디를 발굴하는데 성공
- 라마와 알파카에 코로나19 바이러스의 스파이크 단백질(spike protein)의 수용체 결합 도메인(receptor-binding domain, RBD)을 주입하여 면역반응을 통해 나노바디 형성
* VHH E, VHH U, VHH V, VHH W
○ 또한, X-선 결정학 기법 및 극저온 전자 현미경(cryo-EM)을 통해 코로나19 바이러스 RBD, 스파이크 단백질과 중화 나노바디가 결합한 복합체 3차 구조를 규명하였으며,
- 중화 나노바디가 바이러스 단백질이 실제 표적인 인간 수용체 단백질과 결합하는 것을 경쟁적으로 방해한다는 것을 확인
< 바이러스의 수용체 결합 도메인(RBD)이 나노바디와 결합한 복합체 3차 구조(X-선) >
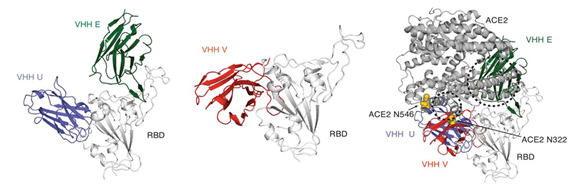
< 바이러스의 스파이크 단백질이 나노바디와 결합한 복합체 3차 구조(cryo-EM) >
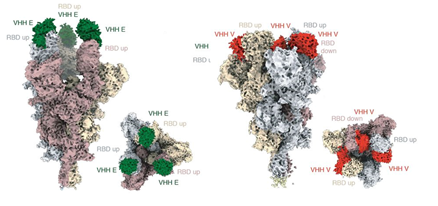
출처 : Science, ‘Structure-guided multivalent nanobodies block SARS-CoV-2 infection and suppress mutational escape’, 2021.01.
※ X-선 결정학 : 단백질 분자가 규칙적으로 배치된 단백질 결정에 X-선을 조사하여 나타나는 회절(diffraction) 현상을 이용하여 3차 구조를 분석. 지금까지 규명된 단백질 3차 구조의 90% 이상을 규명한 가장 보편적이고 널리 사용되는 방법이나, 3차 구조 규명을 위해서는 반드시 단백질 결정을 만들어야 한다는 단점이 있음
※ 극저온 전자현미경(cryo-EM) : 단백질 결정 없이 수용액 내 정제 단백질의 3차 구조를 볼 수 있다는 장점이 있으며, 2013년을 기점으로 해상도가 급격히 좋아지면서 새로운 단백질 3차 구조 규명 기법으로 크게 각광 받고 있음. 다만 아직까지 해상도 면에서 X-선 결정학에 미치지 못하며, 규명 가능한 단백질 크기의 하한선이 존재(최소 80 kDa 이상, 보편적으로는 300 kDa 이상)
□ 연구팀은 나노바디의 연결체 제작을 통한 중화 효과의 극대화를 확인
○ 연구팀은 두 종류의 나노바디를 연결하여 결합력을 9~22배, 중화력을 63~119배 증가시킨 이중 나노바디 연결체를 제작하였으며,
- 나노바디 연결체는 바이러스 스파이크 단백질의 구조 변환을 차단하여 수용체 단백질과의 결합 및 바이러스 칩입을 억제함을 확인
- 코로나19 바이러스 스파이크 단백질을 조기 활성화(premature activation) 상태로 만드는데, 이는 바이러스가 인체세포 칩입에 필수적인 스파이크 단백질의 정상적인 단계적 구조 변환을 차단
○ 또한 항원 인식기가 다른 나노바디/항체를 연결하는 것이 바이러스 중화 효과를 월등하게 향상시키는 새로운 전략임을 입증
영국 연구팀, ‘인공 나노바디’로 코로나19 치료 효과 입증
영국 옥스퍼드, 레딩 대학, 다이아몬드 방사광 가속기 연구소 등이 참여한 공동 연구팀은 코로나19 바이러스의 스파이크 단백질을 표적하는 나노바디를 제작
- 연구팀은 코로나19에 감염된 라마의 회복기 혈청에서 효과적인 항체를 발굴하였으며 이를 기반으로 나노바디를 제작
H11-D4, H11-H4로 이름 붙인 2종의 나노바디가 바이러스 스파이크 단백질의 RBD와 결합하여 인간 ACE2 수용체 단백질과의 결합을 차단하는 것이 확인
- 옥스퍼드 대학의 레이 오웬스(Ray Owens) 교수는 “오래지 않아 코로나19 환자를 위한 초기 치료제가 등장할 것”으로 전망
* 주요 출처 : Nature Structural & Molecular Biology, ‘Neutralizing nanobodies bind SARS-CoV-2 spike RBD and block interaction with ACE2’, 2020.07; The Science Times, ‘인공 나노바디’로 코로나19 치료‘, 2020.07
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
지식
동향
- 산업동향 일본 코로나 등 진단키트 시장 동향 2024-11-25
- 정책동향 코로나바이러스감염증-19 접촉추적격리 정책 국제 비교 및 정책 효과 시뮬레이션 연구 2024-08-16
- 제도동향 코로나바이러스감염증-19 발생 이후 국가병원체자원은행 병원체자원 분양 현황(2020–2023년) 2024-07-24
- 정책동향 코로나바이러스감염증-19 대유행 대응 거버넌스 변화와 정책에 관한 고찰 (2020년 1월–2021년 12월) 2024-02-07
- 기술동향 만성 코로나19 증후군(Long COVID)의 증상 및 관련 연구 동향 2024-01-23


 BioINwatch21-12(2.18)●나노바디 코로나19 치료제로서 새로운 활...
BioINwatch21-12(2.18)●나노바디 코로나19 치료제로서 새로운 활...
 나노바디 개요
나노바디 개요