BioINwatch
(BioIN + Issue + watch) : 바이오 이슈를 빠르게 포착하여 정보 제공프로그래밍이 가능한 치료용 박테리아 플랫폼
- 등록일2022-12-07
- 조회수2996
- 분류생명 > 생명과학, 생명 > 생물공학
-
발간일
2022-12-06
-
키워드
#박테리아#플랫폼
- 첨부파일
-
차트+
?
차트+ 도움말
프로그래밍이 가능한 치료용 박테리아 플랫폼
BioINwatch(BioIN+Issue+Watch): 22-83
◇ 생물학적 조절 원리에 대한 수십 년간의 연구를 통해 CAR-T와 같이 세포의 맞춤화가 가능해졌는데, 최근 Science에서는 특정 신호에 적절하게 응답하는 논리회로로 세포를 프로그래밍할 수 있다는 점을 주목하며 세포 공학(Cell engieering)에 관한 특집호를 발표. 그 중에서 합성생물학 도구를 활용하여 프로그래밍이 가능한 치료용 박테리아 플랫폼을 이슈로 다룸 ▸주요 출처 : Science, Engineering bacteria as interactive cancer therapies, 2022.11.24 |
❏합성생물학 도구는 치료용 박테리아의 유전자 회로를 변경하여 프로그래밍이 가능한 의약품(programmable medicines)이라는 새로운 개념을 구축
○ 박테리아는 단독으로도 면역자극성이고 종양에 대한 면역반응을 유도할 수 있지만, 종양 탐지 및 치료를 개선하기 위해 박테리아 단일 제제로 또는 다른 기술과 조합하여 조작할 수 있는 다목적 플랫폼으로 활용 가능
※ 박테리아는 19세기에 Streptococcus pyogenes와 Serratia marcescens를 주사한 환자에서 관찰된 종양 퇴행의 증거와 함께 잠재적인 암 치료법으로 처음 확인
※ 그 당시에는 알려지지 않았지만 박테리아는 면역자극제로서 종양에 대한 면역 반응을 유도하고 저산소 및 면역억제 종양 미세환경(tumor microenvironments, TME)에서 성장 가능
- Salmonella, Escherichia, Clostridium, Bifidobacterium, Proteus 및 Lactobacillus와 같은 여러 속의 박테리아가 이러한 특성을 입증하며 종양 표적 매개체로서의 유용성을 제안
○ 합성생물학 도구를 통해 박테리아 고유의 면역원성을 변경하고, 추가적인 치료물질을 생산할 수 있도록 리프로그래밍이 가능
- 저분자물질, 독소, 면역조절제, 효소, siRNA(small interfering RNAs) 및 나노바디 등 전신에 투여될 경우 독성이 될 수 있는 여러 종류의 탑재(치료)물질을 암호화하고 국소적으로 전달하도록 박테리아를 유전적으로 리프로그래밍
- 또한 자기공명영상(MRI) 및 집속초음파(FUS)와 같은 이미징기술을 접목하여 박테리아 감지 및 작동, 탑재물질 생산 및 방출을 조절
○ 합성생물학 도구는 치료용 박테리아의 유전자 회로를 변경하여 치료의 공간적, 시간적 제어가 가능하도록 지원
- 합성 유전자회로는 박테리아가 다른 생물 및 이미징기술 등과 보다 효과적으로 상호작용할 수 있도록 설계
박테리아-종양 인터페이스 공학(Engineering the bacteria-tumor interface)
○ (종양 표적화) 종양 내 환경에서 박테리아의 성장을 증가시키거나 암세포에 대한 친화성을 높이는 방식으로 박테리아의 종양 특이성을 향상
- 고농도의 젖산(lactate), 저농도의 산소, 낮은 pH 등과 같은 종양 내 환경에서 잘 자랄 수 있도록 유전자회로를 도입
- 이러한 감지회로는 종양 환경 신호에 반응하기 때문에 박테리아가 종양에서만 성장할 수 있도록 제한
※ 종양 외 다른 조직이 종양 환경 신호 중 하나를 포함할 수 있기 때문에 "AND" 논리 게이트를 통해 감지회로를 결합하면 종양 특이성이 더욱 향상되고 박테리아 돌연변이 탈출 사례가 줄어들어 장기간 생물학적 봉쇄가 가능
- 박테리아는 종양 세포에 보다 특이적으로 결합할 수 있도록 박테리아 세포 표면에 종양 표적 단백질을 발현하도록 조작
< 박테리아-종양 인터페이스 엔지니어링 개념도 >
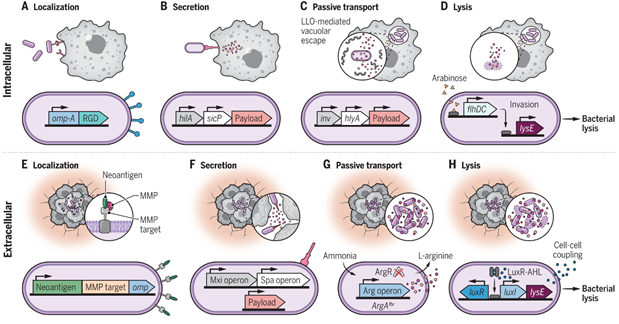
¶ 합성생물학 접근법으로 박테리아의 유전자 회로를 변경하여 세포 내로 치료물질을 전달하는 과정(A∼D), 세포 외에서 종양을 공격하는 과정(E∼H)
출처 : Science, Engineering bacteria as interactive cancer therapies, 2022.11.24.
○ (세포 내 전달) 살아있는 치료제로서 박테리아는 자율적 제어, 감지 및 내재화 과정을 통해 그동안 세포 내 전달이 어려웠던 핵산, 단백질 등의 치료물질을 전달 가능
- S. typhimurium(살모넬라 티피무리움)은 고유의 분비 시스템인 T3SS(type 3 secretion system)*을 사용하여 종양세포로 일련의 치료물질을 전달
* T3SS는 S. typhimurium과 같은 그람 음성 박테리아에서 발견되는 다중 분비 시스템 중 하나로, 바늘 모양의 복합체가 박테리아의 단백질을 숙주세포의 세포질로 직접 주입
- 또한 S. typhimurium는 액포(Salmonella-containing vacuole, SCV)를 통해 숙주의 종양세포 내로 들어가 복제도 가능
- 합성생물학 접근법은 박테리아의 약물 방출을 공간 및 시간적으로 제어할 수 있는데, 예를 들어, 파지(phage) 유래 용해 유전자를 S. typhimurium에 도입하여 용해 유전자의 전사를 일시적으로 일으켜 용해된 박테리아에서 약물이 방출되도록 설계
- "세포 내 전달(intracellular delivery, ID) 살모넬라" 플랫폼은 종양세포 내 효소(phosophatase 1 holoenzymes) 억제 약물을 효과적으로 전달하여 종양을 완화하는 데 활용
○ (세포 외 전달) 세포 외 공간은 박테리아가 고밀도로 성장할 수 있어 더 많은 치료물질을 생성하고 종양 공간 전체에 확산하여 암을 치료
- 세포 외 전달 전략은 프로바이오틱 균주인 E. coli Nissle 1917(EcN)과 같은 비침습성 박테리아를 활용할 수 있는 기회를 제공
- EcN는 타 박테리아 유래의 분비 시스템(Shigella-derived type 3 secretion apparatus)을 암호화하도록 조작하여 치료물질이 세포 외 공간에 분비되도록 설계
- Quorum sensing(QS)를 사용하는 유전자회로는 세포 외 종양 환경에서만 박테리아가 고밀도 성장할 수 있도록 제어하며, 박테리오파지 유래 용해 유전자를 QS 제어 하에 두어 박테리아 증식, 용해 및 치료물질의 세포 외 공간으로의 방출을 조절
- QS 접근법은 박테리아를 종양 부위에 국한하여 지속적으로 치료물질을 전달할 수 있도록 공간 및 시간을 제어할 수 있으며, 또한 순차적인 유전자 발현을 유도하는 회로를 통해 여러 치료물질이 순차적으로 방출될 수 있도록 조정 가능
면역체계 리프로그래밍(Reprogramming the immune system)
○ (선천 면역 리프로그래밍) 종양 내 모여 증식하는 박테리아는 단핵구, 대식세포 및 호중구 등 면역세포 모집 및 활성화를 통해 선천적 면역을 유도
- 선천적 면역세포는 종양 내 군집을 이룬 박테리아의 용해, 제거 등 식균작용(phagocytosis)을 통해 사이토카인 반응도 유도
- 선천적 면역반응이 계속됨에 따라 항원제시세포(antigen-presenting cells, APC)가 종양 안으로 들어가서 파괴된 종양세포와 박테리아를 포집하여 항종양 반응을 더 강하고, 정확하게 조절할 수 있는 추가 상호작용을 제공
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
지식
- BioINwatch 바이오신약 개발을 혁신할 AI 단백질 언어 모델 2025-02-14
- BioINwatch 맞춤형 ASO 치료제 개발에 유연성과 확장성을 제공하는 오가노이드 플랫폼 2025-02-06
- BioINpro [첨단 바이오 연구장비] UK Biobank: 글로벌 연구협력을 위한 플랫폼 2024-10-15
- BioINwatch End-to-End 생성형 AI가 설계한 약물의 임상 2상 결과가 곧 발표될 예정 2024-07-30
- BioINregulation 바이오 분야 이머징 이슈 분석 및 디지털 플랫폼 활용 방안 2024-07-25
동향


 BioINwatch22-83(12.6)●프로그래밍이 가능한 치료용 박테리아 플...
BioINwatch22-83(12.6)●프로그래밍이 가능한 치료용 박테리아 플...
 박테리아-종양 인터페이스 엔지니어링 개념도
박테리아-종양 인터페이스 엔지니어링 개념도