BioINpro
(BioIN + Professional) : 전문가의 시각에서 집필한 보고서 제공[바이오의약을 중심으로 ②] 암백신, 항체단편, 백신제제 분야의 최신 기술 트렌드 및 산업동향
- 등록일2009-06-17
- 조회수15716
- 분류레드바이오 > 의약기술, 제품 > 바이오의약
-
저자/소속
김태억/대덕특구지원본부
-
발간일
2009-06-17
-
키워드
#바이오의약을 중심으로#암백신
Bioin 이슈&특집 2009년 Vol.03 [바이오의약을 중심으로]
암백신, 항체단편, 백신제제 분야의 최신 기술 트렌드 및 산업동향
김태억(경제학박사) 대덕특구지원본부
* 위 자료를 시작으로 바이오분야의 기술사업화와 관련한 자료를 각각의 주제를 가지고 격월로 제공 할 예정입니다. 첫번째로 <바이오의약을 중심으로> 관련하여 5개의 시리즈로 자료를 제공합니다.
◈ 발간시리즈 순서 ◈
[바이오의약을 중심으로 총괄요약]
[바이오의약을 중심으로 ①] 바이오시밀러를 중심으로 본 2009년 바이오의약 산업의 트렌드 분석
[바이오의약을 중심으로 ②] 암백신, 항체단편, 백신제제 분야의 최신 기술 트렌드 및 산업동향
[바이오의약을 중심으로 ③] 2000년대 바이오의약 산업의 현황과 과제
[바이오의약을 중심으로 ④] 바이오기업 펀딩 트렌드
[바이오의약을 중심으로 ⑤] 바이오시밀러 산업동향과 국내기업의 진입전략
FDA의 바이오의약 승인현황과 향후 전망
FDA는 2008년 21개의 신규분자물질에 대한 승인을 내주어 2004년 36개의 NME를 승인했던 한 해를 제외하고는 2000년 이후 점진적으로 하락하고 있던 신물질 승인율에 상승반전을 기록하게 만들었다.
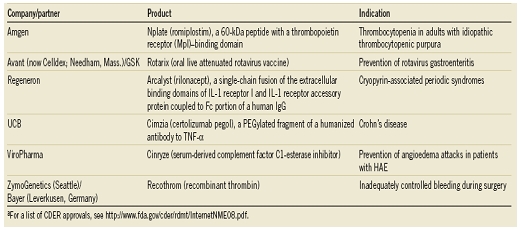
FDA가 2008년에 승인한 바이오신약, NB, Feb, 2009
2007년에는 생물학적제제 2개를 포함한 18개의 NME 승인이 이루어졌고, 2008년에는 총 80개의 NDA와 BLA가 승인이 되었는데, 이들중 대부분은 이미 승인된 물질의 포뮬레이션을 변경하거나 혹은 처방방식의 개조와 관련된 것들이다. 이러한 결과는 어느 정도는 안전성 검증 조건이 훨씬 강화된 2007년의 FDA 시행령 개정안에 영향을 받은 것으로 볼 수 도 있다.
특히 위험평가와 완화전략이라고 번역되는 REMS 메카니즘의 경우는 포스트 마케팅 연구를 넘어서 알려져 있거나 잠재적으로 위험하다고 판단되는 약물이나 생물학적제제에 대한 감시체계를 구축하는 것으로 목표로 하고 있다. 이 메카니즘은 실제 적용을 위한 광범위한 데이터베이스 구축작업에 들어가 있는데 환자, 의사, 그리고 치료제간의 상호작용 등을 포함하는 것으로서 데이타베이스 구축을 위해서는 오랜시간과 대규모의 예산이 필요하다.
................계속
* 로그인 하셔야 자세한 정보를 모두 보실 수 있습니다.
-
이전글
- [바이오의약을 중심으로 ③] 2000년대 바이오의약 산업의 현황과 과제
-
다음글
- [바이오의약을 중심으로 ①] 바이오시밀러를 중심으로 본 2009년 바이오의약산업의 트렌드 분석
지식

