제도동향
천연물신약 임상시험 진입 활성화 기대 !
- 등록일2010-11-01
- 조회수13013
- 분류제도동향 > 종합 > 종합
-
자료발간일
2010-11-01
-
출처
식품의약품안전청
- 원문링크
-
키워드
#천연물신약
- 첨부파일
천연물신약 임상시험 진입 활성화 기대 !
- 비임상자료 면제범위와 제출시기 합리화 -
□ 천연물신약의 비임상시험 자료제출시기와 면제범위가 합리화됨에 따라 앞으로 개발업체의 임상시험 진입이 활성화될 것으로 보인다.
※ 비임상시험자료 : 동물 등을 이용하여 의약품 등의 안전성을 평가하는 시험으로 의약품의 허가 및 임상시험 승인신청 시 필요한 자료. 통상 1년 반에서 2년 정도 소요
□ 식품의약품안전청(청장 노연흥) 국내 천연물신약의 임상시험 진입 활성화를 위해 「생약·한약제제 비임상시험자료 제출기준」을 마련하여 발표하였다.
○ 천연물신약 개발은 선발품목인 스티렌정(동아제약)이 의약품 품목별 생산량 4위, 1,000억원의 매출을 보이는데 힘입어
○ 현재 약 60여개 품목이 임상시험 진행 중이며 지난해 대비 올해 임상시험 승인은 43% 증가한 것으로 나타났다.
□ 금번 비임상시험자료 제출기준의 골자는
○ 비임상시험 자료범위 차등화
- 후보물질의 인체 사용경험 등에 따라 독성시험자료의 범위가 면제·부분면제·제출로 구분되며, 전통적인 복용방법인 물추출물이나 한방의료기관에서 임상적으로 사용하던 제품 등은 앞으로 독성시험자료를 면제할 계획이다.
○ 임상시험 단계 별 비임상시험자료 제출시기 합리화
- 초기 탐색적 임상시험(2상)에서 제출해야할 일부 비임상자료를 확증적 임상시험(3상) 승인 시 제출할 수 있도록 하고 있다.
□ 식약청은 이와 같은 합리와 조치로 비임상시험 기간이 현재의 절반 수준으로 단축될 수 있어 임상시험을 통한 효율적 약효탐색이 가능할 것으로 기대한다고 밝혔다.
<첨부> 1. 최근 5년간 천연물신약 임상시험 승인 현황(2010.10 현재)
2. 개발단계별 임상시험
<첨부>
1. 최근 5년간 천연물신약 임상시험 승인 현황(2010.10 현재)
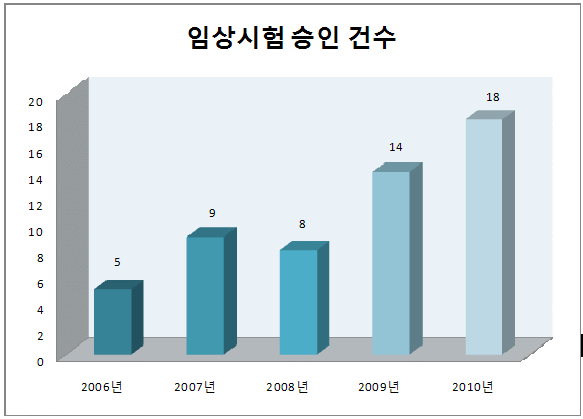
2. 개발단계별 임상시험
|
임상시험의 종류 |
임상시험의 목적 |
예 |
|
임상 약리 시험 (제1상) |
· 내약성 평가 · 약동학과 약력학 정의/서술 · 약물대사와 상호작용 조사 · 치료효과 추정 |
· 용량-내약성 임상시험 · 단독과 반복 투여에 따른 약동학/약력학 임상시험 · 약물 상호작용 임상시험 |
|
치료적 탐색 임상시험 (제2상) |
· 목표 적응증에 대한 탐구 · 후속 시험을 위한 용량 추정 · 치료확증 시험을 위한 시험설계, 평가항목, 평가 방법에 대한 근거 제공
|
· 대리 약리학적 평가 또는 임상적 평 소수의 환자에서의 비교적 단기간 에 걸친 초기 임상시험 · 용량반응 탐색 임상시험 |
|
치료적 확증 임상시험 (제3상) |
· 유효성 입증/확증 · 안전성 자료 확립 · 임상적용을 위한 이익과 위험의 상대평가 근거 제공 · 용량과 반응에 대한 관계 확립 |
· 유효성 확립을 위한 적절하고 잘 통제된 임상시험 · 무작위 배정에 의한 용량반응 임상 시험 · 안전성 임상시험 · 이환율/사망률을 위한 임상시험 · 비교적 간단한 대규모 임상시험 · 대조군을 이용한 비교 임상시험 |
|
치료적 사용 임상시험 (제4상) |
· 일반 또는 특정 대상군/환경에서 이익과 위험에 대한 이해 · 흔하지 않은 이상반응 확인 · 추천되는 용량을 확인
|
· 대조군을 이용한 유효성 임상시험 · 이환율/사망률에 대한 임상시험 · 부가적인 평가 항목에 대한 임상시험 · 비교적 간단한 대규모 임상시험 · 약물경제학적 측면의 임상시험 |
※천연물신약 개발은 일반적으로 치료적 탐색시험(2상)부터 시작됨
-
이전글
- 유헬스케어 의료기기, 시장 진입 준비 완료!
-
다음글
- Synthesis report on code of conduct, voulutary measures and practices towards a responsible development of N&N
지식
동향


 천연물신약_ 임상시험진입_활성화기대.hwp
천연물신약_ 임상시험진입_활성화기대.hwp