제도동향
2024년 US FDA 허가 신약들과 전망
- 등록일2025-02-18
- 조회수1408
- 분류제도동향 > 레드바이오 > 의약기술
-
자료발간일
2025-01-23
-
출처
한국보건산업진흥원
- 원문링크
-
키워드
#2024#FDA#신약
2024년 US FDA 허가 신약들과 전망
[보건산업브리프 Vol.430]
◈ 목차
Ⅰ. 연구 배경
Ⅱ. 2024년 미국 FDA 허가 신약
Ⅲ. 주목할 만한 신약 3가지
Ⅳ. 주목할 만한 신약개발 기업 3개사
Ⅴ. 요약 및 분석
Ⅵ. 참고문헌
◈본문
Ⅰ. 연구 배경
◉︎2024년 세계 의약품 시장은 약 1조 5,787억 달러(매출액 기준)로 예상되며, 그 중 미국 의약품 시장의 규모는 전체의 약 30.1%인 약 4,746억 달러로 압도적으로 큰 시장을 형성하고 있음
●US FDA 허가는 신약의 글로벌 의약품 시장에서 블록버스터가 되기 위한 기점이라고 할 수 있으며, 신약개발의 최신 글로벌 동향을 확인할 수 있는 중요한 정보로 평가됨
−︎2024년 US FDA의 CDER(Center for Drug Evaluation and Research)는 50개의 신약을 허가했고, 이중 합성신약인 NDA(New Drug Application)는 36건, 바이오신약인 BLA(Biologics License Application)은 14건이었음
◉︎본 보고서는 2024년 미국 FDA 시판 허가를 받은 신약들에 대해 살펴보면서, 글로벌 신약개발의 동향 변화를 파악하고 국내 신약개발 기업들에게 줄 수 있는 시사점을 도출해 보고자 함
●미국 FDA 신약 중 주목할 만한 의약품과 신약개발 기업, 향후 상업적 성공 전망과 개발 과정에서 고려해 볼 필요가 있는 부분들을 중점으로 살펴보았음
Ⅱ. 2024년 미국 FDA 허가 신약
◉︎2024년 12월 31일 기준, US FDA CDER는 1년간 총 50개 신약을 허가했는데, 이는 2023년 55개의 신약을 허가한 것에 비하면 다소 줄어들었으나, 2019~2023년 5년 평균치(48.6개)보다 조금 높은 수준
●50개 허가 의약품 중에서 바이오신약은 15개로 전체의 30.0%였으며, 이전 2019년부터 2023년 5년 평균치 28.4%보다는 다소 높았음
< 표 1 > 미국 FDA 허가 신약(NME)과 바이오신약(BLA)의 수

출처 : US FDA CDER 홈페이지
< 표 2 > 2024년 미국 FDA CDER 승인 의약품 목록


자료 : US FDA 홈페이지
◉︎기업별로는 AstraZeneca, Pfizer, MSD 등 글로벌 빅파마(Big Pharma)들의 신약 허가가 다수 있었으나, 2개 이상의 신약 승인을 받은 기업은 Eli Lilly와 Roche에 불과했음
●2024년 US FDA 신약 허가를 받은 50개 의약품 중에서 2023년 매출액 기준 글로벌 Top 30 내의 빅파마가 개발한 제품은 14개로 전체의 28.0%에 불과했으며, 이는 2023년 38.2%과 2022년 37.8%에 비해 크게 줄어든 수치임
−︎상대적으로 중소제약기업(Small and Medium-sized Enterprise, SME)의 비중은 늘었는데, 설립된 지 얼마 되지 않은 Day One Biopharmaceuticals(2018년 설립), X4 Pharmaceuticals(2014년 설립), Botanix Pharmaceutical(2015년 설립) 등이 처음으로 US FDA 신약 개발 기업에 이름을 올림
< 표 3 > 2015년 이후 미국 FDA 신약 기업 중 빅파마 비율
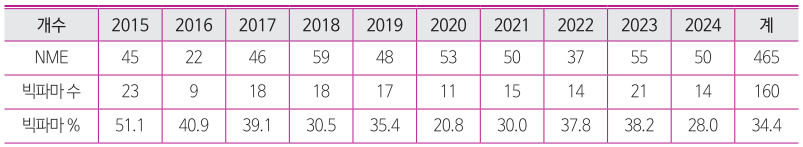
출처 : 자체 조사
◉︎본사 기준으로 제약기업의 국가 비율을 보면, 미국 기업이 54.0%(27개)로 가장 많았고, 유럽 전체 국가의 비중은 36.0%(18개)으로 스위스 10.0%(5개), 영국 6.0%(3개), 프랑스·덴마크·이탈리아가 2개였음
●2024년 FDA 신약 허가 제약바이오 기업 중 미국 기업의 비율은 2022년 64.9%, 2023년 56.4%에 비해서 다소 감소했으며, 27개 기업 중 중소제약기업의 제품이 18개로 66.7%를 차지해 2024년은 중소제약기업들의 FDA 신약 허가 성과가 두드러졌음
< 표 4 > 2015년 이후 미국 FDA 신약 기업 중 미국 기업(본사 기준)의 비율

출처 : 자체 조사
●2024년에는 스위스 제약기업들의 신약개발 성과가 컸는데, ldorsia의 고혈압 치료제 '트리비오(Tryvio)', Basilea Pharmaceutica의 항생제 '제브테라(Zevtera)' 등이 허가 받음
−︎스위스는 2010년 이후 빅파마인 Novaris, Roche 이외에도 Santhera Pharmaceuticasl, Dermavant, ADC Therapeutics 등 다수의 중소제약기업이 미국 FDA 신약 허가를 받았음
●미국과 유럽 이외 국가의 제약기업들의 미국 진출 성과도 있었는데, 중국 기업으로는 Beigene의 PD-1 면역 관문억제제 '테빔브라(Tevimbra)'와 Betta Pharmaceuticals의 자회사인 Xcovery Holdings의 폐암표적치료제인 '엔사코브(Ensacove)'가 허가를 받음
−︎인도 기업으로는 Sun Pharmaceutical Industries의 '렉셀비(Leqselvi)'가 중증 원형 탈모 치료제로 허가받았으며, 한국 기업 중에서 휴젤(Hugel)이 보툴리눔 톡신인 '레티보(Letybo)'로 허가를 받는 데 성공했고 유한양행이 J&J에 기술수출 했던 라즈클루즈(한국명 렉라자)도 승인 받음
−︎2015년 이후 미국 FDA 신약 허가를 받은 465건 중에서 미국 외 국가의 제약기업이 허가를 받은 건은 191건으로, 스위스가 32건으로 가장 많고 일본과 영국이 29건, 아일랜드 17건 순
< 표 5 > 2015년 이후 미국 외 국가의 기업이 FDA 신약 허가를 받은 건수와 비중

출처 : 자체 조사
◉︎(타깃 질환) 2024년 FDA 승인 신약들의 타깃 질환을 보면, 항암(Oncology)가 15건(30.0%)로 가장 높았고, 심혈관(Cardiovascular) 질환이 6건, 순환계(Blood)과 중추신경계(CNS) 질환이 각 5건 순
●2013년 이후 FDA 신약 중 항암제는 133건으로 매년 평균 28.6건이 승인을 받았는데, 2020년 이후 약 30%의 비율을 유지하고 있음
< 표 6 > 2015년 이후 미국 FDA 신약 기업 중 항암제 건수와 비율

출처 : 자체 조사

[ 그림 1 ] 2024년 미국 FDA 신약의 타깃 질환별 비율
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
지식
동향

