기술동향
세포 노화의 분자메카니즘
- 등록일1998-09-01
- 조회수19089
- 분류기술동향
-
자료발간일
1998-09-01
-
출처
다음 카페
- 원문링크
-
키워드
#노화#세포노화#노화 메카니즘
출처: biozine
세포 노화의 분자메카니즘
신득용 / 생명공학연구소 단백질기능R.U. 선임연구원
서 론
약 30 년전 Hayflick과 Moorhead는 in vitro 세포 배양계에서 정상 fibroblast의 성장이 항상 일정한 회수의 세포분열 후에 정지한다는 연구결과를 보고하였다. 그후 이러한 세포의 유 한 증식능은 다른 종류의 세포 배양계에서도 계속 보고되었다. 세포는 증식할 수 있는 제한된 능력을 가지고 있다. 세포는 정해진 회수의 세포분열 후 노화(senescence)라고 불리우는 비가역적인 증식 정지기 (irreversible growth arrest 혹은 terminally non-dividing state) 에 들어간다. 이러한 세포의 노화는 결국 생명체의 노화 진행에 영향을 미친다.
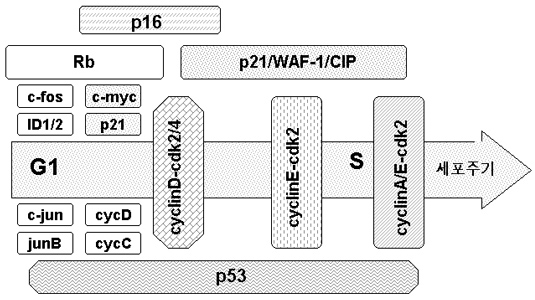
세포의 노화는 세포사멸 (apoptosis, 혹은 programmed cell death)과는 다르다. 노화세포는 장기간 동안 죽지 않고 살아 있으며 세포의 노화가 진행되면서 세포주기의 시간이 길어지는 데, 이는 G1기가 길어지기 때문이며 완전히 노화한 세포는 G1기에서 정지한다. G1기에서 정지한 노화세포는 증식 정지기(Go기)의 세포와는 달리 growth factor 등으로 증식을 자극해도 세포주기를 시작하지 않는다. 세포융합을 이용한 세포학적 실험 결과 노화세포 는 세포증식을 억제하는 증식억제 인자를 적극적으로 발현하고 있다. 1993년 노화세포가 발현하는 증식 억제인자의 하나가 발표되었다. 이 인자 는 세포주기 G1 cyclin-cdk complex (cyclin D/E-cdk2/4)와 결합하여 불활성화하는 단백질로서 이를 발견한 학자들에 의해서 p21, WAF-1, CIP 등으로 명명되었다. 따라서 세포의 노화는 세포주기 조절기능과 밀접한 관련이 있을 것이다. 또한 암 발생 메카니즘과도 관련이 있다.
1. 세포노화의 유전적 프로그램: 노화유전자의 존재
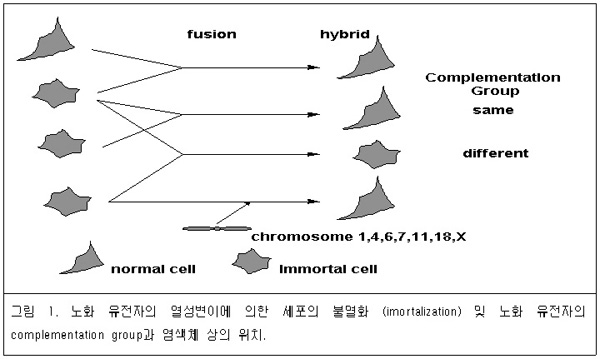
세포 노화 프로그램으로부터 벗어난 암세포를 정상 세포와 융합시켜서 만든 hybrid 세포는 정상세포와 같이 수차례 세포분열 후 노화가 일어난다 (그림 1). 이것은 세포노화가 우성 형질 (dominant phenotype)이라는 것을 시사한다. 즉 암세포의 불멸화는 세포 노화에 관여하는 유전자의 recessive mutation의 결과인 것이 다. 만약 다수의 유전자가 세포노화의 유도에 관여한다면, 불멸화 세포(혹은 암세포)간의 fusion에 의한 hybrid세포에서 세포노 화 혹은 불멸화가 관찰될 것이다. hybrid 세포가 노화를 일으킨다면 그 모세포 (불멸화 세포)는 서로 다른 유전자 결손을 가지고 있을 것 이다. 그러나 만약 hybrid세포가 여전히 노화를 일으키지 않으면 두종류의 모세포는 동일한 유전자의 변이를 가진다고 추정할 수 있다. 즉 동일한 상보 그룹 (complementation group)임을 알 수 있다. 이러한 유전학적인 해석이 약 40종류의 불멸화 세포간에서 이루어졌고 그 결 과 최소한 4종류의 complementation group의 유전자가 노화를 조절하고 있음을 알게 되었다.
Microcell-mediated chromosome transfer기법의 발전에 의하여 하나의 정상 염색체를 불멸화된 세포에 도입하고 세포증식의 변화를 관찰할 수 있게 되었다. 불멸화된 세포에 1, 4, 6, 7, 11, 18번 및 X 염색체를 도입하면 세포의 노화가 유도되는 것이 관찰되었다. 1번 염색체는 group C, 4번 염색체는 group B, 7번 염색체는 group D에 속하는 불멸화세포의 노화를 유도한다. 그러나 6, 11, 18 및 X 염색체는 하나의 complementation group으로 분류되지 않은 불멸화세포의 노화를 유도한다. 그러므로 4 종류 이상의 complementation group이 존재 할 것으로 추정된다.
2. 수명 유전자 (longevity-associated gene)의 존재와 기능
사람을 비롯한 동물의 수명은 어떻게 결정되는 것일까? 과연 분자생물학 연구는 사람 의 수명을 늘릴 수 있는 혹은 노화를 지연시킬 수 있는 방법을 찾아낼수 있을까? 이에 대한 부분적인 대답을 최근의 Science (275, 980-983, 1997)에 실린 Hekimi박사 연구팀의 논문에서 찾을 수 있다.
동물의 수명 혹은 노화의 속도를 결정하는 인자에 대하여 두가지의 가설이 서로 대립 하기도 하고 상호보완되기도 하면서 발전해 왔다. 첫번째의 가설은 대사의 속도가 수명을 결정할 것이라는 생각이다. 각 동물은 일 정한 대사능력을 가지고 있고 대사속도가 빠를수록 노화가 빨리 일어나며 수명도 짧아진다는 것이다. 두번째 가설은 수명은 유전학적으로 결정 이 된다는 것이다. 이러한 관점에서 본다면 노화 혹은 수명을 측정하는 시계는 각 동물에게 각기 다른 속도로 맞추어진 유전적 프로그램일 것이 다.
Hekimi 박사 연구팀이 발표한 caenorhabditis elegans의 clk1 유전자 클로닝 및 구조분석 결과는 전술의 두가지 가설 모두를 동시에 지지하고 있다. mutant clk1 유전자를 가지고 있 는 연충은 wild type clk1 유전자를 가지는 연충에 비하여 약 50% 정도 수명이 길다. mutant clk1을 가지는 연충은 발생초기 의 cell cycle과 embryonic development의 속도가 늦고, 성체가 되어서도 swimming, pumping, defecation 등의 리듬 행동에 장애를 나타낸다. clk1 변이의 효과는 maternal effect를 보여주는데 이는 clk1 유전자가 egg 혹은 발생 초기에 작용하는 것을 시사해 준다. clk1 mutant 연충이 세포의 성장 및 발생 속도가 느린 것은 clk1 mutation 이 세포의 대사능력에 변화를 유발하기 때문일 것으로 추측해 왔다.
clk1 유전자의 클로닝 및 염기배열의 분석은 유전자의 기능에 관한 추측을 가능하게 한다. clk1 유전자는 효모와 rat의 CAT5 유전자와 상동성이 있다. rat으로부터 클로닝한 CAT5 유전자와 마찬가지로 clk1 유 전자가 효모의 cat5 mutation을 complementaion하는 것은 이들 유전자가 구조와 기능이 잘 보존되어 있음을 시사해 준다. 효모의 CAT5 gene은 glycerol, ethanol 등의 비발효성 carbon sources의 대사에 필요한 유전자의 전사조절에 관여한 다고 알려져 있다. cat5 변이주는 glycerol 혹은 ethanol 등의 배지에서 증식할 수 없으며 gluconeogenesis, respiration, glyoxylate cycle 등에 필요한 enzyme의 발현이 일어나지 않는다. 효모 CAT5 유전자의 구체적인 조절기 작은 아직 불분명하지만 세포의 다양한 metabolism pathway의 co-regulation mechanism에 관여할 것으로 추측된다. 연충의 clk1 mutation도 서로 다른 metabolic pathway에 관여하는 것으로 미루어 볼때 효모의 CAT5와 같이 metabolic coordination을 위한 조절기작에 관여할 것이다.
clk1 유전자가 효모의 metabolic regulator와 구조 및 기능에 있어서 유사하다는 발 견은 clk1 mutation에 의하여 대사속도가 slow down되고 노화의 속도가 지연 됨으로써 mutant 연충의 수명 이 연장된다고 추측할 수 있다. 앞으로 연충과 효모에 있어서 이들 유전자의 기능이 밝혀지면 대사속도의 조절 및 대 사의 by-product 생성이 어떻게 노화의 속도와 수명기간을 조절하는 지 알 수 있을 것이다. Superoxide dismutase 유전자를 발현하는 transgenic fly가 수명이 연장된다는 사실이 최근 알려져 있는데, 이 사실은 대사의 부산물 (toxic by-product)에 의해서 세포내 damage가 축적됨으로써 노화가 촉진되고 수명이 짧아지는 것을 시사한다.
그러나 대사 속도 및 세포내 damage의 축적이 노화의 전 과정을 조절할 것 같지는 않 다. 쥐와 박쥐는 비슷한 대사속도를 가지고 있지만 수명은 5배에서 10배정도 다르다. 이는 노화를 조절하는 genetic response 역할을 시사한다. 또한 werner’s syndrome(조로증)을 유발하는 유전자가 DNA helicase인 것으로 최근 밝혀져 있는데 (science, 272, 258), 이러한 사실들로 미루어 볼때 metabolism-generated DNA damage에 대한 genetic response 가 노화의 속도를 결정할 것이다. 그렇다면 response의 실체는 무엇일까?
3. 세포노화와 유전자 발현
노화세포에서 세포주기 조절 유전자들의 발현을 보고하는 많은 논문들이 발표되고 있 다. 증식 정지기에 있는 세포(Go)와 노화 세포를 증식 자극인자로 처리 한 후 세포주기 유전자들의 발현을 비교하면 노화세포 의 특징적인 유전자 발현을 조사할 수 있다. 두 종류의 세포에서 증식 자극 후 공통적으로 H-ras, c-jun, jun B 등의 발현이 나타났으나 노화세포에서는 c-jun의 발현이 유도되지 않았다. 그러므로 c-jun의 발현을 억제하는 인자가 노화세포에서 발현되고 있다고 볼 수 있다. 최근에는 differential screening법을 이용하여 어린세포와 노화세포의 유전자 발현을 정량적으로 분석할 수 있게 되었다. 이 방법에 의해서 AP1 (activator protein 1), CREBP (cAMP response element binding protein), ID1, 및 ID2 (inhibitor of DNA binding)의 전사활성이 노화의 진행에 따라 감소하는 것이 밝혀졌다. 그러나 이들 전사인자의 활성 감소가 세포노화의 원인인지 노화의 결과인지는 아직 명확하지 않다.
|
그림 2. 노화세포의 특징적인 세포주기 관련 유전자의 발현. 노화섬유아세포를 증식 자극후 유 전자 발현의 변화를 나타낸다. |
4. 세포노화와 Telomere
염색체 말단의 불완전한 DNA복제가 세포증식 능력의 감소를 초래하고 세포노화를 유 발한다는 가설이 1973년 Olovnikov 등에 의하여 발표된 이래 염색체 말단구조와 세포노화의 관련성에 관한 많은 연구가 수행되 어 왔다. 염색체 말단, 즉 telomere는 repeated sequence로 구성되어 있으며 염색체의 분해 및 다른 염색체와의 결합으로부터 자 신의 염색체를 보호하는 기능을 가지고 있다. 염색체 말단구조의 상실이 세포노화와 관련이 있다는 최초의 실험적 증거는 1990 년 Harley 등에 의하여 발표되었다. Harley 등은 인체배양 fibroblast의 terminal restriction fragement(TRF)의 길이가 세포분열의 회수에 따라 감소하는 것을 발견하였다. 또한 노인으로부터 분리한 fibroblast와 혈액세포의 TRF의 길 이가 어린이의 세포의 TRF보다 짧다. 그러나 in vitro에서 불멸화된 세포와 암세포는 세포분열을 계속해도 Telomere의 길이가 감소되 지 않았다. 이러한 결과는 인체의 정상세포가 세포분열 즉 DNA 복제를 계속할수록 telomere의 길이가 감소하며, 결국 세포가 telomere의 단축된 길이를 감지하고 세포분열을 중지시켜서 세포노화를 초래할 것을 시사한다. 불멸화된 세포는 염색체 말단, telomere의 길이를 안정적으로 유지하기 위하여 telomerase의 높은 활성이 필수적인 것일 것이다. 이러한 telomere 가설은 정상세포의 세포분열 과 노화를 연결하는 중요한 분자기작을 제시한다.
그러나 활발한 후속연구의 결과들은 기존의 모델을 더욱 복잡하게 만들어 가고 있 다. telomrease의 결손을 가지는 불멸화된 세포주가 발견되었고, 불멸화된 B, T세포를 telomerasae의 활성 저해를 유도해 도 세포의 불멸화 상태에 아무런 영향을 주지 않았다. 또한 정상세포에서도 telomerase의 발현이 발견되었고, 이들 세포는 세포 분열에 따라 telomere의 길이가 감소했다. 체세포 융합에 의한 hybrid에서 노화와 telomerase의 활성은 서로 관련이 없었다.
최근 holiday 등은 telomere 가설을 조정할 수 있는 실험결과들을 발표하였다. 세포 분열에 의하여 탄생한 두 개의 daughter 세포가 서로 다른 수준의 증식능력을 가질수있으며 실험적인 조작에 의하여 인체 fibroblast의 life span을 향상시킬 수 있다는 것이다. 그럼에도 불구하고 telomere가설은 현재 가장 유력한 모델로서 mitotic clock의 분자적 이해의 기초를 제공한다.
5. 세포노화와 암 억제 유전자
암 관련 유전자가 세포의 노화에 어떤 영향을 미치는 것일까? 암과 노화란 전혀 관련 성이 없어 보이지만 사실은 동전의 앞·뒷면과 같은 관계에 있다. 암 세포가 무한증식 하기 위해서는 세포의 유한증식을 지 배하는 세포 노화 프로그램을 무시해야만 한다. 암 발생과정에서 정상세포의 불멸화 (immortalization)과정이 바로 이런 노화 프로그램으로부터 벋어나기 위한 과정이다. 세포의 불멸화 과정에는 다양한 암 관련 유전자가 작용하는 것이 밝혀져 있다. 따라서 oncogene의 일부 는 노화 프로그램을 해체하는 작용을 할 것으로 보인다.
p53 및 RB 등의 항암유전자는 많은 암세포에서 변이 등에 의하여 그 기능이 상실되 어 있고, 암세포에서 과발현시키면 세포의 증식 정지 혹은 세포사멸 (apoptosis)을 일으킨다. 암세포는 세포의 정상적인 노 화기작의 지배를 받지않고 무한증식이 가능하다. 세포노화는 SV40 T항원 등의 DNA tumor virus의 유전자의 발현이나 p53, Rb 등의 항암유전자 의 antisense DNA, 혹은 인체암세포에서 고빈도로 발견되는 dominant-negative p53 mutant에 의하여 지연될 수 있 다.
최근 필자의 연구실은 p53 항암 유전자가 암세포의 노화를 유도한다는 새로운 사실 을 발견하였다. p53 유전자의 선택적인 발현 시스템을 구축하고 암세포에서 p53 유전자를 과발현 시킨 결과 세포주기의 정 지에 이어서 노화가 시작되는 것을 비가역적인 세포증식의 정지, cdc2, cyclin A, B의 발현감소, p21/Waf1의 발현유도, Rb의 탈인산화, β-galactosidase marker의 출현 등에 의하여 확인하였다. 이 결과는 p53 유전자가 암세포에서 작동하지 않고 있는 노화 프로그램을 자극하여 활성화 하여 이미 수명을 초과한 암세포를 노화시키는 것으로 보인다.
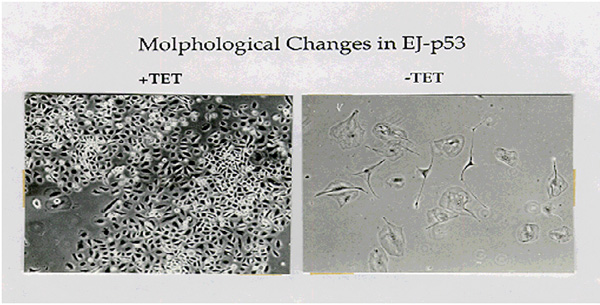
그림 3. p53 유전자의 선택적 발현에 의한 암세포의 노화. (+)tetracyclin 조 건하에서는 p53 유전자를 발현하지 않고 정상적으로 성장하지만 (-)tetracyclin 조건하에서 p53 유전자가 발 현되고 세포주기 정지와 함께 노화가 시작된다(Shin et al., Proc. Nat'l. Acad. Sci. USA, 94, 9684).
6. 세포노화와 세포주기
세포의 노화는 세포주기 G1기에서 정지한 후 아직 알려지지 않는 다른 종류의 신호전 달계와 협력하여 비가역적인 증식 정지와 동시에 노화기로 들어갈 것으로 보인다. 대부분의 노화 세포에서는 G1 cyclin-cdk complex 의 활성이 억제되어 있고 증식 자극후에도 정지기의 세포와는 달리 이들 complex가 활성화 되지 않는다. 따라서 G1 cyclin- cdk complex의 활성을 억제하는 시스템이 노화에 중요한 역할을 수행할 것으로 추측해 볼 수 있다. p21의 발현은 세포 분열이 한계수명에 가까워 질수록 증가하여 완전히 노화한 세포에서는 어린 세포보다 약 10-20배 정도 많이 발현된다. p21의 발현은 p53 에 의하여 제어되기 때문에 p53의 dominant negative 변이를 도입했을 경우 세포분열의 한계수명이 연장된다는 결과는 p53의 기능 상실에 의한 p21 발현의 감소때문일 것이다. 최근 p21 유전자를 knock out시킨 세포에서 세포수명의 연장이 보고되었 다. 따라서 p21의 발현이 노화의 진행에 중요한 인자임에는 틀림없다. 그러나 p21의 발현증가가 이미 알려진 것처럼 cyclin E/D- cdk2/4의 활성감소와 Rb의 탈인산화로 이어지는 일련의 cascade에 의한 것인지 혹은 다른 경로의 미지의 인자들이 관여하는 것인지는 명확하지 않다. 그러나 최근 Rb의 발현이 세포노화를 유도할 수 있다는 보고가 계속 발표되고 있기 때문에 적어도 Rb를 매개 로 하는 경로가 노화의 진행에 관여하는 것은 사실인 것 같다. p21과 같이 cyclinD-cdk4 복합체의 활성을 저해하는 p16의 역할도 주목된다. p16 의 발현도 노화의 진행에 비례해서 증가힌다.
세포노화 연구의 전망
인체는 분열세포와 비분열세포로 구성되어 있고 이들의 성질과 변화에 따라 인체의 노화가 진행될 것이다. 뇌세포와 신장세포 등의 비분열세포의 상실 혹은 기능저하는 생명을 위협하는 주요 요인이다. 따라서 비분열조직으로 구성되어 있는 선충(c. eleganse)과 초파리의 수명연장 변이체의 분자 유전학적 분석은 노화 연구의 중요한 전환점을 제공해 줄 수 있을 것이다. 한편 조직의 기능저하는 그들을 구성하는 분열세포의 기능저하와 관련이 있다. 최근 유전적 조로를 유발하는 werner′s syndrome의 유전자가 발견되어 DNA helicase인 것으로 밝혀졌다. 세포주기를 제어하는 시스템과 노화와의 관련성에 중요한 단서를 제공하고 있다.
세포의 불멸화 과정에 관여하는 적어도 4종류의 M2기 유전자의 실체가 밝혀지면 세포 노화를 이해하는데 중요한 계기가 될 것으로 기대된다. 노화에 다른 신체기능의 저하와 노화 관련 질환의 대부분은 세포의 비정상 적인 노화의 결과로서 나타나는 퇴행성 기능변환이 원인일 것으로 생각된다. 따라서 노화 프로그램의 분자적 실체가 규명되면서 이러한 신체기 능의 장애와 질환을 예방할 수 있는 지식이 생겨날 것을 기대해 본다.
|
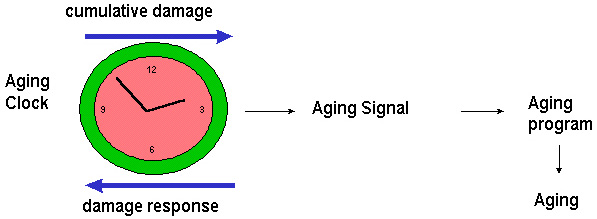
그림 4. 노화의 가설. 인체 내에 존재하는 노화시계(Aging clock)는 damage의 축적과 damage를 해소하는 damage response의 평형에 의하여 조절되고 이 신호는 세포증식을 조 절하는 시스템에 전달될 것이다. |
|
신득용 / 생명공학연구소 단백질기능 R.U. 선임연구원 ■ 주소:(305-333) 대전광역시 유성구 어은동 52 |
지식
- BioINwatch 노화 시계(aging clock)를 늦추는 당뇨병 치료제 2024-10-10
- BioINwatch 특정 줄기세포에 대한 항체로 노화된 면역체계의 회춘 가능성 제시 2024-05-09
- BioINpro [면역제어 기술]대사·후성유전학 기반 면역노화(immunosenescense)의 이해 2023-11-21
- BioINwatch 생식 노화를 복구하는 천연 폴리아민, 스페르미딘(spermidine) 2023-11-09
- BioINwatch 젊은 혈액(young blood)에서 뇌 노화를 되돌리는 혈소판 인자 4(Platelet factor4) 발굴 2023-09-19
동향