기술동향
A small molecule kinase inhibitor for CNS diseases: Dr. Larry Park
- 등록일2005-05-13
- 조회수8132
- 분류기술동향
-
자료발간일
2005-05-13
-
출처
IBRIC
- 원문링크
-
키워드
#CNS diseases
출처 : IBRIC
A small molecule kinase inhibitor for CNS diseases: Dr. Larry Park
(Senior Research Scientist/Group Leader), Vertex Pharmaceuticals
개요
우리에게 새로운 생명을 부여하는 존재로 크게 인식되기도 하며 한편으로는 필요시 항상 손쉽게 구입할 수 있는 존재로 인식되는 약. 이러한 약들이 세상에 탄생하기까지 그 일면에는 많은 사람들의 부단한 노력과 끊임없는 창조성이 요구되며 또한 긴시간과 많은 경비가 소요된다. 신약개발은 현재 21세기의 국가 경쟁력을 좌우할 만한 첨단기술로 각광받고 있는 생명공학(Biotechnology)분야의 핵심이라고 할만큼 많은 제약기업들이 과감한 연구개발투자를 통해 신약개발에 힘쓰고 있으며 이러한 낮은 성공확률에도 도전하며 장기간 연구개발에 투자할 수 있는 힘은 바로 인간 생명의 존엄성에 가치를 둔 과학자들의 인체에 보다 안전하며 효과적인 약품을 개발할 수 있다는 믿음에서 나오는 것이라 본다.
이와 관련지어, 현재 약품연구개발에 널리 응용되고 있는 신기술인 화학유전체학(chemogenomics)분야를 선두적인 입장에서 개척해 온 보스톤 소재 제약회사 Vertex Pharmaceuticals에서 뛰어난 리더십을 발휘하며 중추신경계질환 관련 약품개발에 훌륭한 성과를 거두고 있는 Dr. Larry Park과의 인터뷰를 통해 그의 academia로부터 제약업계로의 진출동기, 현재 연구의 주요 관심사 및 활동 그리고 장래희망 및 포부에 대해 알아보았다.
Q. Pharmaceutical에서 신경과학(neuroscience)과 관련된 연구를 하게 된 동기는
저는 커가면서 약의 효능에 대한 관심과 함께 인간생명에 실질적으로 도움을 줄 수 있는 일을 하고 싶다는 생각을 갖게 되었습니다. 그리고, 이러한 생각들은 학부과정에서 분자생물학 및 생리학의 bridge역할을 함으로써 양분야를 포괄적으로 공부할 수 있는 제약학 pharmacology and toxicology)을 선택하는 동기가 되었으며 그 이후, academia로부터 자신의 창의성과 능력을 발휘하여 혁신적인 신약개발에 도전할 기회를 부여하는 mid-sized pharmaceutical 세계로 뛰어들면서 보다 구체화, 현실화될 수 있었습니다.
제가 특히 뇌(brain)와 척추(spinal cord)영역을 일컫는 (중추신경계(CNS, central nervous system 클릭!)분야에 관심을 갖게 된 계기는 대학원 및 연구원(postdoc)과정에서 다양한 퇴행성신경질환을 유발시킬 가능성이 있는 nitric oxide (NO)의 과생성 및 oxidative stress와 연관된 미토콘드리아의 기능적 장애(mitochondrial dysfunction)에 대한 연구를 통해서였습니다. 코넬대학에서 연구원과정을 마친 2000년도에 scientist로서 제약회사에 첫발을 내딛어 뇌졸중(stroke)과 관련된 연구를 시작하였으며 2001년부터 지금까지 Vertex Pharmaceuticals에서 senior scientist 및 group leader로서 치매, 뇌졸중, 정신질환과 같은 CNS 질환을 비롯하여 면역계 질환, 심혈관질환등 다양한 질병들의 치료요법 대상인 kinase inhibitor을 중점적으로 연구함으로써 그와 관련된 연구결과를 토대로 한 신약개발에 중점을 두고 있습니다.
Q. 연구주요관심사 및 현재그룹활동은
Human genome의 약 2%을 차지하며 ATP-dependent enzyme로 알려진 (kinase 클릭!)는 지금까지 500개 이상 발견되었으며 CNS질환, 암, 면역성 질환등과 관련된 kinase을 대상으로 하여 치료목적의 kinase inhibitor을 연구개발하는 것이 저를 비롯한 많은 회사들의 주요관심사입니다. 현재까지 시판되고 있는 것으로는 Novartis 가 암치료제로 개발한 BRC-ABL inhbitor 인Gleevec 을 시작으로 AstraZeneca 의 Iressa 그리고 OSI Pharmaceuticals 의 Tarceva등이 있습니다. 저의 현재 연구목표는 chemogenomics와 crystallography을 이용하여 관심의 대상인 enzyme과 compound의 구조를 이해 및 조절하는 차원의 연구 즉, kinase의 active site로 알려진 ATP-binding pocket을 target으로 하여 chemical compound를 그 pocket에 binding시킨후, 이러한 molecule-compound complex안에서의 modification을 통해 가장 potent하고 ive한 compound를 발견하는 것입니다 (Fig 1).
Fig 1. ATP in Catalytic Site Of Protein Kinase (electrostatic surface, left)
and Protein Kinase Inhibitor (red surface, right) -클릭!
저의 주요관심분야이자 연구대상인 GSK3 (Fig 2, glycogen synthase kinase-3)은 1970년대 처음으로 그 존재가 밝혀진 kinase로서 일반적으로 다른 kinase와는 달리 active form으로 존재하며 인산화(phosphorylation)에 따라 그 활성이 억제되는데 현재까지 cell survival, glucose metabolism등 다양한 생리적인 현상들과 관련된 multiple pathways을 merge하는 kinase로써 알려져 있어 pharmaceutical interest가 되고 있습니다. 현재 저는 CNS질병치료에 가장 효과적인 GSK3 inhibitor을 찾아내는 일에 집중하고 있으며 이와 관련된 연구성과로는 GSK3의 isoform(alpha/beta)중에 하나로서 뇌에서 많이 발현되는 beta-form이 뇌졸중의 유발(onset) 및 진전(progression)과 깊게 연관되어 있다는 연구결과를 토대로 2003년도에 개발된 GSK3 beta kinase인 VX-608이 있습니다. 그리고 이러한 VX-608는 전임상단계 (preclinical trial, 동물모델을 이용한 in vivo실험단계)을 통해 뇌졸중으로 인해 발생하는 조직손상을 줄이고 그 증상을 호전시킨다는 실험결과를 얻음으로써 그 효능이 입증되었습니다.
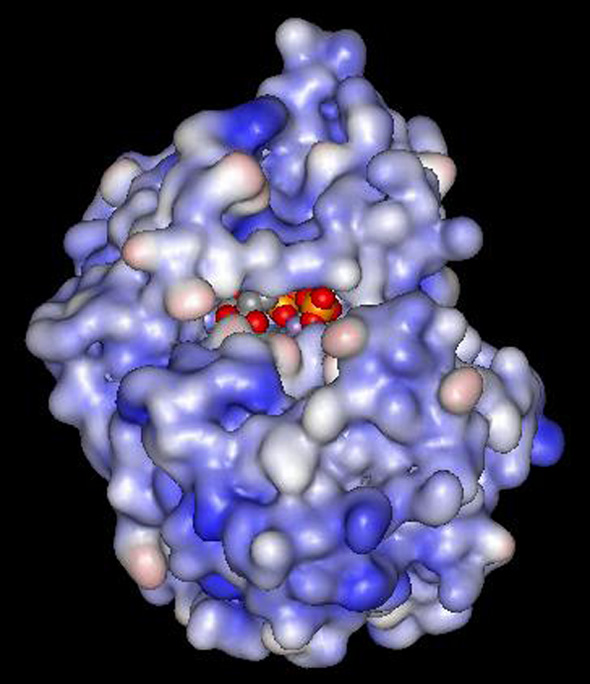
Fig2. GSK3-beta structure (Ter Haar et al., Nature Structural Biology, Volume 8)
다른 CNS질환의 therapeutic target으로서 GSK3은 정신질환인 조울증(bipolar affective disorder) 및 정신분열증(schizophrenia)의 치료약으로 널리 사용되고 있는 lithium의 주요 target중에 하나로서 알려져 있으며 또한, 최근 발표된 치매증상의 뇌에서 활성형태인 GSK3가 증가한다는 연구결과는 치매증상의 주요특징인 Tau의 비정상적인 인산화, beta-amyloid 생성등의 연관성을 높혀주고 있습니다. 또한, Parkinson's disease에 중요한 dopaminergic pathway에 GSK3가 관련된다는 보고자료가 있으며 또한 beta-catenin의 인산화와 연관지어 대장암 및 췌장암의 유발 가능성도 보고되고 있습니다 (fig 3). 그러므로 저희그룹은 CNS 질환을 중점으로 이러한 다양한 질병에 직접적, 간접적으로 관련된 GSK3의 역할을 철저히 분석함으로써 치료목적의 가장 적합하며 효과적인 kinase inhibitors을 개발하는데 주력하고 있습니다.
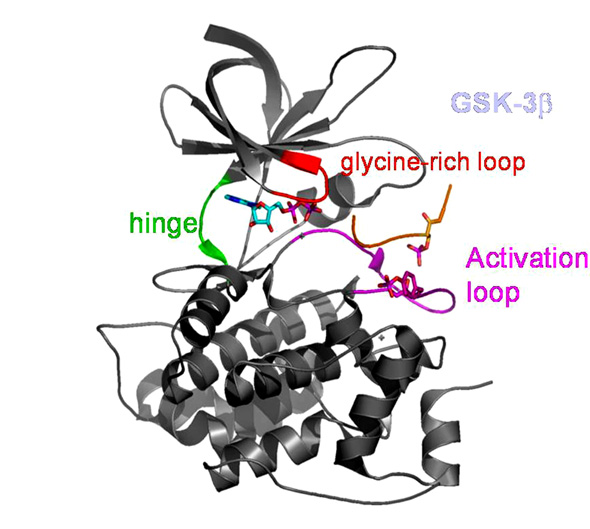
Fig 3. GSK3-beta at the crossroads of signaling pathways
(Eldar-Finkleman, H. Trends in Mol Med, 8:126, 2002)
Q. 미래과제 및 과학자들과 공유하고 부분은
인간을 대상으로 하는 임상실험단계(clinical trial)로 갈 수 있는 약이 되기 위해서는 약의 작용을 다루는 약역학 (PD, pharmacodynamics), 시간경과에 따른 약효과의 지속성을 관찰하는 약동학(PK, pharmacokinetics) 그리고 독성검사인 toxicology등의 test를 통해 요구되는 필수조건을 구비해야 하며 또한, tablet 또는 liquid등으로 형태로 조재(formulation)될 수 있는지의 여부도 결정적인 주요요건중에 하나입니다. 예를 들어 ATP-binding pocket을 target한 kinase inhibitor들은 대체로 약 MW 400 의 작은 분자들로서 hydrophilic하지 않아 그 용해성(solubility)이 저하됨으로써 약형태로 formulation되는 어렵다는 단점을 가지고 있고 이와같이 많은 risk와 trials를 거쳐서야 인체를 위한 하나의 약품이 탄생된다고 볼 수 있을 만큼 약품개발은 힘든 것이라 생각합니다. 그래서 현재 시판되고 있는 제품들, 특히 asprin이나 Tylenol과 같은 약품들을 개발한 분들을 노력과 수고를 좀더 이해하게 되었고 그런분들과 같이 항상 생명에 도움을 주고 인류에 도움이 되는 일을 하고 싶습니다. 또한, 미래에 한방에서 많이 쓰이는 약초등을 이용하여 예방차원의 치료약개발에 관심에 있으며 차후에 쌓은 경험을 토대로 약품개발 및 기술차원에서의 consulting도 하고 싶습니다.
최근 들어 Biotech/Pharmaceuticals와 academia간에도 공동연구를 통해 좋은 경험을 쌓고 있으며 제약업계로의 진출에 관심이 있으신 과학자 여러분들에게 드리고 싶은 말은 제 경험으로 볼 때 제약업계는 academia에 비해 연구차원에서 보다 높은 융통성(flexibility)와 적응력(adaptability)이 필요하다고 봅니다. 그리고 효과적이며 효율적인 communication skill 또한 회사 진출 및 회사생활에 도움이 될 것이라 봅니다.
참고자료
ㅇThe human central nervous system
ㅇChemogenomics : an emerging strategy for rapid target and drug discovery (Naure Review Genetics, 2004)
ㅇGSK3 inhibitors: development and therapeutic potential (Nature reviews, 2004)
ㅇGlycogen synthase kinase 3: a drug target for CNS therapies (Journal of Biochemistry, 2004)
ㅇGSK-3alpha regulates production of Alzheimer's disease amyloid-beta peptides (Nature, 2003)
< Dr. Larry CH Park, Ph.D. 약력소개>

Dr. Larry Park은 UCLA (University of California at Los Angeles)에서 학부 (생물학전공)를 마친후 UC at IRVINE에서 중추신경계와 관련된 nitric oxide (NO)와 CNS mitochondiral benzodiazepine receptors에 대한 연구로 제약학분야에서 박사학위를 받았다, 그 이후 연구원으로 Cornell University Medical School에서 oxidative stress, mitochondrial dysfunction & neurodegenerative diseases 관련연구를 하였으며, California소재 Galileo Pharmaceuticals에서 scientist로서 제약업계에 첫발을 내딛은 후 현재 보스톤 소재 Vertex Pharmaceuticals에서 senior research scientist 및 group leader로서 재직 중이다. 현재 CNS질환과 면역계 질환 치료목적의 kinase inhibitors 약품을 연구개발하고 있다.
ㅇHomepage : Vertex pharmaceuticals Inc
ㅇe-mail: Larry_Park@vrtx.com
ㅇ Phone: 617-444-6492 (w), 617-444-6713 (fax)
Publications
Papers
1. Park LCH, Chen C, Zhang H, Oh L, Loo A, Crumrine C, Furey B, Ma J, Yao YM. A ive GSK3 inhibitor VX-608 provides significant protection in models of ischemic stroke. In preparation.
2. Shao Z, Bhattacharya K, Bhattacharya S, Hsich E, Park LCH, Walters B, Germann U, Wang YM, Mohanlal R, Kuida K, Namchuk MN, Salituro F, Yao YM, Hou YM, Chen X, Aronowitz M, Tsichlis P, Force T, Kilter H. c-Jun N-terminal kinases mediate reactivation of Akt and cardiomyocyte survival after hypoxic injury in vitro and in vivo. Submitted.
3. Gibson GE, Zhang H, Xu H, Park LC, Jeitner TM (2002) Oxidative stress increases internal calcium stores and reduces a key mitochondrial enzyme. Biochim Biophys Acta, 1586:177-189.
4. Park LCH, Zhang, H., Albers DS, Augood SJ, Browne SE, Martin DM, Adamson D, Hutton JM, Standaert DG, Vonsattel JPG, Beal MF, and Gibson GE. (2001) The role of mitochondrial enzyme and oxidative stress in the cerebellum of PSP. J. Neurosci Res., 66:1028-1034.
5. Park LCH, Zhang, H, and Gibson GE. (2001) Co-culture with astrocytes or microglia protects metabolically impaired neurons. Mech. Ageing Dev. 123:21-27.
6. Andreassen OA, Ferrante RJ, Huang HM, Dedeoglu A, Park L, Ferrante KL, Kwon J, Borchelt DR, Ross CA, Gibson GE, and Beal MF (2001) Dichloroacetate exerts therapeutic effects in transgenic mouse models of Huntington's disease. Ann Neurol, 50:112-117.
7. Gibson GE, Haroutunian V, Zhang H, Park LCH, Mohs R, Sheu K-FR, and Blass JP. (2000) Reductions in brain a-ketoglutarate dehydrogenase activity in Alzheimers Disease correlate with dementia severity. Ann Neurol., 48: 297-303.
8. Park LCH, Calingasan NY, Uchida K, Zhang H, and Gibson GE. (2000) Metabolic impairment elicits brain cell-type ive s in oxidative stress and cell death. J. Neurochem., 74: 114-124.
9. Gibson GE, Zhang H, Sheu KR, and Park LC. (2000) Differential alterations in antioxidant capacity in cells from alzheimer patients.Biochim Biophys Acta 1502(3):319-329.
10. Park LCH, Calingasan NY, Sheu K-FR, and Gibson GE. (2000) Quantitative histochemistry of ?-ketoglutarate dehydrogenase activity in the brain and in cultured cells. Anal. Biochem., 277: 86-93.
11. Albers DS, Augood SJ, Park LCH, Browne SE, Martin DM, Adamson J, Hutton JM, Standaert DG, Vonsattel JPG, Gibson GE, and Beal MF. (2000) Frontal lobe dysfunction in Progressive Supranuclear Palsy: Evidence for oxidative stress and mitochondrial impairment. J. Neurochem., 74: 878-881.
12. Park LCH, Zhang H, Sheu K-FR, Calingasan NY, Kristal BS, Lindsay JG, and Gibson GE. (1999) Metabolic impairment induces oxidative stress, compromises inflammatory responses, and inactivates a key mitochondrial enzyme in microglia. J. Neurochem. 72: 1948-1958.
13. Calingasan NY, Chun WJ, Park LCH, Uchida K, and Gibson GE. (1999) Oxidative stress is associated with region-specific neuronal death during thiamine deficiency. J. Neuropathol. Expt. Neurol., 58: 946-958.
14. Cho S, Volpe BT, Bae Y, Hwang O, Choi H J, Gal J, Park LCH, Chu CK, Du J, and Joh TH. (1999) Blockade of tetrahydrobiopterin synthesis protects neurons after transient forebrain ischemia in rat: a novel role for the cofactor. J. Neurosci., 19(3): 878-889.
15. Park LCH, Gibson GE, Bunik V, and Cooper AJL. (1999) Inhibition of mitochondrial enzymes in PC12 cells exposed to S-(1,1,2,2-tetrafluoroethyl)-L-cysteine. Biochem. Pharmacol. 58: 1557-1565.
16. Conti B, Park LCH, Calingasan NY, Kim Y, Kim H, Bae Y, Gibson GE, and Joh TH. (1999) Cultures of astroctes and microglia express interleukin 18. Mol. Brain Res., 67(1): 46-52.
17. Calingasan NY, Park CH, Gandy SE, and Gibson GE. (1998) Disturbances of the blood-brain barrier without abnormal expression of amyloid precursor protein or neuronal loss during late stages of thiamine deficiency in guinea pigs. Develop. Neurosci., 20:454-461.
18. Calingasan NY, Park LCH, Calo LL, Trifiletti RR, and Gibson GE. (1998) Induction of nitric oxide synthase and microglial responses precede ive cell death induced by chronic impairment of oxidative metabolism. Am. J. Pathol., 153:599-610.
19. Xue BG, Whittermore ER, Park CH, Woodward RM, Lan NC, and Gee KW. (1997) Partial agonism by 3a,21-Dihydroxy-5b-pregnan-20-one (5b-THDOC) at the GABAA receptor neurosteroid site. J. Pharm. Exp. Ther., 281:1095-1101.
20. Park CH, Carboni E, Wood PL, and Gee KW (1996) Characterization of peripheral benzodiazepine type sites in a cultured murine BV-2 microglial cell line. Glia, 16:65-70.
21. McCauley LD, Park, CH, Lan, NC, Tomich, JM, Shively, JE, and Gee KW. (1995) Benzodiazepines and peptides stimulate pregnenolone synthesis in brain mitochondria. Eur. J. Pharm., 276:145-153.
Reviews/Chapters
1. Gibson GE, Calingasan NY, Park LCH, and Zhang H. (1999) Oxidative stress and a key metabolic enzyme in Alzheimer brains, cultured cells, and an animal model of chronic oxidative deficits IN Oxidative/energy metabolism in neurodegenerative disorders. Anals New York Acad. Sci., New York, Vol. 893, pp79-94.
2. Gibson GE, Park LCH, Sheu RK-F, Blass JP, and Calingasan NY. (2000) The a-ketoglutarate dehydrogenase complex in neurodegeneration. Neurochem. Intl., 36: 97-112.
3. Park LCH (2001) Metabolic impairment elicits brain cell-type ive s in oxidative stress and cell death. Neurochem News, No. 1, June, 2001, pp116-117.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
-
이전글
- 식물생명과학에 의해 생산된 기능성식품
-
다음글
- 산야초류의 항암성

