기술동향
재조합 항체 단편을 이용한 암 면역치료(Recombinant antibody fragment-based cancer immunotherapy)
- 등록일2018-09-27
- 조회수6596
- 분류기술동향 > 레드바이오 > 의약기술
-
자료발간일
2018-09-18
-
출처
생물학연구정보센터(BRIC)
- 원문링크
-
키워드
#항체 단편#면역치료#암#항체
- 첨부파일
재조합 항체 단편을 이용한 암 면역치료(Recombinant antibody fragment-based cancer immunotherapy)
목차
1. 서론
2. 본론
2.1 재조합 항체 단편
2.1.1 전체 항체 및 항체 단편
2.1.2 절단에 의한 항체 단편화
2.1.3 유전자 클로닝을 통한 재조합 항체 단편 작성
2.2 면역관문억제제
2.3 재조합 항체 단편을 이용한 면역치료
3. 결론
4. 참고문헌
1. 서론
암을 치료하기 위한 대표적인 방법은 수술, 화학치료, 방사선치료라 말할 수 있다. 이러한 3대 암치료의 뒤를 잇는 제4의 암치료법으로 최근 주목받고 있는 것이 면역치료(immuno therapy)이다 [2]. 1990년대까지 알려진 면역치료는 인체 내부 ‘전체’의 면역력을 높여 암과 싸우도록 하는 방법이 사용되었는데, 활성화림프구치료법(LAK요법, CAT요법 및 NK세포치료법), 인터페론(IFN-a, IFN-b, IFN-g) 및 인터로이킨(IL-2) 등을 사용하는 cytokine 치료법을 예로 들 수 있다. 하지만 이러한 방법은 암세포 특이적이 아니라 체내 전체의 면역력을 높이는 비특이적 치료법이었기 때문에 어느정도 진행이 된 암치료에 있어서는 한계를 나타내었다. 1990년에 접어들어 면역세포가 암세포를 공격하는 메커니즘이 밝혀지면서 면역세포를 활성화시켜 정상세포에는 영향을 미치지 않으며 암세포만을 공격하도록 하는 암세포 특이적 치료법 및 면역응답을 제어하는 분자의 활성을 억제하는 방법을 이용하는 치료법이 제안되기 시작되었고, 이들을 통하여 암 면역치료법이 비약적으로 발전되었다.
전자인 면역세포가 암세포를 공격하는 기능을 활성화하는 대표적인 치료법으로 수지상세포 백신치료법을 들 수 있는데, 암세포를 인지하는 신호를 수지상세포가 림파구에 전달하여 암을 공격하는 면역시스템을 이용한 것이다. 이렇게 세포를 사용하여 면역력을 증가시키는 방법 외에 항체를 사용하여 면역력을 증가시키는 방법이 주목을 받고 있는데, 대표적으로 Rituximab는 B 세포 표면에 발현하는 CD20이라는 단백질을 인식하는 항체로 CD20에 결합하여 암세포화된 B 세포의 증식을 억제한다. 이와 비슷한 원리의 항암제로 Trastuzumab(사람 종양유전자인 Her2/neu의 유전자산물인 HER2 단백질에 특이적으로 결합함으로써 항종양효과를 나타내는 항암제) 등이 있다. 후자인 면역억제를 제어하는 방법은 PDL1 및 CTLA4와 같은 면역체크포인트를 저해하는 물질로 항체를 이용하는 것이 요점이 되는데, 대표적으로 항PDL1항체(Nivolumab, Pembrolizumab), 항CTLA4항체(ipilimumab)를 들 수 있다. 이러한 면역체크포인트억제제는 직접 암세포를 공격하는 것이 아니라 암세포를 공격하는 T 세포의 활성을 억제하는 분자의 활동을 저해하는 기능을 하기 때문에 T 세포는 암세포에 대항하는 본래의 공격성을 되찾을 수 있게 되어 항암효과를 나타낸다. 또한 상기한 두가지 치료법을 병용함으로써 치료 효과를 높일 수 있다.
본 리포트에서 다룰 내용은 최근에 그 효용성이 부각되고 있는 면역응답을 억제하는 분자의 활성을 제한하는 항체를 이용한 암면역치료법에 관한 최근의 연구 동향이 되겠다. 특히 항체중에서도 그 크기가 작고 유전자 클로닝을 통해 대량생산이 가능한 재조합 항체 단편(recombinant antibody fragment)을 이용한 방법에 초점을 두어 설명하고자 한다.
2. 본론
2.1 재조합 항체 단편
2.1.1 전체 항체(Full-sized antibody) 및 항체 단편(Antibody fragment)
항체는 Y자 형태로 간략히 표현될 수 있는데, 한개의 H chain (Heavy chain)과 두개의 L chain (Light chain)으로 구성된다. 또한 항체 중에서 항원이 결합하는 부위를 가변 영역(Variable region) 이라 하고 그 외의 부분을 정상 영역(Constant region)이라 하는데, 이들의 초기 알파벳을 조합하여 VH, VL, CH (항원결합부위에서 가까운 쪽에서부터 CH1, CH2, CH3), CL로 명명한다.
항체의 크기는 약 150 kDa인데 이보다 더 작은 크기의 항체가 필요할 경우 Fv (VH+VL), scFv (VH와 VL을 펩타이드 링커로 연결, Fv보다 항원결합력이 강함) 또는 Fab (VH+CH1과 VL+CL을 disulfide bond로 연결)와 같은 항체 단편을 사용할 수 있는데, 이들 항체 단편은 항원결합부위를 갖고 있으면서도 그 크기가 각각 약 25 kDa, 25 kDa, 50 kDa으로 Y자 형태를 띄는 전체 항체보다 작기 때문이다. 뿐만 아니라 Immunohistochemistry 및 Flow cytometry analysis를 사용하는 세포 실험에 항체가 사용될 경우 Fc (H chain 중에서 VH+CH1 이외의 부분, 즉 CH2+CH3으로 이루어진 항체의 밑기둥 부분) 수용체를 포함하는 세포를 사용하게 되면 비특이적 반응이 발생할 수 있기 때문에 이러한 경우에 Fc가 제거된 항체 단편을 사용하는 것이 유리하다.
목차
1. 서론
2. 본론
2.1 재조합 항체 단편
2.1.1 전체 항체 및 항체 단편
2.1.2 절단에 의한 항체 단편화
2.1.3 유전자 클로닝을 통한 재조합 항체 단편 작성
2.2 면역관문억제제
2.3 재조합 항체 단편을 이용한 면역치료
3. 결론
4. 참고문헌
1. 서론
암을 치료하기 위한 대표적인 방법은 수술, 화학치료, 방사선치료라 말할 수 있다. 이러한 3대 암치료의 뒤를 잇는 제4의 암치료법으로 최근 주목받고 있는 것이 면역치료(immuno therapy)이다 [2]. 1990년대까지 알려진 면역치료는 인체 내부 ‘전체’의 면역력을 높여 암과 싸우도록 하는 방법이 사용되었는데, 활성화림프구치료법(LAK요법, CAT요법 및 NK세포치료법), 인터페론(IFN-a, IFN-b, IFN-g) 및 인터로이킨(IL-2) 등을 사용하는 cytokine 치료법을 예로 들 수 있다. 하지만 이러한 방법은 암세포 특이적이 아니라 체내 전체의 면역력을 높이는 비특이적 치료법이었기 때문에 어느정도 진행이 된 암치료에 있어서는 한계를 나타내었다. 1990년에 접어들어 면역세포가 암세포를 공격하는 메커니즘이 밝혀지면서 면역세포를 활성화시켜 정상세포에는 영향을 미치지 않으며 암세포만을 공격하도록 하는 암세포 특이적 치료법 및 면역응답을 제어하는 분자의 활성을 억제하는 방법을 이용하는 치료법이 제안되기 시작되었고, 이들을 통하여 암 면역치료법이 비약적으로 발전되었다.
전자인 면역세포가 암세포를 공격하는 기능을 활성화하는 대표적인 치료법으로 수지상세포 백신치료법을 들 수 있는데, 암세포를 인지하는 신호를 수지상세포가 림파구에 전달하여 암을 공격하는 면역시스템을 이용한 것이다. 이렇게 세포를 사용하여 면역력을 증가시키는 방법 외에 항체를 사용하여 면역력을 증가시키는 방법이 주목을 받고 있는데, 대표적으로 Rituximab는 B 세포 표면에 발현하는 CD20이라는 단백질을 인식하는 항체로 CD20에 결합하여 암세포화된 B 세포의 증식을 억제한다. 이와 비슷한 원리의 항암제로 Trastuzumab(사람 종양유전자인 Her2/neu의 유전자산물인 HER2 단백질에 특이적으로 결합함으로써 항종양효과를 나타내는 항암제) 등이 있다. 후자인 면역억제를 제어하는 방법은 PDL1 및 CTLA4와 같은 면역체크포인트를 저해하는 물질로 항체를 이용하는 것이 요점이 되는데, 대표적으로 항PDL1항체(Nivolumab, Pembrolizumab), 항CTLA4항체(ipilimumab)를 들 수 있다. 이러한 면역체크포인트억제제는 직접 암세포를 공격하는 것이 아니라 암세포를 공격하는 T 세포의 활성을 억제하는 분자의 활동을 저해하는 기능을 하기 때문에 T 세포는 암세포에 대항하는 본래의 공격성을 되찾을 수 있게 되어 항암효과를 나타낸다. 또한 상기한 두가지 치료법을 병용함으로써 치료 효과를 높일 수 있다.
본 리포트에서 다룰 내용은 최근에 그 효용성이 부각되고 있는 면역응답을 억제하는 분자의 활성을 제한하는 항체를 이용한 암면역치료법에 관한 최근의 연구 동향이 되겠다. 특히 항체중에서도 그 크기가 작고 유전자 클로닝을 통해 대량생산이 가능한 재조합 항체 단편(recombinant antibody fragment)을 이용한 방법에 초점을 두어 설명하고자 한다.
2. 본론
2.1 재조합 항체 단편
2.1.1 전체 항체(Full-sized antibody) 및 항체 단편(Antibody fragment)
항체는 Y자 형태로 간략히 표현될 수 있는데, 한개의 H chain (Heavy chain)과 두개의 L chain (Light chain)으로 구성된다. 또한 항체 중에서 항원이 결합하는 부위를 가변 영역(Variable region) 이라 하고 그 외의 부분을 정상 영역(Constant region)이라 하는데, 이들의 초기 알파벳을 조합하여 VH, VL, CH (항원결합부위에서 가까운 쪽에서부터 CH1, CH2, CH3), CL로 명명한다.
항체의 크기는 약 150 kDa인데 이보다 더 작은 크기의 항체가 필요할 경우 Fv (VH+VL), scFv (VH와 VL을 펩타이드 링커로 연결, Fv보다 항원결합력이 강함) 또는 Fab (VH+CH1과 VL+CL을 disulfide bond로 연결)와 같은 항체 단편을 사용할 수 있는데, 이들 항체 단편은 항원결합부위를 갖고 있으면서도 그 크기가 각각 약 25 kDa, 25 kDa, 50 kDa으로 Y자 형태를 띄는 전체 항체보다 작기 때문이다. 뿐만 아니라 Immunohistochemistry 및 Flow cytometry analysis를 사용하는 세포 실험에 항체가 사용될 경우 Fc (H chain 중에서 VH+CH1 이외의 부분, 즉 CH2+CH3으로 이루어진 항체의 밑기둥 부분) 수용체를 포함하는 세포를 사용하게 되면 비특이적 반응이 발생할 수 있기 때문에 이러한 경우에 Fc가 제거된 항체 단편을 사용하는 것이 유리하다.
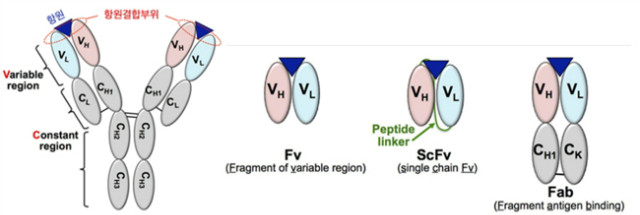
그림 1. 사람 및 마우스 등에서 발현되는 자연 항체 및 항체 단편의 모식도.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
지식
동향
발간물
- 이슈 보고서 2019 바이오미래유망기술의 이야기 - 제6화 “암 오가노이드 연계 면역세포 치료기술” 편 2019-07-29
- 이슈 보고서 2019 바이오미래유망기술의 이야기 - 제5화 “광의학 치료기술” 편 2019-07-09
- 이슈 보고서 2019 바이오미래유망기술의 이야기 - 제2화 “조직별 면역세포의 세포체 지도” 편 2019-05-16
- 정책/기획보고서 효율적 암 연구개발을 위한 국립암센터기관고유연구사업 성과분석 및 평가 2013-02-22
- 정책/기획보고서 암정복추진연구개발사업 성과분석 및 발전방안 도출을 위한 기획연구 2013-02-22


 pdf_0003080.pdf
pdf_0003080.pdf