기술동향
면역 매개성 질환에서 숙주-미생물총 간의 상호작용
- 등록일2021-06-21
- 조회수5520
- 분류기술동향 > 레드바이오 > 의약기술
-
자료발간일
2021-06-17
-
출처
생물학연구정보센터(BRIC)
- 원문링크
-
키워드
#면역매개성질환#숙주-미생물
- 첨부파일
면역 매개성 질환에서 숙주-미생물총 간의 상호작용
◈목차
1. 서론
2. 면역계의 발달
3. 장벽(gut barrier) 및 인체의 방화벽(firewall)
4. 구강 미생물총(Oral microbiota)
5. 피부 미생물총(Skin microbiota)
6. 호흡기 미생물총(Respiratory microbiota)
7. 유전, 환경 그리고 미생물총
7.1. 유전자와 미생물총 간의 상호작용
7.2. 자가면역 및 미생물총에 미치는 환경적 영향
8. 미생물총과 면역 관용
8.1. 보조 T 세포의 편향화
8.2. 방관자 면역세포의 활성화
8.3. 에피토프 확산
8.4. 교차반응
8.5. 이중 T 세포 수용체
9. 면역 매개성 질환들의 치료법
9.1. 미생물총 기반 맞춤형 치료법
9.2. 기회병원성 공생미생물 백신 접종
9.3. 기회병원성 공생미생물 백신 접종
9.4. 식이법으로 인한 장내 미생물총 구성의 변화
9.5. 균주-특이적 파지 치료법
10. 향후 전망
10.1. 자가면역질환 관련 균류
10.2. 자가면역질환 관련 바이러스
10.3. 트랜스킹덤(transkingdom) 상호작용
11. 결론
◈요약문
숙주-미생물총 간의 상호작용은 면역계(immune system)의 발달에 있어서 필수적인 생물학적 과정이다. 오늘날 보편화된 도시 문화와 현대인들의 생활방식은 숙주와 미생물총 사이의 항상성을 무너뜨리고 있으며, 이러한 현상은 현재 지속적으로 증가하고 있는 면역 매개성 질환(immune-mediated disease) 환자들의 수치와 연관성이 있을 것으로 생각되고 있다.
본 리뷰에서는 지금까지의 메타게놈(metagenome) 연구와 숙주-미생물총 간의 상호작용의 기작들에 대한 연구 결과들을 바탕으로 숙주와 미생물총 사이의 상호작용이 면역 매개성 질환에 미치는 영향과 미생물총 기반 면역 매개성 질환 치료법들에 대해 다루었다.
키워드: 숙주-미생물총 간의 상호작용, 면역 매개성 질환
분야: Immunology, Microbiology, Physiology
◈본문
1. 서론
생물체의 면역계는 병원균으로부터 숙주를 보호할 뿐만 아니라, 숙주의 다양한 기관에 서식하는 유익한 미생물총이 숙주와 함께 공생할 수 있도록 발달되었다. 건강한 인체 내에서 면역 관용 (immunological tolerance)은 조절 T 세포(regulatory T cell, Tregs)에 의해 유지되지만, 조직 손상 등의 현상으로 인해 항상성 동요 (homeostatic perturbation)가 발생하게 되면, 면역 관용은 무너지며, 이로 인해 과도한 면역 반응들이 유도되어 면역 매개성 질환들이 일어난다.
일반적으로 면역 매개성 질환들은 자가 항원(self-antigens), 이식된 항원(transplanted antigens), 꽃가루나 먼지와 같은 환경 물질들에 의해 면역 세포들이 과도하게 활성화되어 발생하나, 체내에 특정 항원의 결여로 인한 염증으로 인해 일어나기도 한다. 본 리뷰에서 중점적으로 다룬 미생물총(microbiome)은 면역 매개성 질환들의 발병 원인 중 하나로 숙주와 미생물총 사이의 비정상적인 상호작용은 면역 세포들의 과도한 활성을 유도하여 면역 매개성 질환들을 일으킨다.
예를 들어, 내부적 또는 외부적 요인들로 인해 인체의 기관계들의 항상성이 무너져 공생균들이 기존의 서식지를 벗어나 다른 기관으로 이동하게 되면 이 생물체들은 그곳에서 면역세포들을 자극하여 면역 관용을 파괴시킨다. 본 리뷰에서는 숙주와 미생물총 간의 상호작용에 의해 발달된 면역 반응과 이러한 면역 반응이 면역 매개성 질환들을 일으키는 기작에 대해 다루었다.
본 리뷰가 제공한 정보들은 향후 미생물총 기반 면역 매개성 질환 치료제를 개발하는데 있어서 중요한 실마리를 제공할 것이다.
2. 면역계의 발달
면역계는 감염 초기에 작용하는 선천 면역(innate immunity)과 감염 후기에 반응하는 후천/ 획득 면역(adaptive/ acquired immunity)으로 나뉜다. 선천 면역은 1차 방어 수단으로 감염 초기에 작용하기 때문에 항상 활성화되어 있거나, 즉각적으로 활성화될 수 있는 상태를 유지한다.
선천 면역에 관여하는 대표적인 세포들로는 대식세포(macrophage), 자연 살생 세포(natural killer cell, NK cell), 수지상 세포(dendritic cell) 등이 있으며, 이 세포들은 표면에 위치한 패터인식수용체(pattern recognition receptor, PRR)를 통해 지질다당류(lipopolysaccharide, LPS)와 같은 병원균 특이적인 물질들을 인식함으로써 활성화된다.
반면, 후천 면역은 2차 방어로 작용하는 시스템으로 선천 면역이 감염 물질을 처리하지 못하는 경우에 작동하여 이물질들을 제거한다. 척추동물들의 경우에는 선천 면역과 후천 면역이 서로 상호작용함으로써 비자기(non-self) 물질들을 인식하여, 이물질들을 선택적으로 제거하는 동시에 자가 물질들이 최소한의 손상을 입도록 한다.
이와 같은 균형적인 면역계로 인해 숙주와 미생물총은 공존하면서 서로의 생존에 이익을 제공하는 관계를 형성한다. 예를 들어, 위장관(gastrointestinal tract)에 서식하는 알칼리게네스(Alcaligenes)와 림프 조직(lymphoid tissue)에 서식하는 박테리아들은 인터루킨-10(interleukin-10, IL-10)의 분비를 자극함으로써 숙주 세포의 염증 반응을 억제하는 동시에 박테리아의 군집화(colonization)를 안정화 시킨다.
하지만, 특정 작용 또는 현상으로 인해 미생물총의 불균형이 발생하게 되면, 숙주와 미생물총 사이에 비정상적인 상호작용 일어나며, 그 결과 면역 항상성이 무너져 자가면역(autoimmunity), 알레르기(allergy), 만성 염증성 질환(chronic inflammatory disease) 등의 면역 매개성 질환들이 발생한다.
숙주와 미생물총 간의 상호작용에 악영향을 미치는 대표적인 요소로는 항생제와 위생 시설이 있다. 1928년 영국 미생물학자인 알렉산더 플레밍(Alexander Fleming)이 페니실린(penicillin)을 처음 발견한 이래로 인류의 평균 수명이 증가하였지만, 항생제의 남용으로 인해 숙주와 미생물총 사이의 상호작용이 무너졌으며, 이러한 결과는 지난 수십 년 동안 증가한 면역 매개성 질환 발생률과 상관관계가 있을 것으로 생각되고 있다.
3. 장벽(gut barrier) 및 인체의 방화벽(firewall)
장내 미생물총에 의한 과도한 면역 반응을 피하는 가장 효과적인 방법은 장벽을 튼튼하게 유지하는 것이다. 건강한 장은 상피세포(epithelial cell)와 점막층(mucosal barrier)으로 둘러싸여 있으며, 다양한 화학 물질들(예: 분비형 면역글로불린 A, 항균 펩티드 등)의 보호를 받고 있다.
장내 미생물총 또한 다양한 방법을 통해 숙주의 장벽 온전성(integrity)에 기여하는데 이들은 톨-유사 수용체(Toll-like receptor, TLR), NOD-유사 수용체(nucleotide-binding oligomerization domain-like receptor, NLR) 등 면역 반응에 관여하는 수용체들을 활성화시켜 장벽 항상성 유지와 림프 조직(gut-associated lymphoid tissue, GALT)의 발달에 영향을 주며, 상피세포를 자극하여 혈청 아밀로이드 A(serum amyloid A)를 생산함으로써, 장내 도움 T17 세포(helper T 17 cell)의 후천성 면역 반달에 기여한다.
그 외에도 식이섬유 물질이 풍부한 음식물의 섭취로 인하여 장내 미생물들에 의해 생산되는 짧은 사슬 지방산(short chain fatty acids, SCFAs)은 Tregs의 생산을 촉진하여 항염증성(anti-inflammatory) 환경을 조성함으로써 장벽 항상성을 유지한다. 따라서, 장내 미생물총의 불균형은 과도한 면역 세포 반응을 일으켜 염증성 장 질환(inflammatory bowel disease, IBD)과 같은 장 특이적 면역 매개성 질환을 야기한다.
장내 미생물총에 의한 면역 반응은 장에만 국한되어 있지 않다. 장내 미생물총이 장과 관련된 기관들에도 영향을 미친다는 사실이 이미 여러 연구들을 통해 입증되었다. 기관형성(organogenesis) 과정에서 위장관과 마찬가지로 내배엽(endoderm)에서 발생하는 췌장(pancreas)은 비교적 위장관과 인접하여 위치해 있기 때문에, 장내 미생물총이 쉽게 이동할 수 있는 기관이다.
특정 기관에 서식하던 미생물총이 다른 기관으로 이동하는 현상을 “전위(translocation)”라고 하는데, 이와 같이 미생물총이 기존에 서식하던 기관에서 다른 기관으로 전위하게 되면, 과도한 면역 반응이 유도되어 면역 매개성 질환이 일어난다. 예를 들어, 장내 미생물총의 전위가 췌장에서 발생하는 경우, 이 기관에서 면역 세포들이 과도하게 활성화되어, 자가면역에 의한 제1형 당뇨병(type 1 diabetes, T1D) 또는 췌장염(pancreatitis)이 일어날 수 있다.
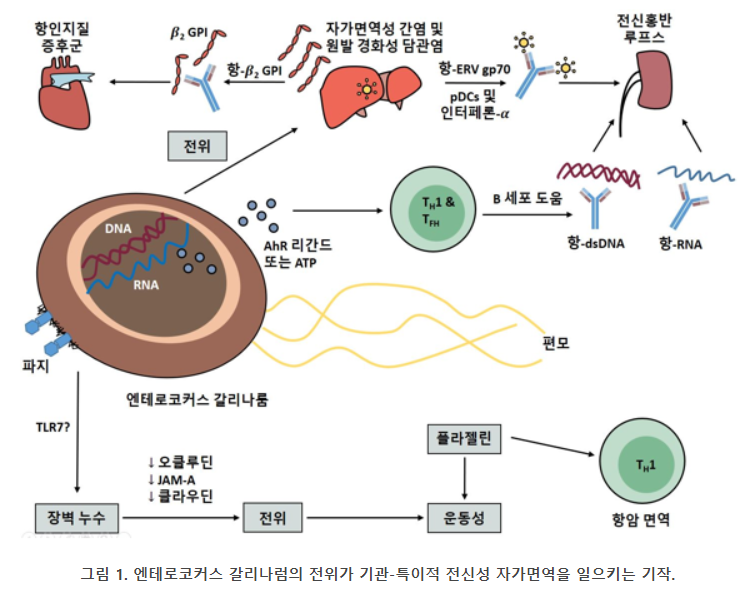
간(liver) 또한 내배엽에서 발생하는 기관들 중 하나로 장내 미생물총의 전위로 인해 과도한 면역 반응이 발생할 수 있다. 예를 들어, 장내 미생물 중 하나인 엔테로코커스 갈리나럼(Enterococcus gallinarum)은 소장(small intestine)에서 장간막림프절(mesenteric lymph node, MLN), 간, 비장(spleen) 등의 기관으로 전위하여 조직 자가면역(systemic autoimmunity)을 일으킨다 (그림 1).
또 다른 예로 클렙시엘라 뉴모니아(Klebsiella pneumonia)는 장벽을 손상시켜 간으로 이동하여 다른 기회병원성 공생미생물과 함께 TH17을 자극하여, 염증 반응을 유발함으로써 원발 경화성 담관염(primary sclerosing cholangitis, PSC)을 일으킨다. 장내 미생물의 전위와 면역 매개성 질환의 상관관계는 최근에 전신홍반루푸스(systemic lupus erythematosus, SLE) 환자들과 자가면역 간염(autoimmune hepatitis) 환자들을 바탕으로 진행된 생체 조직 검사에서 엔테로코커스 갈리나럼의 DNA가 검출됨에 따라 이러한 사실이 다시 한 번 입증되었다.
이와 같은 결과들은 간, MLN, 비장 등 장 관련 기관들이 장내 미생물총에 의한 자가면역에 취약하며, 이 기관에서 발생하는 자가면역은 전신성 자가면역 질환(systemic autoimmune disease)으로 이어질 수 있음을 의미한다.
숙주와 장내 미생물총 사이의 상호작용은 장-간 축(gut-lung axis)뿐만 아니라 신경계(nervous system)와 같은 기관계에서도 작용한다. 뇌는 앞서 언급한 기관들에 비해 장으로부터 비교적 멀리 위치하며, 위장관과는 달리 외배엽(ectoderm)에서 발생하지만, 이 기관 또한 장내 미생물총의 영향을 받는다.
뇌의 경우, 아직까지 장내 미생물총의 전위가 관찰된 바 없으며, 혈액뇌관문(blood-brain barrier, BBB)으로 인해 장내 미생물총의 전위가 불가능한 것으로 생각되고 있으나, 장내 미생물들이 생산하는 물질들이 장-뇌 축(gut-brain axis)을 통해 중추 신경계(central nervous system, CNS)를 자극하여 숙주의 행동에 영향을 미치는 것으로 알려져 있다.
5. 피부 미생물총(Skin microbiota)
피부를 포함한 대부분의 장기들의 표면에서도 고유의 미생물총이 발견된다. 대표적인 예가 스타필로코커스 에피더미디스(Staphylococcus epidermidis)로 이 균주는 황색도도상구균(Staphylococcus aureus)과 같은 병원균이 피부에 정착하는 것을 방지한다. 장내 미생물총과 마찬가지로 피부 미생물총의 불균형 또한 다양한 경로를 통해 국소 또는 전신 면역 반응을 과도하게 활성화시킴으로써, 피부 관련 자가 면역 질환을 일으킨다.
아토피 피부염(atopic dermatitis)의 경우에는 피부 미생물총과 T 세포 사이의 상호작용에 의해 발생한다. 사람을 비롯한 모든 동물들은 출생 시 피부에 존재하는 공생균에 노출되면서, Tregs는 이들에 대한 면역 관용을 획득하며, 기억 T 세포(memory T cell) 및 효과 T 세포(effector T cell)가 생성된다.
이러한 T 세포들의 기능 상실은 제2형 도움 T 세포(type 2 helper T cell, TH2)에 의한 상처 치유 경로를 지속적으로 활성화시켜 아토피성 피부 염증 질환들을 일으킨다.
SLE, 쇼그렌 증후군(Sjogren’s syndrome)과 같은 자가면역질환의 경우에는 피부 미생물총에 의한 항원 교차 반응성(antigen cross-reactivity)에 의해 발생한다. 이 질환을 앓고 있는 대부분의 환자들은 공생균이 생산하는 Ro60의 동일 조상 단백질(orthologue)에 대한 항체를 가지고 있으며, 항-Ro60-양성(anti-Ro60 positive) 루푸스 환자의 혈청을 공생균의 Ro60 리보핵산단백질(ribonucleoprotein)과 반응시키면 면역침전(immunoprecipitation)이 일어난다.
추가적으로, Ro60 생산 장내 미생물들을 무균 쥐(germ free mouse)에 이식하였을 때, 면역 복합체 침착(immune complex deposition)으로 인한 신장염(nephritis)이 발생하는 현상이 관찰된 바 있다.
장-피부 축(gut-skin axis)은 미생물총이 피부 자가면역을 일으키는 또 하나의 경로로 이러한 기작을 통해 일어나는 대표적인 피부 질환으로는 백반증(vitiligo)이 있다. 이 질환은 T 세포에 의한 자가면역 질환으로 피부 멜라닌 세포(melanocyte)의 손상에 의해 일어난다. 암피실린(ampicillin)의 복용과 백반증의 상관관계를 증명하는 실험 결과가 보고된 바 있으며, 아직까지 정확한 기작은 밝혀지지 않았지만, 암피실린에 의한 장내 미생물총의 구성에 변화가 백반증을 야기한다고 생각되고 있다.
6. 호흡기 미생물총(Respiratory microbiota)
호흡기 관련 면역 매개성 질환은 폐의 혈액-공기 장벽(blood-air barrier)에 서식하는 미생물총의 불균형에 의해 발생한다. 집 먼지 진드기(house dust mite)가 TH2 사이토카인(TH2 cytokine)의 양을 증가 시켜, 기도 호산구 증가증(airway eosinophilia)을 악화시키는 현상과 에어로졸화된 오브알부민(aerosolized ovalbumin)이 NK T 세포의 수치를 증가시키는 현상들이 동물실험을 통해 확인된 바 있다.
이러한 현상들은 신생아 쥐의 경우, 미생물총의 균형을 통해 완화되었지만, 성체 쥐의 경우에는 미생물총에 의한 효과를 보지 못했다.
호흡기 관련 면역 매개성 질환들은 폐에 서식하는 미생물총뿐만 아니라, 장내 미생물총에 의해서도 일어난다. 장내 박테리아의 대사 물질인 SCFAs는 폐의 TH2 사이토카인의 수치를 감소시키는 동시에 Tregs의 수치를 증가 시켜 천식(asthma)과 같은 알레르기성 기도 질환을 예방한다.
아직까지 장내 미생물의 전위로 인한 호흡기 관련 면역 매개성 질환들의 발생이 관찰된 바는 없으나, 패혈증(sepsis) 환자로부터 박테로이데스(Bacteroides)와 엔테로코커스(Enterococcus spp.) 등의 장내 미생물들이 폐로 전위하는 현상이 관찰된 바 있기에 장내 미생물의 전위가 호흡기 관련 면역 매개성 질환들을 발생시킬 수 있는 가능성이 열려있다.
장내 기생충의 경우에는 장-폐 축을 통해 TH2와 면역글로불린 E(immunoglobulin E, IgE)의 수치를 증가 시켜 면역 매개성 질환의 발병률을 감소시킨다. 이러한 결과는 장내 기생충이 비교적 적은 선진국 사람들에게서 아토피성 질환의 발병률이 높은 현상과 일치한다.
장내 기생충은 면역 활성 이외에도 장내 미생물총의 구성을 더욱 다양화시킴으로써, SCFAs와 폐의 Tregs의 수치를 증가 시켜 천식의 발병률을 감소시킨다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보


 pdf_0003821.pdf
pdf_0003821.pdf