기술동향
T 세포 및 NK 세포를 이용한 세포 치료제 개발 현황
- 등록일2021-07-09
- 조회수5801
- 분류기술동향 > 레드바이오 > 의약기술
-
자료발간일
2021-07-06
-
출처
생물학연구정보센터(BRIC)
- 원문링크
-
키워드
#t세포#nk세포#세포치료제
- 첨부파일
T 세포 및 NK 세포를 이용한 세포 치료제 개발 현황
◈목차
1. 서론
2. 본론
2.1. 세포 치료법이란?
2.2. 세포 치료제의 종류
2.2.1. 키메릭 항원 수용체 발현 T 세포(Chimeric Antigen Receptor-T, CAR-T)
2.2.2. T 세포 수용체 T 세포(T Cell Receptor-T, TCR-T)
2.2.3. 세포독성 T 림프구(Cytotoxic T Lymphocyte, CTL)
2.2.4. 종양 침투 림프구(Tumor Infiltrating Lymphocyte, TIL)
2.2.5. 자연살해세포(Natural Killer cell, NK cell)
2.2.6. 키메릭 항원 수용체 발현 자연살해세포(Chimeric Antigen Receptor-Natural Killer cell, CAR-NK)
3. 결론
4. 참고문헌
◈요약문
암은 전 세계적으로 많이 발병되면서 높은 사망률을 보이는 질병이다. 이러한 암을 치료하기 위한 방법으로는 수술요법, 방사선 요법, 화학요법 그리고 현재 많이 각광받고 다양한 방법의 연구가 이루어지고 있는 면역치료요법이 있다. 면역치료요법은 생체 내 면역시스템을 이용하는 방법으로 다른 치료법들의 한계점을 극복할 수 있는 방법으로 제시되는 치료법이다. 본 글에서는 면역치료요법 중 많이 개발되고 있는 세포 치료제의 연구 동향에 대해 논하고자 한다.
키워드: Cancer therapy, Immunotherapy, CAR-T, CAR-NK
분야: Cancer Biology/Oncology, Immunology, Medicine
◈ 본문
1. 서론
암은 다양한 요인에 의해 세포의 비정상적인 성장을 유도하여 발생하는 질병으로서, 전 세계적으로 많이 발병되는 질환이다. 2015년 세계보건기구(World Health Organization, WHO)의 보고에 따르면, 암은 172개국 중 91개국에서 1~2위, 22개국에서는 3~4위의 사망원인으로 보고된 질병이다.
그리고 2018년 기준으로 전 세계에서 1,800만 명의 새로운 암 환자가 발생하고, 960만 명의 암 환자가 사망한다고 보고되었다. 또한, 한국에서도 마찬가지로 암이 사망원인 1위이며 다른 원인들보다 최소 3배 이상 높은 사망률을 보였고 매년 그 수가 증가하고 있다고 보고되었다. 이렇듯 암은 예전부터 많은 연구가 되었고 치료율도 많이 증가하였지만, 아직까지 높은 발병률과 사망률을 보이는 질병이다 [1, 2].
이러한 암을 치료하는 방법으로는 수술요법(Surgery), 방사선요법(Radiotherapy), 화학요법(Chemotherapy) 그리고 현재 각광받고 있는 면역 치료법(Immunotherapy)이 있다 [3]. 일반적으로 암 치료법으로는 수술•방사선•화학요법이 사용되고 있지만, 각각의 한계점 및 부작용이 있다.
수술 요법의 경우 전이성 암 환자에게는 적용이 어려우며, 방사선 및 화학요법의 경우 암세포뿐만 아니라, 정상세포에도 영향을 주는 강한 독성으로 생체 시스템을 무너뜨려 다양한 부작용을 보인다. 이러한 한계점 및 부작용을 최소화할 수 있는 방안으로 면역치료요법이 제시되었고, 전 세계적으로 많은 연구소에서 관심을 보이며 다양한 방법으로 치료에 개발 연구를 진행하고 있다.
면역치료요법은 생체 내 면역 시스템의 활성 및 억제를 통하여 암의 성장 억제/ 제거하는 치료법이며, 그 방법으로는 항원제시세포로써 우수한 기능을 가진 수지상 세포를 이용하여 생체 내 암 특이적인 CD8 T 세포의 형성을 유도하는 수지상 세포 백신(Dendritic cell-based vaccine), 면역세포의 활성을 저해하는 세포 표면 신호 전달 단백질을 억제하여 면역세포의 암에 대한 활성을 증진시키는 항체 치료법(Immune checkpoint inhibitor, ICI) 그리고 세포 독성이 높으며 암을 특이적으로 살상할 수 있는 기능을 가진 NK/T 세포를 이용한 세포 치료법(Cell therapy) 등이 있다.
수지상 세포 백신의 경우, 암 특이적인 항원이 있어야 적용이 가능한데, 현재 이를 적용하여 다양한 암 종에 대해 연구하고 있지만, 특이적으로 발현되는 암 항원이 극소수이기에 적용이 제한적이다. 그리고 항체의 경우, 현재 임상 적용 및 다양한 암 종에 대해 효능이 증명되어 사용 중에 있는 제제이다.
하지만, 항체의 타겟 단백질이 암세포에서 과발현되지 않은 경우 사용이 제한되고, 단독 치료법으로 적용 및 효능은 높지 않다고 보고되었다. 최근에 많은 연구가 되고 있는 세포 치료제는 암세포에 특이적으로 세포 독성 반응을 보이는 면역세포를 이용하여 면역시스템의 활성을 유도함으로써 암을 치료할 수 있도록 하는데 중점을 둔 치료법이다. 저자는 이 리포트에서 현재 시점을 중점으로 이루어 지고 있는 연구 및 개발을 하고 있는 세포 치료제에 대해 다루고자 한다 [4, 5].
2. 본론
2.1. 세포 치료법이란?
세포 치료법은 면역 치료법 중 한 가지 방법으로 세포의 약용 효과를 이용하여, 환자에게 주입하여 치료하는 치료법으로, 암의 경우 세포 매개 면역을 유도할 수 있는 T 세포 또는 NK 세포를 이용하는 방법이다. 이러한 면역 세포 치료법은 암 치료에 대한 다른 치료법들의 전이성 암에 적용 불가하거나, 정상세포에도 좋지 않은 영향을 줄 수 있는 제한요소들을 극복할 수 있는 방안이라고 생각한다. 또한, 면역 시스템의 활성을 유도가 국소부위에서만 발생되는 것이 아닌 생체 전반적으로 발생 및 작용을 유도하여 전이성 암종 및 재발을 예방 할 수 있는 방법으로도 제시 될 수 있을 것이다.
현재, 국내•외 많은 연구소들에서 강력한 세포 독성 기능이 있는 T 세포 및 NK 세포를 이용한 세포 치료제 연구가 진행되고 있다. 같은 종에서 추출한 정상세포를 이용한 동종 세포 또는 환자에게 추출한 자가 세포를 이용한 세포 치료 연구를 하고 있으며, 이 세포들의 암에 대한 특이적인 반응과 살상능력을 증진시키기 위하여, 유전자 삽입 및 제거 기술(CAR or TCR engineering)을 이용하고 있다.
일반적으로 암세포에 과발현되어 있는 세포 표면 단백질을 찾아 이를 인식할 수 있는 키메릭 항원 수용체(Chimeric Antigen Receptor, CAR)를 발현 시켜, T 세포 또는 NK 세포가 암세포에 활성 반응이 유도되어 암을 제거할 수 있도록 하는 방법을 적용하여 사용하고 있다. 암세포를 특이적으로 인식하기 위한 다른 접근 방법으로는, 암세포에만 특이적으로 반응할 수 있는 T 세포 수용체(T cell Receptor, TCR)를 이용한 세포 치료 방법이 있다. 이렇듯 세포 치료제는 암세포를 타겟하고 인식할 수 있는 기능을 부여 받아 적용되기에 조직에서 성장하고 있는 원발암 종양뿐만이 아닌, 전이되어 있는 암도 같이 타겟팅하여 제거할 수 있다 [6-12].
더 나아가, 이 세포 치료제로 인한 생체 내 면역시스템 활성으로 인하여 자발적인 암 특이적인 면역세포들이 형성되어 추후의 암의 재발 또한 예방할 수 있게 도울 수 있을 것이다. 그렇기에 현재 많은 연구소들에서 면역세포를 이용한 항암면역치료제 개발에 많은 투자와 관심을 갖는 것이라 생각한다.
그림 1. 세포 치료제의 임상 사용법.
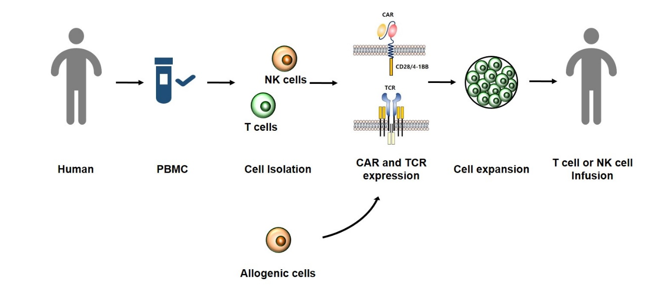
2.2. 세포 치료제의 종류
2.2.1. 키메릭 항원 수용체 발현 T 세포(Chimeric Antigen Receptor-T, CAR-T)
키메릭 항원 수용체는 현재 세포 치료제에 많이 적용하여, 연구 및 개발이 되고 있는 방법으로 암세포에 특이적으로 과발현되어 있는 표면 단백질을 타겟으로 하여, T 세포가 암세포에 활성 반응을 보여 암의 세포 사멸을 유도하는 방법이다. 많은 항원(CD19, CD20, HER2, MSLN 등)에 대해 연구가 되었고 개발되어 다양한 암종에 대해 임상 적용되고 있으며, 특히, 혈액암(Hematologic malignancy)에서 우수한 효과를 보이고 있다.
CAR-T 세포는 암 항원을 인식하게 되면, 세포가 활성화되어 세포 독성 능력을 나타내도록 유전자 삽입을 하였고, 일반적으로 T 세포의 주조직적합성복합체(Major Histocompatibility Complex, MHC)-T 세포 수용체(T cell receptor, TCR) 및 2차 신호전달체계 없이도 세포 활성을 나타나게 하였다. 이를 “CAR-T”라고 명명하여 사용되며, 현재는 기존의 1세대 CAR-T부터 활성 및 증식을 증진시킨 4세대 CAR-T 까지 발전되어 연구가 되어 있다. CAR의 하위 신호 전달 체계에 TCR의 전달체계를 이용하여 MHC-TCR 활성 효과가 나타나도록 하였고, 현재 임상 연구에는 2~3세대 CAR-T 세포가 적용 연구되고 있다 [6-12].
하지만, 키메릭 항원 수용체는 세포 표면의 항원만 인식할 수 있고, 이 항원이 암세포에 특이적으로 과발현 되어있지만, 적게 발현되어 있는 정상세포에도 반응을 할 수 있다. 그리고, 혈액암에 대해서 우수한 효과를 보이지만, 신경독성 및 사이토카인 방출(Cytokine Release Syndrome, CRS)이라는 부작용이 있다고 보고되었다. 또한, CAR-T 세포 치료법은 혈액암에서는 효능을 보이지만, 고형암에서는 그 효과가 미미한 것으로 나타났다. 이를 보완하기 위해 면역 활성에 도움을 줄 수 있는 사이토카인 유도 신호 전달을 이용한 4세대 CAR-T 세포 연구가 되고 있다.
암에 특이적으로 반응할 수 있는 TCR을 이용하는 것은 제한적이기에 좀 더 광범위하게 작용하여 암을 제거할 수 있는 CAR를 이용한 세포 치료제 개발은 국•내외(NORVATIS, GILEAD, MJCELLBIO, Celgene, TESSA Therapeutics, 녹십자 Cell)에서 활발하게 연구가 진행되고 있다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보


 pdf_0003830.pdf
pdf_0003830.pdf