기술동향
미국 FDA 2022년 회계년도 심사수수료 확정
- 등록일2021-08-18
- 조회수3892
- 분류기술동향 > 레드바이오 > 의약기술
-
자료발간일
2021-08-17
-
출처
한국바이오협회
- 원문링크
-
키워드
#미국 FDA #회계년도#심사수수료
- 첨부파일
미국 FDA 2022년 회계년도 심사수수료 확정
◈본문
- 전문의약품 신약 심사수수료 사상 처음 3백만 달러 넘어 -
- 전년대비 제네릭의약품 2만 8천달러 인상,의료기기 사전허가비 9천달러 인상 -
- 바이오시밀러 신청비는 동결,바이오시밀러 개발지원 프로그램비는 44.2% 인하 -
◊ 금년 10월부터 시작되는 미국 mA의 2022년 회계연도 예산이 미국 상원 예산위원회에서 전년보다 2억 달러가 증가한 3414억 달러로 통과됨.
- 동 예산에는 27.23억 달러의 의약품,의료기기 등의 이용자 부담금(User Fee)이 포함
◊ 27.23억 달러의 이용자 부담금에는 기업들이 전문의약품 심사신청시 내야 하는 전문의약품 이용자부담금이 11.42억 달러,제네릭의약품 이용자부담금 5.28억 달러,바이오시밀러 이용 자부담금 0.43억 달러,의료기기 이용자부담금 2.41 억 달러 등이 포함
- 이외에 동물용의약품,동물용제네릭의약품 등이 이용자 부담금에 포함
◊ 이용자부담금은 기업들이 FDA에 의약품이나 의료기기 등의 시판 허가 등을 위해 내야 하는 심 사수수료로 의약품이나 의료
기기의 종류별로 비용에 차이
- 중소기업이나 희귀의약품 등의 여부에 따라 비용은 면제 또는 감면됨.
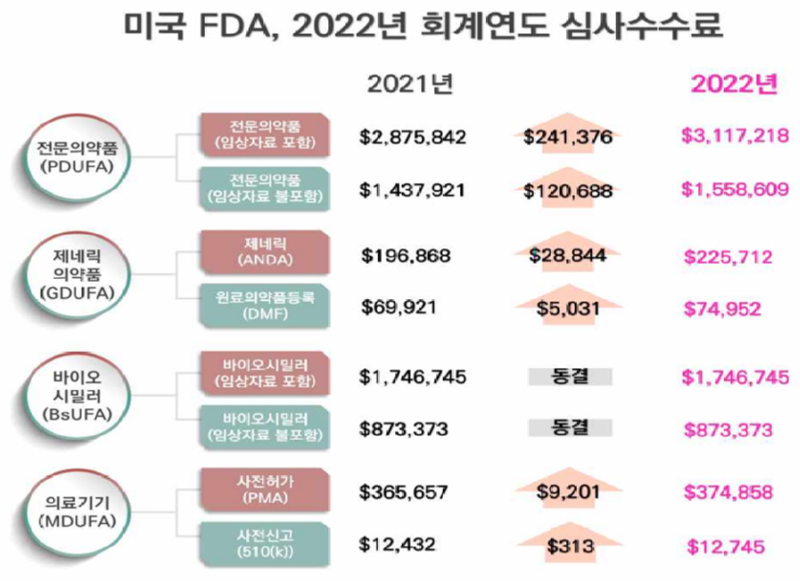
◊ 미국 FDA 2022년 회계연도의 의약품 및 의료기기 심사수수료(이용자 부담금)는,
- 전문의약품 신약 신청비용은 3,117,218달러(약 24억원)로 전년에 비해 241,376달러 증가 - 제네릭의약품 신청비용은 225,712달러로 전년에 비해 28,844달러가 증가
- 바이오시밀러 신청비용은 1,746,745달러로 전년과 동일. 다만,바이오시밀러 개발지원 프로 그램비는 초기 및 연간 비용이 각각 45,310달러씩 인하
- 사전허가가 필요한 의료기기 신청비용은 374,858달러로 전년에 비해 9,201달러 증가
◊ 의약품이나 의료기기는 시장에 출시되기 전에 여러 단계의 복잡한 공급 사슬을 거치고,점점 관련된 인허가 규제 업무가 복잡해지고 새로운 규제 환경이 도입되어야 하는 현실 등이 반영 되어 규제기관의 심사수수료는 증가 추세에 있음.
O 한국의 경우,신약(신규 생물의약품 포함)의 품목허가 신청비용은 8,031,000원,의료기기 제 조•수입 허가신청 비용은 1,495,000원으로,한국의 심사수수료는 미국에 비해 신약은 0.23%, 의료기기는 0.36% 수준이 됨. (환율 1,100원/$ 적용시)
〈참고〉미국 FDA, 2022년 회계연도 이용자부담금(User Fee) 중 일부 내용 요약
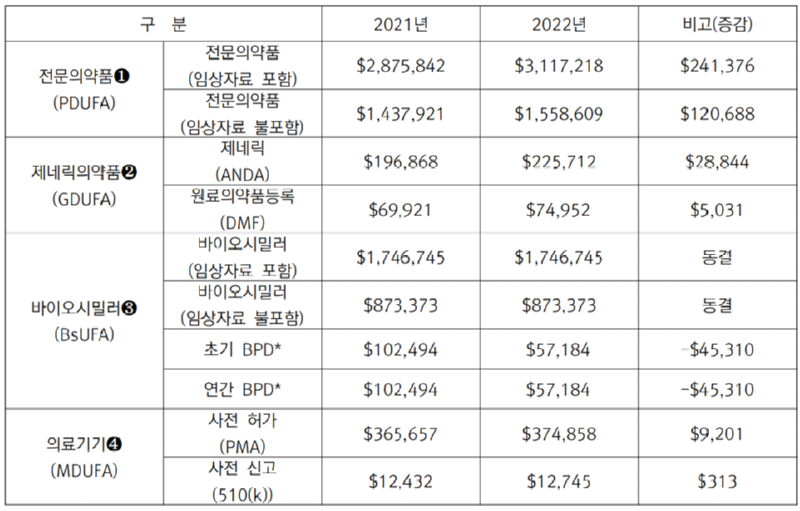
◎전문의약품의 경우 전문의약품 이용자부담금법(PDUFA: Prescription Drug User Fee Act)에 따라 정해지며, 임상시험 자료 검토 필요 여부에 따라 비용 2배 차이(필요한 경우 필요없는 경우보다 2배 높음)
◎제네릭의약품의 경우 제네릭의약품 이용자부담금개정법(GDUFA: Generic Drug User Fee Amendments)0]] 따라 정해지며, 원료의약품 또는 완제의약품 시설이나 해외나 국내 소재 여부에 따라 비용 차이
◎바이오시밀러의 경우 바이오시밀러 이용자부담금개정법(BsUFA: Biosimilar User Fee Amendments)에 따라 정해지며, 전문의약품과 마찬가지로 임상자료 심사 필요 여부에 따라 비용 2배 차이
* Biological product developmentffiPD)는 바이오시밀러의 개발 및 승인을 신속하게 진행시키기 위한 미국 FDA 심사관과 기업과의 공식적인 미팅 프로그램으로 초기(Initial BPD)와 연간(Amiual BPD)으로 구분
◎의료기기의 경우 의료기기 이용자부담금개정법(MDUFA: Medical Device User Fee Amendments)0]] 따라 정해 지며, 사전허가나 사전신고가 필요한 경우나 신기술(De novo) 의료기기 등에 따라 비용 차이
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보
지식


 미국 fda 2022년 회계년도 심사수수료 확정_한국바이오협회.pdf
미국 fda 2022년 회계년도 심사수수료 확정_한국바이오협회.pdf