기술동향
p53 돌연변이를 타겟하는 효과적인 암 치료
- 등록일2019-08-06
- 조회수15624
- 분류기술동향
-
자료발간일
2019-08-01
-
출처
생물학연구정보센터(BRIC)
- 원문링크
-
키워드
#p53#oncogene#tumor suppressor gene
- 첨부파일
p53 돌연변이를 타겟하는 효과적인 암 치료
도 민 재 KAIST 화학과
[요약]
종양 억제 유전자 TP53은 암에서 가장 빈번하게 돌연변이가 발생하는 유전자다. 야생형(wild type) p53은 여러 경로로 종양 발달을 억제할 수 있다. 그러나 TP53의 돌연변이로 인해 p53이 비활성화되면 종양 세포의 사망 기작을 회피하고 빠르게 증식할 수 있게 된다. TP53 돌연변이 의 높은 빈도 때문에 돌연변이 p53의 정상 기능을 회복시키고, 이에 따라 종양 세포의 사망 유도하여 암을 치료하려는 노력이 이루어져 왔다. 서로 다른 전략을 통해 미스센스(missense) 돌연변이 p53 단백질을 재활성화시킬 수 있는 작은 분자들이 확인되었으며, 두 가지 화합물을 현재 임상실험을 거치는 단계이다. 본 총설 논문에서는 돌연변이 p53의 약리적 재활성화와 관 련된 최근 진행 상황을 논의하고, 이러한 전략의 문제와 해법을 알아본다.
Key Words: p53, oncogene, tumor suppressor gene, missense mutation, nonsense mutation
[목차]
1. 서론
2. p53의 구조와 돌연변이
3. 미스센스 돌연변이 표적 치료
4. 넌센스 돌연변이 표적 치료
5. 결론
[내용]
1. 서론
p53 전사 인자는 DNA 손상이나 원암유전자 활성 등의 스트레스 조건에서 켜지게 되는 세 포의 스트레스 센서 기능을 한다. 정상 조건에서 p53 단백질 수준은 p53이 프로테아좀(proteasome) 을 통해 분해될 수 있도록 하는 E3 유비퀴틴(ubiquitin) 단백질 접합효소(ligase)인 MDM2에 의해 음 성피드백(negative feedback) 조절을 받고 있기 때문에 낮은 편이다. 세포 스트레스는 p53, MDM2 단 백질에 대한 인산화 작용을 통해 p53과 MDM2의 결합을 방해하고, p53 아세틸화를 자극하여 p53 축적과 활성화를 이끌어 낸다. 그 결과 p53이 타겟하는 p21 단백질을 생성하는 CDKN1A (dependent kinase inhibitor 1A), 그리고 세포 사멸을 조절하는 BAX (BCL2 associated X), BBC3로도 알려진 (PUMA p53 upregulated modulator of apoptosis), PMAIP1로도 알려진 NOXA 등의 유전자들을 발현시 킨다. 이를 통해 세포 주기를 억제하고 세포 사멸을 유도하게 된다. 최근의 연구에 의해 p53이 SLC7A11 유전자가 인코딩(encoding)하는 시스테인(cysteine)/글루타메이트(glutamate) 역수송체 (antiporter) XCT의 발현을 감소시키고, GLS2 유전자가 인코딩하는 글루타미나제(glutaminase) 2의 발 현을 증가시켜서 대사를 조절하여 세포가 페로토시스(ferroptosis)에 의한 죽음에 민감하도록 만들 수 있다는 것이 알려졌다. 또한 p53은 TIGAR 유전자가 인코딩하는 해당 과정 조절 포스타파아제 (phosphatase)와 같은 효소들의 발현을 증가시킨다는 것도 알려졌다. 게다가 p53은 DNA 수리, 분화, 줄기세포 재생 등 다양한 세포 과정에 관여한다. 종양성 스트레스는 p53과 관련된 DNA 손상 반응 신호전달 경로를 자극하는데, 이는 발암과정의 주요한 장벽 중 하나이다.
TP53 유전자의 체세포 돌연변이는 인간의 종양에서 자주 일어난다. TP53 생식세포 돌연변이 는 LFS 증후군(Li?Fraumeni cancer predisposition syndrome)과 관련이 있다. 또한 p53 결핍 쥐에서 발견되는 높은 종양 비율은 p53의 중요한 종양 억제 역할을 한다는 확실한 증거가 된다. 그러나 p53 매개 종양 억제의 정확한 메커니즘은 완전히 파악되지 않고 있다. p53 의존적 세포 주기 억제와 사멸 경로는 오랫동안 p53 매개 종양 억제에 결정적이라고 생각되어 왔다. 놀랍게도 최근의 데이터 는 CDKN1A, BAX, PUMA, NOXA의 발현 증가를 통한 세포 주기 억제 및 사멸을 유발하는 p53의 능 력이 생체 내 실험에서 p53 매개 종양 억제에 불필요한 것으로 드러났다. 대신 대사와 산화환원 (redox) 균형에 관여하는 p53 표적 유전자들인 TIGAR, FDXR (ferredoxin reductase), PRKAB1 (protein kinase AMP-activated non-catalytic subunit beta 1) 및 SENS1 (sestrin 1)이 p53 종양 억제 경로에서 핵심적인 역할을 할 수 있다.
TP53 유전자는 지금까지 알려진 인간 암에서 가장 빈번하게 변이가 발생한 유전자로, 종양 발생 중 TP53 비활성화에 대한 강한 선택압(selective pressure)의 존재를 나타낸다. RB1, APC (adenomatous polyposis coli), PTEN과 같은 종양 억제 유전자의 돌연변이와는 대조적으로, 대부분의 TP53 돌연변이는 미스센스 돌연변이다. 더욱이 많은 돌연변이는 p53 단백질의 GOF (gain-of-function) 활동을 획득하여, p53 그룹의 다른 구성원인 종양 단백질 p63과 p73을 비활성화할 수 있게 된다. 따 라서 종류에 따라 정도의 차이는 있지만 미스센스 돌연변이가 있는 TP53은 종양 진행을 활발히 촉 진하는 원암유전자(oncogene)로 간주될 수 있다. 관찰된 GOF 활동은 발암과정 중에 유전자 기능의 완전한 손실보다는 TP53 미스센스 돌연변이가 주로 나타나게 되는 강력한 선택압을 설명할 수 있다. 그럼에도 불구하고 TP53 돌연변이의 약 10% 정도 되는 작지만 상당한 비율은 야생형 기능이 손상된 잘린 p53 단백질이 발현되게 하는 넌센스(nonsense) 돌연변이다.
본 총설 논문은 p53 돌연변이의 야생형 기능 복원을 위한 전략에 초점을 맞추고 있다. 우리 는 p53 돌연변이를 표적으로 하는 분자의 개발과 관련해 지금까지 이루어진 진전에 대해 토론하고, 임상 개발에 대한 최신 동향을 살펴본다. 또한 넌센스 돌연변이를 가진 TP53의 전사를 약리적으로 유도하는 최근의 연구를 다룬다.
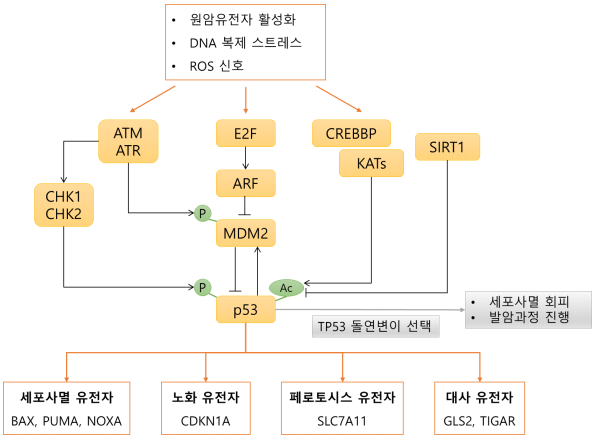
그림 1. p53 네트워크.
p53은 초기 종양 세포의 활성 원암유전자, DNA 복제 문제, ROS 등에 의해 유도된다. p53은 MDM2와 음성피드 백 구조를 이루고 있다. ATM, ATR, CHK1, CHK2에 의한 MDM2과 p53의 인산화(P)는 p53-MDM2 결합을 방해하 여 p53을 안정화시킨다. CREBBP, KAT5에 의한 p53의 아세틸레이션(Ac)은 DNA 결합을 위해 p53을 활성화시킨 다. p53 아세틸화는 SIRT1에 의해서도 조절된다. E2F, ARF는 MDM2 억제를 통해 p53을 유도한다. 스트레스 상 황에 대한 세포의 반응 경로에서 p53의 핵심적인 역할 덕분에 TP53 돌연변이에 대한 강한 선택압을 설명할 수 있다.
2. p53의 구조와 돌연변이
게놈 염기서열 분석 결과 12종류의 암 환자 중에서 42%가 돌연변이 TP53을 가지고 있는 것으로 나타났다. 그러나 TP53 변이율은 종양 유형에 따라 크게 다르다. 예를 들어, 일부 신장세포암(renal clear cell carcinoma)의 TP53 돌연변이율은 2.2%에 불과한 반면, 고도 장액성 난소암(high-grade serous ovarian cancer)의 TP53 돌연변이율은 거의 95%이다.
암의 TP53 돌연변이의 대다수는 DNA와 결합하는 핵심 도메인인 100~300 잔기(residue)에 위치한 미스센스 돌연변이다. 가장 자주 영향을 받는 다섯 잔기는 Arg273, Arg248, Arg175, Arg245, Arg282 이다. 대부분의 미스센스 TP53 돌연변이 는 p53의 DNA 결합을 방해한다. p53의 종양 억제제로서 정상적인 기능을 손상시키는 많은 TP53 변 이는 단백질의 자유 에너지를 증가시켜 그 구조를 불안정하게 만든다.
미스센스 돌연변이 p53 단백 질은 크게 DNA 접촉 돌연변이 또는 구조적 돌연변이로 분류될 수 있다. p53-R273H 돌연변이와 같 은 첫 번째 유형의 돌연변이는 DNA와 직접 접촉하는 잔기를 대체한다. 이는 반드시 p53 단백질 구 조에 심오한 영향을 미치는 것은 아니지만, 그럼에도 불구하고 단백질의 열안정성(thermostability)을 감소시킬 수 있다. 두 번째 유형의 돌연변이는 핵심 도메인의 접힘을 방해하는 아미노산 대체물을 생성한다. 예를 들어 p53-R175H와 같은 돌연변이가 생성하는 잔기는 빽빽하게 포장된 소수성 β-시트 구조에 위치하는 경우가 많다. 구조적 돌연변이는 보다 광범위한 구조적 왜곡 및 감소한 열안정 성을 특징으로 한다.
표 1. 각 tumour 타입에 따른 TP53 돌연변이 빈도와 가장 흔한 변이 종류
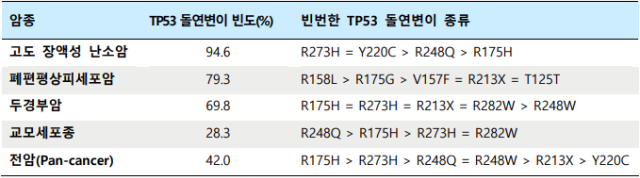
코돈(codon) 175와 273의 대체는 인간 종양에서 가장 일반적인 TP53 돌연변이에 속하지만, 종양 유형에 따라 돌연변이 패턴은 다르게 나타난다. 예를 들어 폐편평상피세포암(lung squamous cell carcinomas)은 담배 연기 내 발암물질 노출과 관련된 p53-R158L 및 p53-V157F 돌연변이와 같은 TP53 변형을 자주 수반한다. 본질적으로 모든 종양 관련 TP53 미스센스 변이는 서열상 DNA 결합에 영향을 미치지만, 각 아미노산이 대체하는 p53 구조, DNA 결합 및 파트너 단백질과의 상호작용에 따라 고유한 영향을 미칠 가능성이 있다. 따라서 돌연변이 p53 단백질은 정상 종양 억제 기능의 다 양한 손실과 GOF을 획득한 상이한(heterogeneous) 단백질군이라고 볼 수 있다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
-
다음글
- 플라스틱 분해 인공미생물
-
이전글
- 세포 배양 자동화 기술 최신 동향


 pdf_0003292.pdf
pdf_0003292.pdf