BioINwatch
(BioIN + Issue + watch) : 바이오 이슈를 빠르게 포착하여 정보 제공지난해(2019년) 미국 FDA 승인 신약, 총 48개
- 등록일2020-02-10
- 조회수7348
- 분류레드바이오 > 의약기술, 제품 > 바이오의약
-
발간일
2020-01-30
-
키워드
#미국#FDA
- 첨부파일
-
차트+
?
차트+ 도움말
BioINwatch(BioIN+Issue+Watch): 20-8
지난해(2019년) 미국 FDA 승인 신약, 총 48개
◇ 미국 FDA의 2019년 신약 허가건수는 48건으로, 역대 최다 승인건수를 기록했던 2018년 대비 18.6% 감소. 승인된 신약의 21%는 바이오신약 이며, 44%는 희귀의약품, 42%는 혁신신약(first-in-class)으로 새로운 영역에서 다양한 신약들이 허가
▸주요 출처 : FDA‘s CDER(CENTER FOR DRUG EVALUATION AND RESEARCH), Advancing Health Through Innovation : New Drug Therapy Approval 2019, 2020.1
■ 2019년 한해 동안 미국 FDA가 허가한 신약은 총 48건으로, 2018년 59건에 비해 18.6%(11건) 감소
○ 미국 FDA 의약품평가센터(CDER)의 2019년 신약 승인 건수는 총 48건으로, 2017년 46건, 2018년 59건에 이어 꾸준히 많은 신약을 허가
- 승인된 신약 중 바이오신약은 10개로 약 21%이며, 2010년~2019년 누적 승인 신약에서 바이오신약의 비중은 23.5%로 20%대 점유
※ 2019년 승인된 바이오신약 : Enhertu, Padcev, Adakveo, Reblozyl, Beovu, Polivy, Skyrizi, Evenity, Cablivi, Jeuveau
< 미국 FDA 신약 승인 현황(2000~2019) 및 신약 종류별 승인 현황(2010~2019) >
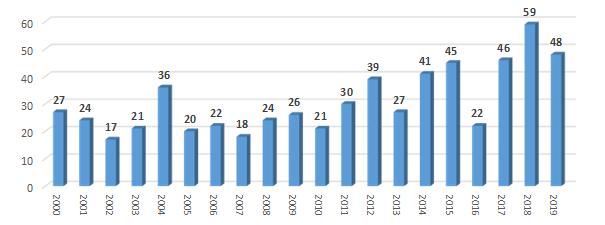
| 2010 | 2011 | 2012 | 2013 | 2014 | 2015 | 2016 | 2017 | 2018 | 2019 | 합계 |
합성신약 (NDA Approvals) | 15 | 24 | 33 | 25 | 30 | 33 | 15 | 34 | 42 | 38 | 289 |
바이오신약 (BLA Approvals) | 6 | 6 | 6 | 2 | 11 | 12 | 7 | 12 | 17 | 10 | 89 |
합계
바이오신약 비중(%) | 21 | 30 | 39 | 27 | 41 | 45 | 22 | 46 | 59 | 48 | 378 |
40.0 | 25.0 | 18.2 | 8.0 | 36.7 | 36.4 | 46.7 | 35.3 | 28.8 | 20.8 | 23.5 |
출처 : FDA(https://www.fda.gov/), Novel Drug Approvals for 2015 ~ 2019
■ 지난해 허가된 신약의 44%는 희귀의약품, 42%는 혁신신약(first-in- class)으로, 새로운 영역에서 환자를 치료하는 다양한 신약들이 허가
○ 의학적 미충족 요구를 충족시키거나 환자의 치료를 진전시키는데 도움이 되는 혁신적인 의약품을 승인
- 희귀질환, 신경 및 정신장애, 감염병, 심장・폐・순환기・내분기질환, 자가면역질환, 여・남성 특정 건강문제, 암 및 혈액질환 등에서 건강을 향상시키는 새롭고 혁신적인 치료제를 승인
※ 희귀질환(Rare Diseases) : 48건의 신규허가 중 21건이 희귀의약품 지정을 받은 신약으로, 낭포성 섬유증, 겸상적혈구질환, 시신경척수염(neuromyelitis optica spectrum disorder), 전신경화증 관련 간질성폐질환(systemic sclerosis-associated interstitial lung disease(SSc-ILD) 등의 치료제 승인
※ 심장, 폐, 순환기 및 내분비 질환(Heart, Lung, Circulatory, and Endocrine Diseases) : 트랜스티레틴 매개성 아밀로이증(transthyretin mediated amyloidosis), 정맥혈전색전증, 당뇨병 등을 치료하는 치료제 승인
※ 자가면역(Autoimmune Conditions) : 전신성 홍반성루프스(systemic lupus erythematosus), 비방사선학적 척추관절염(non-radiographic axial spondyloarthritis), 람베르트- 이튼 근무력 증후군(Lambert-Eaton myasthenic syndrome) 등의 치료제 승인
※ 여성/남성 특정 건강문제(Women’s and Men’s Specific Health Issues) : 여성의 성욕 감소장애, 산후우울증, 남성의 성선기능저하증 치료제 승인
○ 승인된 신약 48개 중 42%인 20개가 혁신신약(First-in-class; 동종계열 최초 약물)으로 승인
- 44%인 21개는 희귀질환(Rare Diseases) 치료제이며, 신속한 개발 및 승인을 촉진하기 위한 신속심사, 우선심사 등의 규제경로를 적극 활용
※ 48건 중 17건는 신속심사(Fast Track)로, 13건은 획기적 치료제(Breakthrough therapies)로 지정. 28건은 우선심사(Priority Review) 대상으로 지정되었으며, 9건은 가속승인(Accelerated Approval) 대상으로 지정
- 또한 48건 중 33건(69%)은 다른 국가에서 승인받기 전에 미국에서 최초로 승인되었으며, 43건(90%)은 최초허가신청서(first cycle)로 승인
※ First cycle approval: 추가 자료 제출 없이 최초허가 신청서만으로 승인을 획득
○ 승인된 신약의 개발사로는 노바티스가 5건으로 가장 많은 신약을 승인
- ABBVIE, DAIICHI SANKYO, GENENTECH(Roche사가 인수)은 각각 2건의 신약을 승인받음
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
지식
- BioINwatch 「국가 바이오기술 이니셔티브 법안」, 미국 상·하원 초당적 발의 2025-06-30
- BioINwatch 미국 NSCEB, 국가전략기술로서의 생명공학 육성에 관한 전략 보고서 발간 2025-06-23
- BioINwatch 미국 보건복지부에 대한 예산 삭감 및 조직 개편 계획이 담긴 예비 문서 공개 2025-06-09
- BioINpro [이슈페이퍼] 『美신흥생명공학에 관한 국가안보위원회(NSCEB)』 전략 보고서 - 미국 생명공학의 미래 설계- 2025-06-02
- BioINwatch 미국 ARPA-H가 추진하고 있는 23개 프로그램 2025-04-24
동향


 BioINwatch20-8(1.30)●지난해(2019년) 미국 FDA 승인 신약 총 4...
BioINwatch20-8(1.30)●지난해(2019년) 미국 FDA 승인 신약 총 4...
 < 미국 FDA 신약 승인 현황(2000~2019) 및 신약 종류별 승인 현황(2010~2019) >
< 미국 FDA 신약 승인 현황(2000~2019) 및 신약 종류별 승인 현황(2010~2019) >
 2019년 미국 FDA 승인 신약 리스트(48개)
2019년 미국 FDA 승인 신약 리스트(48개)