기술동향
신호전달 세포소기관으로서 미토콘드리아는 포유류 줄기세포 운명을 제어한다.
- 등록일2021-07-30
- 조회수8469
- 분류기술동향 > 플랫폼바이오 > 바이오융합기술
-
자료발간일
2021-07-29
-
출처
생물학연구정보센터(BRIC)
- 원문링크
-
키워드
#세포소기관#줄기세포#미토콘드리아
- 첨부파일
신호전달 세포소기관으로서 미토콘드리아는 포유류 줄기세포 운명을 제어한다.
◈목차
1. 서론
2. 미토콘드리아의 여러 기능
3. 줄기세포에서 미토콘드리아의 재평가
4. 미토콘드리아 활성산소는 줄기세포 운명을 조절한다.
5. TCA 회로 대사산물에 의한 줄기세포 운명의 조절
6. NAD+/ NADH 비율은 줄기세포의 운명과 기능을 조절한다.
7. 피루브산 대사는 줄기세포의 운명과 기능을 지휘한다.
8. 미토콘드리아 역동성은 줄기세포 운명을 조절한다.
9. 결론
◈요약문
최근 보고된 증거들은 미토콘드리아 대사가 줄기세포의 운명을 결정하는데 필요하다는 개념을 뒷받침한다. 역사적으로 미토콘드리아 대사는 각각 adenosine triphosphate (ATP) 및 tricarboxylic acid (TCA) 회로 대사산물의 생산과 연결되어 줄기세포 생존과 성장을 지원하는 것으로 알려져 왔다. 그러나, 이제 이러한 대표적인 역할을 넘어서 신호전달 세포소기관(signaling organelles)으로서, 미토콘드리아가 줄기세포의 운명과 기능을 조절한다는 것이 분명해졌다. 이 리뷰에서는 미토콘드리아가 활성산소(Reactive Oxygen Species, ROS) 생성, TCA 회로 대사산물 생산, NAD+/NADH의 비율 조절, 피루브산(pyruvate) 대사 및 미토콘드리아 역동성(mitochondrial dynamics)을 통해 어떻게 포유류 줄기세포의 운명과 기능을 제어하는지에 대한 핵심적이고 개념적인 발상에 중점을 둔다.
키워드: TCA cycle, pyruvate, epigenetics, ROS, acetyl-CoA, L-2-HG, mitochondrial dynamics
분야: Biochemistry, Cell_Biology, Developmental_Biology
◈본문
1. 서론
줄기세포는 줄기세포 pool을 유지하기 위해 세포 분열을 겪을 뿐만 아니라, 조직 항상성을 생성하고 유지하기 위해 전구 세포 집단으로 분화하기도 한다. 많은 성체 줄기세포(adult stem cell)들은 휴면 상태(quiescence)를 유지하다가, 다양한 세포 운명이 결정되면서 대사의 변화를 동반한다.
줄기세포는 독특한 영양소 가용성을 가진 다양한 미세환경(niche)에 존재하며, 그것은 줄기세포 대사의 변화에도 반영된다. 전통적으로 대사는 줄기세포, 전구세포 또는 분화된 세포의 다양한 대사적 수요를 지원하기 위해 줄기세포 운명의 변화와 동반되는 것으로 생각되었다. 그러나, 지난 10년간의 여러 연구들은 대사의 변화가 줄기세포의 운명을 좌우할 수 있으며, 전사 네트워크가 줄기세포의 운명을 제어하는 방법과 유사하게 기능할 수 있음을 보여주었다.
이것은 줄기세포 대사가 손상된 조직을 재생하거나, 정상적인 노화 과정의 조직을 회춘(rejuvenation)시키기 위한 목표가 될 수 있다는 인식으로 이어졌다.
본 리뷰는 줄기세포 대사에 관한 모든 문헌에 대한 철저한 검토가 아니며, 미토콘드리아 대사가 어떻게 활성산소(Reactive Oxygen Species, ROS) 생산, TCA (Tricarboxylic acid) 회로 대사산물 생성, 감소된 nicotinamide adenine dinucleotide (NAD+/NADH)에 대한 산화율, 피루브산(pyruvate) 대사와 관련되는지, 그리고 미토콘드리아 역동성(mitochondrial dynamics)이 어떻게 생체 내에서(in vivo) 쥐와 인간 줄기세포 운명을 좌우하고, 쥐와 인간 줄기세포의 만능성(pluripotency) 상태를 유지하는 것과 관련되는지에 대한 주요 발전을 강조하고자 한다.
2. 미토콘드리아의 여러 기능
미토콘드리아 대사는 세포 생존과 증식을 지원하고 다양한 세포 상태를 조정한다. 미토콘드리아를 ‘세포의 동력원’으로 간주하는 고전적인 기능은 산화적 인산화(oxidative phosphorylation, OXPHOS) (즉, 이화작용)에 의해 ATP (adenosine triphosphate)를 생성하는 것이다 (그림 1). 이에 상응하는 핵심 기능으로 지질 및 뉴클레오타이드(nucleotides)와 같은 거대분자를 생성하는 citrate, oxaloacetate 등의 TCA회로 대사산물을 생산함으로써, 동화작용(anabolic)을 지원하는 것이 있다 (그림 1).
산화적 TCA 순환 기능은 기능적으로 전자전달계(electron transport chain, ETC)와 연결되어 있다. 그러나, TCA 회로는 전자전달계가 손상되었을 때, 주로 aspartate 생산을 위해 pyruvate carboxylase (PC)를 사용하여 피루브산에서 oxaloacetate (OAA)를 생성하고, citrate 합성을 위해 글루타민(glutamine) 의존적 환원 카르복실화(carboxylation)를 사용하는 환원 기전에 의해 계속해서 대사산물을 생성할 수 있다.
전자전달계 복합체 III는 de novo pyrimidine 합성의 핵심 속도 제한 효소인 DHODH (dihydroorotate dehydrogenase) 활성에도 필요하다. 해당 과정(glycolysis)과 TCA회로 흐름은 동화작용의 수요를 충족시키기 위해 대사산물을 생성한다는 점을 유의하는 것이 중요하다.
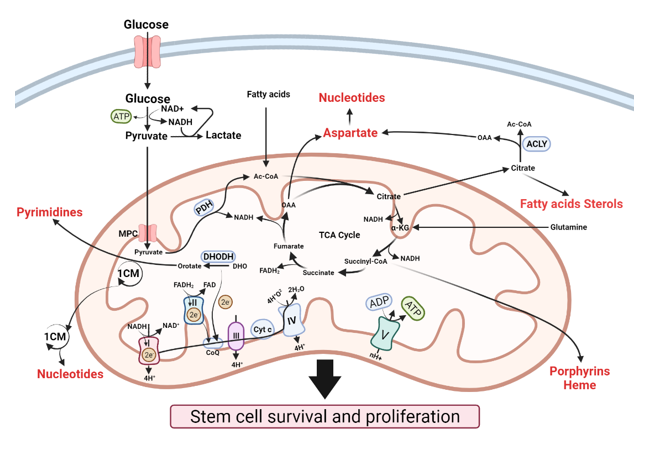
그림 1. 생체 에너지 및 생합성 소기관으로서 미토콘드리아는 줄기세포 생존 및 증식을 지원한다.
포도당 및 여러 다른 기질(예: fatty acids 및 glutamine)은 생합성 중간체 및 NADH 및 FADH2와 같은 환원 등가물을 생성하는 TCA 회로에 공급된다. 또한, 미토콘드리아 1탄소 대사(one-carbon metabolism, 1CM)는 생합성 중간체를 제공한다. 중간 기질은 지질 및 뉴클레오타이드와 같은 거대 분자의 합성에 사용되며 환원 등가물은 줄기세포 생존 및 증식을 지원하는 산화적 인산화에 의한 ATP 생성을 위한 연료를 공급한다.
(Ac-CoA, acetyl-coenzyme A, acetyl-CoA ; OAA, oxaloacetate; DHO, dihydroorotate; MPC, mitochondrial pyruvate carrier; ACLY, ATP citrate lyase; DHODH, dihydroorotate dehydrogenase; PDH, pyruvate dehydrogenase.)
지난 20년 동안의 연구를 통해 미토콘드리아에서 이질적(disparate) 신호 전달의 일부분이 세포의 운명과 기능을 제어한다는 미토콘드리아 대사의 세 번째 기능이 알려졌다 (그림 2). 표준 신호 전달 경로는 종종 미토콘드리아 ATP, acetyl-coenzyme A (acetyl-CoA) 및 활성산소를 각각 필요로 하는 인산화(phosphorylation), 아세틸화(acetylation) 및 산화(oxidation)를 포함하여 단백질 내 아미노산의 번역 후 변형에 관여한다.
미토콘드리아는 cytochrome c를 방출하여 케스페이스 의존적 세포 사멸(caspase-dependent cell death)을 시작하고 미토콘드리아 DNA (mtDNA)를 방출하여 다중 염증성 연쇄반응(multiple inflammatory cascades)을 시작할 수 있다. 또한, 미토콘드리아는 유리 칼슘(free Ca2+)의 주요 조절자 역할을 하여 다양한 Ca2+ 의존적 신호 전달 연쇄반응 및 전사 네트워크를 제어한다.
미토콘드리아 외막(outer membrane)은 미토콘드리아 항 바이러스 신호 단백질(mitochondrial antiviral signaling protein, MAVS)의존성 선천성 면역 반응 및 Bcl-2 (B-cell lymphoma 2) 의존성 세포 사멸과 같은 다양한 신호 전달 복합체의 물리적 플랫폼으로써 기능한다. 또한, 미토콘드리아 모양과 역동성은 세포의 운명과 기능을 결정하는데 중요한 원인으로 작용할 수 있다.
최근 개념은 소포체(endoplasmic reticulum) 및 리소좀(lysosomes)과 미토콘드리아 상호작용(crosstalk)이 세포 운명과 기능을 조절할 수 있다는 것이다. 이와 더불어 리소좀에 의한 미토콘드리아 품질 관리는 줄기세포 운명에 영향을 미친다. 핵심적인 부분은 미토콘드리아 기능의 변화가 줄기세포 운명에 결정적인 전사(transcription)의 변화보다 앞선다는 것이다. 따라서 미토콘드리아는 신호전달 세포소기관(signaling organelles)이며, 본 리뷰에서는 줄기세포의 운명과 기능을 제어하는 핵심 접점으로 미토콘드리아 대사의 이러한 측면을 개념적으로 강조한다.
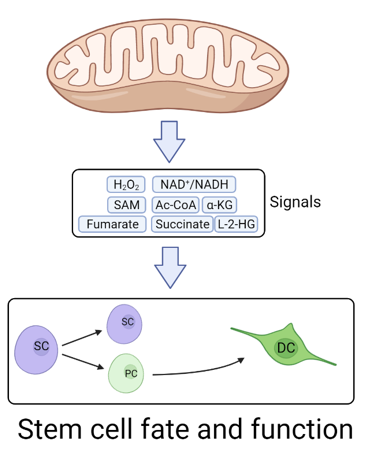
그림 2. 신호전달 세포소기관으로서 미토콘드리아는 줄기세포의 운명과 기능을 조절한다.
미토콘드리아는 줄기세포 유지, 전구 집단에 대한 운명 결정 및 다양한 세포 유형으로의 분화를 제어하기 위한 세포 신호로 작용할 수 있는 ROS 및 다양한 대사산물을 생성한다.
(SC, stem cell; PC, progenitor cell; DC, differentiated cell.)
3. 줄기세포에서 미토콘드리아의 재평가
21세기 대사 연구의 부흥은 1920년대 종양 절편이 충분한 산소가 있는 상태에서 포도당(glucose)을 흡수하고, 젖산(lactic acid)을 분비한다는 Otto Warburg의 관찰과 관련이 있다. 실제로 여러 연구에서 줄기세포가 Warburg 효과를 나타낸다고 보고했다.
더욱이 해당 과정의 전사 활성화 인자로 알려진 저산소증 유발 인자(hypoxia- inducible factors, HIFs)가 줄기세포 운명을 조절하는 것으로 입증되었다. 조혈모줄기세포(hematopoietic stem cells, HSC)에서 MitoTracker Green (MTG)과 같은 염료를 사용하여 미토콘드리아 함량을 평가하였다. 그 결과, 조혈모줄기세포에서 다능성 전구 세포(multipotent progenitors, MPPs)로 전환되는 동안 미토콘드리아 함량이 감소함을 보여주었다.
이러한 연구는 해당 과정이 줄기세포 운명을 조절하는 주된 대사 표현형이라는 단순한 발상을 이끌어 냈다. 그러나, 최근 연구에서는 조혈모줄기세포가 MTG를 적극적으로 배출하는 xenobiotic efflux pumps를 포함하고 있기 때문에 미토콘드리아 함량을 측정하기 위한 염료로써, MTG를 사용하는 것에 의문을 제기했다. 방출 펌프(efflux pumps)의 저해제인 verapamil을 추가하면 조혈모줄기세포에서 MTG 염색이 하위 전구조혈집단보다 더 많이 증가했다.
이러한 결과는 미토콘드리아 대비 핵 DNA 함량을 측정함으로써 확인되었다. 경쟁적인 이식 실험에서 verapamil 처리 후 MTG가 높은 조혈모줄기세포가 장기적인 재집단(repopulation) 활성을 나타냈다. 미토콘드리아 함량의 또 다른 측정 방법으로 cytochrome c oxidase의 소단위 VIII에 미토콘드리아 표적 신호가 융합된 형광 단백질인 mito-Dendra2를 보유한 쥐는 조혈 계통에서 다능성 전구 세포보다 조혈모줄기세포에서 더 높은 mito-Dendra2 형광 신호를 보였으며, 경쟁 이식 분석(competitive transplantation assays)에서는 높은 mito-Dendra2 형광 신호를 가진 조혈모줄기세포가 장기적인 재집단 활성을 가지고 있는 것으로 나타났다.
또한, ATP 생성을 위해 해당 과정에 의존하는 만능성 및 휴면 상태의 성체 줄기세포는 일반적으로 완전히 기능하는 미토콘드리아를 풍부하게 가지고 있다. 또한, 인간 만능줄기세포(human pluripotent stem cell, hPSC)는 분화된 세포와 유사한 산소 소비율을 나타낸다. 중요한 것은 지난 몇 년 동안 쥐를 대상으로 한 유전 연구에서 Ptpmt1 (PTEN-like mitochondrial phosphatase 1), 피루브산 또는 지방산 산화(fatty acid oxidation), 미토콘드리아 분열/ 융합(fission/ fusion)이 생체 내에서 줄기세포 운명을 조절하는데 미토콘드리아 전자전달계가 기능한다는 사실이 입증된 것이다. 따라서, 줄기세포는 해당 과정과 미토콘드리아 대사에 의해 생성된 별개의 대사산물을 통합하여 줄기세포의 운명과 기능을 조절한다.
배아 발달과 성체 조직 항상성 및 복구는 self-renewal을 겪고 다른 계통의 세포를 생성하는 줄기세포 집단에 의존한다. 줄기세포의 감소는 노화와 많은 퇴행성 질환의 특징이다. 당연히 미토콘드리아 기능 장애는 이러한 표현형과 관련이 있다. 예를 들어, mtDNA polymerase gamma (POLG) 돌연변이 쥐는 조혈 전구 세포(hematopoietic progenitor cells, HPC), 신경 줄기세포(neural stem cells, NSC) 및 장 줄기세포(intestinal stem cells, ISC)를 포함하여, 다른 줄기 및 전구 세포의 기능 장애를 초래하는 mtDNA 돌연변이를 축적한다. 종합적으로, 이러한 연구는 다양한 맥락에서 줄기세포의 운명과 기능을 제어하는데 있어 미토콘드리아의 중요성을 강조한다.
4. 미토콘드리아 활성산소는 줄기세포 운명을 조절한다.
활성산소는 산소를 함유하는 자유기(oxygen-containing free radicals) 또는 화합물을 지칭하며, 산소 분자보다 반응성이 크다. 세포 내 활성산소에는 4가지 주요 형태가 있다: superoxide radical anion (O2-), hydroxyl radical (•OH), hydrogen peroxide (H2O2) 및 lipid hydro-peroxides (LOOH). 미토콘드리아 전자전달계 복합체 I, III 및 세포질 막 결합 NADPH (reduced nicotinamide adenine dinucleotide phosphate) 산화 효소(NOX)는 O2- 생성의 주요 부위이다 (그림 3a). O2-는 생성 즉시 미토콘드리아 기질의 superoxide dismutase 2 (SOD2)와 미토콘드리아 막간 공간 및 세포질에서 superoxide dismutase 1 (SOD1)의 작용에 의해 보다 안정적인 H2O2로 환원된다.
H2O2는 단백질의 기능, 안정성 및 세포 내 위치에 중요한 특정 황 함유 아미노산(즉, cysteine과 methionine)을 직접 산화시킴으로써, 신호분자 역할을 한다. 이러한 산화는 일반적으로 항산화제의 작용에 대해 가역적이다.
Peroxiredoxins은 H2O2를 물(H2O)로 변환하는 주요 해독제이다. 또한, H2O2는 철(Fe2+)의 존재 하에, •OH를 생성할 수 있다. 다중 불포화 지방산(polyunsaturated fatty acids, PUFA)은 •OH와 반응하여 페롭토시스(ferroptosis)를 유발할 수 있는 LOOH를 생성한다. 유비퀴논(ubiquinone, Q)의 유비퀴놀(ubiquinol, QH2)로의 Glutathione peroxidase 4 (GPX4) 및 ferroptosis suppressor protein 1 (FSP1) 의존적 환원은 LOOH를 해독할 수 있다. 항산화 유전자의 발현은 forkhead box protein O (FOXO) 계열 구성원 및 nuclear factor (erythroid-derived 2)-like 2 (NRF2)를 포함한 다양한 전사인자(transcription factors)에 의해 조절되며, 활성산소가 줄기세포에 손상을 줄 수 있는 수준으로 증가하는 것을 방지한다.
포유류 만능줄기세포(pluripotent stem cells, PSC)의 미토콘드리아 활성산소 매개 조절과 관련된 일반적인 논제는 iPSC 및 배아 줄기세포가 유전체 무결성(genome integrity)을 유지하기 위해 낮은 수준의 내인성 활성산소를 가지며, 적절한 활성산소 수준은 다른 계통으로의 분화에 필요하다는 것이다.
참고로, 삼배엽(three germ layers)의 모든 세포를 생성할 수 있는 PSC는 preimplantation epiblast의 내부 세포 덩어리(inner cell mass, ICM), early post-implantation epiblast 또는 epiblast stem cells (EpiSCs)로부터 분리될 수 있다. 또한, PSC는 만능성 관련 전사인자(pluripotency-associated transcription factors)를 발현하여 체세포에서 확립될 수 있다.
PSC는 세포 배양 조건에 의존하는 primed (보다 발생학적으로 분화된 상태)와 naïve의 두 가지 다른 상태로 배양될 수 있다. Naïve 및 primed PSC는 일반적으로 각각 ICM 및 early post-implantation epiblasts의 세포와 분자 특성을 공유한다. 미토콘드리아 호흡 사슬의 억제 또는 미토콘드리아 막 전위(mitochondrial membrane potential, MMP)의 탈분극(depolarization)은 PSC 분화를 방지하지만, 만능성을 유지한다.
mtDNA의 돌연변이는 미토콘드리아 H2O2 생산을 증가시키고 iPSC 리프로그래밍 효율성과 self-renewal을 감소시킨다. 미토콘드리아 H2O2 생산을 감소시키는 mitochondria-targeted ubiquinone (MitoQ)을 처리하면 이러한 결함을 완화시킨다. 그러나 MitoQ의 추가는 wild-type iPSC 및 신경줄기세포에 독성을 유발한다. 종합적으로, 이러한 결과는 PSC의 생존력(viability)을 유지하기 위해 낮은 기저 수준의 미토콘드리아 H2O2가 필요하며 미토콘드리아 H2O2의 증가는 줄기세포능(stemness) 손실을 유발하고 분화에 필요함을 나타낸다.
미토콘드리아 활성산소는 성체 줄기세포의 휴면 상태, 활성화, 증식, 분화 및 고갈의 중요한 조절자로써 관련되어 있다. 휴면 상태, self-renewing 성체 줄기세포는 일반적으로 낮은 기저 수준의 활성산소를 유지하며, 이는 줄기세포의 운명 결정(commitment)과 증식 및 분화 중에 적당히 증가한다.
활성산소 수준이 가장 낮은 조혈모줄기세포는 self-renewal 잠재성이 가장 높다. FOXO 계열 전사인자는 다양한 항산화 유전자의 발현을 활성화하여 성체 줄기세포에서 활성산소 수준을 낮게 유지한다. FOXO3 결핍 또는 FOXO1/3/4-deficient 쥐 신경줄기세포 및 신경전구세포(neural progenitor cells, NPC)는 출생 직후 급속한 증식과 뇌 크기의 증가를 보이며, 그 후 신경줄기세포 및 신경전구세포 둘 다 세포의 수와 self-renewal 능력이 급격히 감소한다. 쥐 조혈모줄기세포 및 골격근 줄기세포(skeletal muscle stem cells, MuSC) 또는 ‘‘satellite cells’’는 self-renewal 능력 유지를 위해 FOXO3의 유사한 필요 조건(similar requirement)을 나타낸다.
산화 스트레스를 조절하는 것 외에도 FOXO는 미토콘드리아 산화 대사를 조절한다는 점에 유의하는 것이 중요하다. 새로운 통합 개념은 성체 줄기세포 self-renewal 및 정지를 위해 낮은 수준의 미토콘드리아 활성산소가 필요하고, 정상적인 줄기세포 증식 및 분화를 위해서는 미토콘드리아 H2O2 생산의 증가가 필요하다는 것이다 (그림 3).
대조적으로, 비정상적으로 높은 미토콘드리아 H2O2 수치는 줄기세포 고갈을 유발한다. 예를 들어, mitochondrial carrier homolog 2 (MTCH2)의 손실은 미토콘드리아 질량, ATP 및 활성산소 수준의 증가를 유발하고 조혈 줄기 및 전구 세포(hematopoietic stem and pro-genitor cells, HSPC)의 세포주기 진입을 촉진한다.
여러 다른 연구에 따르면, 낮은 기저 수준의 활성산소는 정원 줄기세포(spermatogonial stem cells), 신경줄기세포 및 기도 기저 줄기세포를 포함한 다양한 성체 줄기세포의 self-renewal 능력을 유지하는데 필수적이라는 것을 보여주었다. 줄기세포에서 미토콘드리아 전자전달계 생성 활성산소의 생산을 제어하는 요인이 무엇인지는 알려져 있지 않다.
한 가지 단서는 조혈모줄기세포가 조혈모줄기세포의 유지 및 기능을 위해 미토콘드리아 지방산 산화(FAO)를 필요로 한다는 관찰에서 비롯된다. FAO는 NADH 및 FADH2 (dihydroflavine-adenine dinucleotide)를 통해 전자전달계에 전자를 제공하여 조혈모줄기세포의 운명 및 기능을 위한 활성산소를 생성할 수 있다.
미토콘드리아 H2O2 수준의 중간 정도의 생리학적 증가는 조혈모줄기세포, 각질 줄기세포, 기도 기저 줄기세포, 골격근 줄기세포, 신경줄기세포 및 중간엽 줄기세포(mesenchymal stem cells, MSC)를 포함한 다양한 성체 줄기세포의 운명 결정, 증식 및 분화에 필요하다. AKT1/2 double-deficient 조혈모줄기세포에서 감소된 미토콘드리아 H2O2수준은 분화의 정지 및 결함을 증가시키며, 이는 이러한 세포에서 약리학적으로 미토콘드리아 H2O2 수준을 증가시킴으로써 완화될 수 있다.
증가된 미토콘드리아 H2O2는 주로 p38 mitogen-activated protein kinase (MAPK) 및 FOXO 전사인자 계열의 활성을 조절함으로써 쥐 조혈모줄기세포의 분화를 유도한다. 또한, 방사선이 치사수준으로 조사된 쥐(lethally irradiated mice)에 조혈모줄기세포를 이식 후, 초기 증식과 호밍(homing) 동안 미토콘드리아 H2O2 수준의 증가가 필요하며, 이는 활성산소가 골수(bone marrow) 미세환경에서 조혈모줄기세포 호밍에 필수적일 수 있음을 나타낸다.
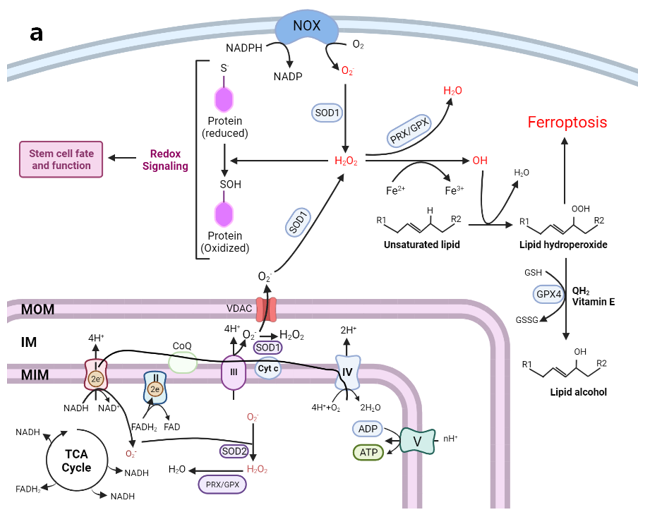
그림 3. ROS는 줄기세포의 운명과 기능을 조절한다.
a. 미토콘드리아 전자전달계와 세포질 NADPH 산화효소(NOX)는 세포에서 superoxide radical (O2_)을 생성하는 두 가지 주요 부위이다. 미토콘드리아 복합체 I은 미토콘드리아 기질에서만 O2_를 생성하는 반면, 복합체 III는 기질과 막간 공간 모두에서 O2_를 생성한다. 생성 직후, O2_는 superoxide dismutases (SOD2 in the matrix, SOD1 in the intermembrane space and cytosol)에 의해 보다 안정적이고 막투과성인 H2O2로 전환된다. 또한 미토콘드리아 O2_는 voltage-dependent anion channels (VDAC)을 통해 미토콘드리아를 빠져나갈 수 있으며 세포질에서 H2O2로 전환된다. H2O2는 줄기세포의 운명과 기능에 중요한 산화 환원 민감성 단백질의 특정 황 함유 아미노산(주로 cysteine)을 산화시켜 기능, 안정성 및 세포 내 위치를 제어할 수 있다. 과량의 H2O2는 Fe2+ 산화와 결합된 Fenton 반응을 통해 hydroxyl radical (•OH)을 생성할 수도 있다. •OH는 다중불포화지방산(PUFA)을 산화시키고 ferroptosis에 의해 세포사를 유도할 수 있는 지질 과산화수소를 생성할 수 있다. 과도한 ROS는 독성이 있으므로 세포는 ROS 항상성을 유지하기 위해 peroxiredoxins (PRX) 및 glutathione peroxidases (GPX)와 같은 다른 ROS scavengers를 가지고 있다.
(GSH, glutathione; GSSG, glutathione disulfide; QH2, ubiquinol; MOM, mitochondrial outer membrane; IM, intermembrane space; MIM, mitochondrial inner membrane.)
b. 줄기세포는 self-renewal 능력의 유지를 위해 낮은 기초 수준의 ROS가 필요하다. FOXO 단백질은 다양한 ROS scavengers의 발현을 활성화하여 낮은 ROS 수준을 유지하는데 도움이 된다. ROS의 적당한 생리학적 증가는 전구 세포에 대한 운명 결정과 다른 세포 유형으로의 분화에 필요하다. 그러나, 과도한 ROS 축적은 줄기세포 고갈로 이어진다.
(SC, stem cell; PC, progenitor cell; DC, differentiated cell.)
과도한 활성산소 축적은 줄기세포의 노화 및 세포자멸(apoptosis)뿐만 아니라, 휴면 상태의 소실(loss of quiescence) 및 줄기세포 고갈을 초래한다. 예를 들어, FOXO3 손실로 인한 활성산소 수준의 증가는 조혈모줄기세포 휴면 상태의 소실을 초래한다. 유사하게, ATM-deficient 쥐에서 증가된 활성산소 수준은 p38-MAPK 경로를 활성화하여 조혈모줄기세포 고갈을 유발하며, 이는 항산화제 또는 p38-MAPK 억제제로 장기간 치료하면 되돌릴 수 있다.
또한, 줄기세포의 미세환경은 휴면 상태와 분화 사이에서 활성산소 균형을 유지할 수 있다. 예를 들어, 골수에서 al-pha-smooth muscle actin (a-SMA)를 발현하는 단핵구(monocytes)와 대식세포(macrophage)의 드문 집단(rare population)이 정상 상태 조건(steady-state conditions)과 sublethal-irradiation 유발 스트레스 조건에서 조혈모줄기와 전구세포를 보호하는 것으로 밝혀졌다. a-SMA+ 단핵구와 대식세포는 높은 수준으로 cyclooxygenase 2 (COX2)를 발현하고, COX2 유래 prostaglandin E2 (PGE2)는 조혈모줄기세포에서 protein kinase AKT의 억제를 통해 활성산소 생성을 감소시킨다.
참고로, 낮은 활성산소 수준을 가진 조혈모줄기와 전구세포는 일반적으로 휴면 상태이며, 장기 repopulation 능력이 우수한 반면, 활성산소 수준이 높은 조혈모줄기와 전구세포는 단기 repopulation 능력이 있으며, 골수 분화에 대한 편향을 나타낸다. 또한, PGE2는 조혈모줄기세포와 전구세포의 케모카인(chemokines) CXCR4와 근처 기질 세포의 CXCL12의 발현을 증가시킨다.
CXCR4-CXCL12의 상호 작용은 조혈모줄기세포의 휴면에 필수적이다. 또 다른 연구에 따르면, 조혈모줄기세포에서 발현되는 gap junctions의 connexin 구성 요소인 connexin-43 (Cx43)은 조혈모줄기세포에서 기질 세포(stromal cells)로 전달되는 활성산소에 의한 산화 스트레스 유발 노화(oxidative-stress-induced senescence)로부터 조혈모줄기세포를 보호한다.
미세환경의 낮은 산소 장력(tension)은 조혈모줄기세포의 활성산소 수준을 낮게 유지하는데 도움이 된다. 예를 들어, perisinusoidal 골수 영역에는 투과성이 낮은 동맥 혈관이 포함되어 있어 쥐의 휴면 조혈모줄기세포에서 활성산소 수준을 낮게 유지하는데 도움이 된다. 반면에, 투과성이 더 높은 sinusoids (가는 혈관)는 활성산소 수준을 높이고, 조혈모줄기와 전구세포의 활성화, 이동 및 분화를 유도한다. 따라서, 세포는 자기 재생 능력과 기능을 보호하기 위해 줄기세포에서 비정상적인 활성산소 수준을 방지해야 한다.
LOOH는 줄기세포의 주요 독성 활성산소일 가능성이 있지만, LOOH 생성을 방지하는 유전적 개입으로 검증될 필요가 있다. 앞으로의 연구는, H2O2 또는 다른 활성산소가 줄기세포의 운명과 기능을 유지하기 위한 경로를 구체적으로 표적화하는 방법에 대해 상세히 규명할 필요가 있다.
5. TCA 회로 대사산물에 의한 줄기세포 운명의 조절
다른 세포와 마찬가지로 줄기세포의 정체성과 기능은 주로 유전자 발현 프로파일에 의해 결정된다. 진핵세포에서 유전자 전사는 전사인자와 염색질(chromatin) remodelers 및 modifiers 간의 정교한 조정을 통해 제어된다. DNA와 뚜렷한 히스톤 메틸화(methylation)는 종종 성체 줄기세포의 self-renewal능력을 촉진하는 반면, 탈메틸화(demethylation)는 줄기세포 활성화와 증식 및 분화를 초래한다.
다양한 TCA 회로 대사산물은 많은 염색질 변형 효소(chromatin-modifying enzymes)의 기질이며, 염색질 변형을 제어하여 유전자 발현을 조절할 수 있다 (그림 4). 예를 들어, 활성 염색질 변형인 히스톤 아세틸화(acetylation)는 histone acetyltrans-ferases (HAT)에 의해 촉매되며 기질로 acetyl-CoA가 필요하다. 마찬가지로, DNA와 히스톤 메틸화 및 탈메틸화는 유전자 발현 조절과도 관련이 있다.
단계적 산화를 촉매함으로서 시토신(cytosine) 메틸화 역전에 참여하는 Jumonji-C-도메인 함유 ten-eleven Translocation (TET) 효소와 히스톤 탈메틸화효소(JmjC-domain-containing histone demethylases, JHDM)는 a-ketoglutarate (a-KG) 의존성 dioxygenases이며 줄기세포 운명 및 기능의 주요 조절자이다. a-KG와 구조적으로 유사한 succinate, fumarate 및 2-hydroxyglutarate (D 및 L 동형 모두)는 TET 및 JHDM을 경쟁적으로 억제하여, 유전자 발현을 조절할 수 있다. 또한 미토콘드리아 1 탄소 대사(one-carbon metabolism, 1CM)는 히스톤과 DNA 메틸화에 필요한 S-adenosylmethionine (SAM)의 cellular pool에 기여한다.
유사하게 전사 후 유전자 발현을 조절하는 RNA N6-methyladenosine 메틸화 및 탈메틸화는 각각 SAM 및 a-KG에 의해 조절될 수 있다. 본 리뷰에서는 포유류 배아 및 성체 줄기세포 운명의 조절에서 두 TCA회로 중간체인 acetyl-CoA 및 a-KG의 역할에 초점을 맞추었다.
히스톤 아세틸화(histone acetylation)에 필요한 세포질 acetyl-CoA는 각각 citrate와 acetate를 기질로 사용하는 ATP citrate lyase (ACLY) 및 acyl-CoA synthetase short-chain family member 2 (ACSS2)에 의해 생성된다.
쥐 및 hPSC는 DNA 저메틸화(hypomethylation), 풍부한 활성 히스톤 변형 (예: H3 and H4 acetylation and H3K4 trimethylations) 및 낮은 이질염색질(heterochromatin)을 특징으로 하는 개방형 염색질 구조를 갖는다. 이 독특한 염색질 상태를 유지하기 위해 PSC는 분화된 세포에 비해 뚜렷한 대사 요구 사항을 가지고 있다.
예를 들어, 만능줄기세포는 풍부한 히스톤 아세틸화 마크와 만능성 및 self-renewal 능력을 유지하기 위해 높은 acetyl-CoA 수준을 필요로 한다. 그러나, acetyl-CoA의 공급원은 인간 만능줄기세포와 쥐 배아줄기세포(mouse embryonic stem cell, mESC) 간에 서로 다르다. mESC에서 포도당과 트레오닌(threonine) 이화작용(catabolism)은 높은 acetyl-CoA 수준에 기여한다.
참고로, 트레오닌 이화작용은 미토콘드리아에서 acetyl-CoA와 글리신(glycine)을 생성하며, mESC는 이 과정에 크게 의존한다. 반면에, hPSC에는 트레오닌 탈수소 효소(threonine dehydrogenase, TDH)가 부족하며, acetyl-CoA는 주로 포도당 유래 피루브산에서 생성된다. hPSC에서 미토콘드리아 acetyl-CoA는 cit-rate 형태로 세포질로 방출된다.
Citrate는 ACLY 효소에 의해 acetyl-CoA로 다시 전환되며 H3K9/K27 아세틸화에 필요하다. 대조적으로, hPSC의 초기 분화 동안 해당 과정에서 파생된 ace-tyl-CoA는 citrate를 통해 세포질로 방출되지 않으며, H3K9/K27 아세틸화 지표의 손실과 관련이 있다. 중요한 것은 acetyl-CoA의 전구체인 acetate를 처리하면 H3K9/K27 아세틸화 지표가 증가하고 hPSC 및 mESC의 초기 분화가 지연되므로 acetyl-CoA 수준의 감소는 아마도 히스톤 아세틸화 표시를 감소 시켜 염색질에 대한 접근성을 떨어뜨림으로써, PSC의 초기 분화를 유도한다는 것을 나타낸다.
반대로, 성체 줄기세포에서 ACLY에 의해 생성된 acetyl-CoA는 부분적으로 유전자 발현의 히스톤-아세틸화-매개 조절을 통한 분화에 필요하다. 따라서, TCA- 사이클 생성 acetyl-CoA는 mESC 및 hPSC의 줄기세포능 및 성체 줄기세포의 분화를 제어한다.
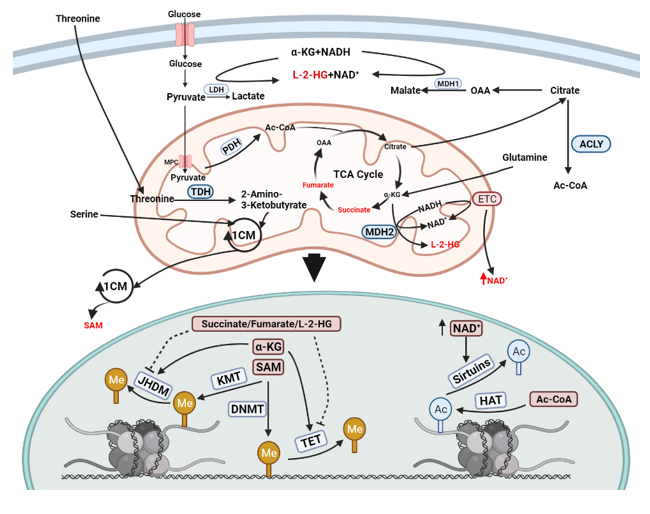
그림 4. TCA 주기 대사산물과 NAD+/NADH 비율은 염색질 변형을 통해 줄기세포의 운명과 기능을 조절한다.
Citrate-derived acetyl-CoA는 histone acetyltransferases (HAT)의 기질이다. NAD+-dependent histone deacetylases인 sirtuin은 histone acetyl marks를 제거할 수 있다. 미토콘드리아는 sirtuin의 활성을 조절하는 세포 NAD+/NADH 비율의 핵심 조절자이다. 유사하게, 미토콘드리아 1탄소 대사(1CM)는 histone & DNA methyl-transferases (각각 KMT 및 DNMT)의 기질인 S-adenosyl methionine (SAM)의 생산에 기여한다. 또한 cytosine methylation의 역전(reversal)과 관련된 Jumonji-C-domain-containing ten-eleven translocation (TET) 효소 및 histone demethylases (JHDM)는 α-KG를 필요로 하며, 이들 효소는 succinate, fumarate 및 L-2-HG에 의해 경쟁적으로 억제될 수 있다.
(OAA, oxaloacetate; MPC, mitochondrial pyruvate carrier; ACLY, ATP citrate lyase; LDH, lactate dehydrogenase; MDH1, malate dehydrogenase 1; MDH2, malate dehydrogenase 2; PDH, pyruvate dehydrogenase; TDH, threonine dehydrogenase.)
DNA와 히스톤 메틸화는 메틸 공여자인 SAM에 의해 진행된다. Naïve hPSC는 활성 염색질의 특징적인 표시인 H3K4 트리메틸화(trimethylation)를 조절하기 위해 SAM 수준을 제어한다.
그러나, SAM은 naïve hPSC에서 낮은 수준으로 유지되어, 억제성 H3K27 트리메틸화 지표도 낮은 수준으로 유지한다. SAM을 소비하는 Nicotinamide N-methyltransferase (NNMT) 효소는 hPSC에서 상향 조절되며, SAM 및 H3K27 트리메틸화 마크를 낮은 수준으로 유지하는데 필요하다. Nicotinamide N-methyltransferase (NNMT)의 knockdown은 SAM 수준과 H3K27 트리메틸화 지표를 증가시키고, HIF를 활성화하고, Wnt 신호를 억제하며, naïve 상태에서 primed 상태로 전환을 유도한다.
반면에, JHDM과 TET는 a-KG를 기질로 사용한다. a-KG는 naïve와 primed된 포유류 PSC의 운명에 다른 영향을 미친다. naïve mESC는 일반적으로 글루타민과 포도당 이화작용을 통해 높은 수준의 a-KG를 유지한다.
Naïve mESC는 높은 a-KG/succinate 비율과 DNA 및 히스톤 저메틸화를 나타내어 고도로 접근 가능한 유전체를 유지한다. 글루타민은 naïve PSC 배양에 없어서는 안되지만, 글루타민이 없는 배지에서 배양된 naïve mESC는 a-KG 수준이 감소하고, 총 트리메틸화가 증가하며 H3K9, H3K27, H3K36 및 H4K20 잔기에서 총 모노메틸화(monomethylations)가 감소한다.
중요한 것은 세포 투과성 dimethyl a-KG (DMKG)로 처리하면, mESC에서 H3K27 및 H4K20 트리메틸화 지표의 증가가 역전되므로 트리메틸화의 증가가 실제로 세포의 a-KG 수준 감소로 인해 발생한다는 것이 확인된 바 있는 것이다. 또한, naïve mESC의 자발적인 분화 동안에도 a-KG 수준이 감소하고, cell-permeable dimethyl a-KG (DMKG) 처리로 인해 유전자좌에서 DNA 및 히스톤 탈메틸화가 활성화되어, 만능성인자 발현의 억제를 늦춤으로써 분화를 지연시킬 수 있다.
또한, DMKG는 mESC 만능성 및 self-renewal 능력을 촉진하는 것으로 나타났다. naïve mESC의 세포 내 a-KG 수준은 만능성을 유지하도록 phos-phoserine aminotransferase 1 (Psat1) 효소에 의해 조절된다. Psat1의 발현은 핵심 만능성 인자 Oct4, Sox2 및 Nanog에 의해 조절된다.
Psat1은 3-phosphohydroxy-pyruvate와 glutamate의 3-phosphoserine 및 a-KG로의 전환을 결합하는 de novo serine 합성 경로의 효소이다. 대조적으로, a-KG 수준의 증가는 primed hPSC 및 쥐 EpiSC (mEpiSC)의 분화를 촉진하는 반면, 글루타민으로부터 a-KG 생산의 억제는 primed hPSC 분화를 지연시킨다. Succinate 축적, succinate dehydrogenase A (SDHA)의 약리학적 억제 또는 genetic knockdown에 의해 유도된 a-KG/succinate 비율의 감소는 primed hPSC 분화를 지연시킨다.
이 효과는 a-KG/succinate 비율을 증가시키는 DMKG 처리에 의해 완화될 수 있다. 또한, a-KG/succinate 비율의 증가 또는 감소는 TET 및 JHDM 효소를 각각 활성 또는 억제함으로써, primed PSC의 운명을 조절하는 것으로 보인다.
Self-renewing 성체 줄기세포는 종종 저산소(hypoxic) 미세환경에 상주하며 일반적으로 해당 작용을 한다. 저산소증은 미토콘드리아 전자전달계 기능을 감소 시켜, L-2-hydroxyglutarate (L-2-HG)와 succinate 축적을 증가시킨다. 결과적으로 높은 succinate/a-KG 또는 L-2-HG/a-KG 비율은 각각 TET 및 JHDM 효소의 활성을 저해하고 DNA 및 히스톤 탈메틸화를 억제함으로써, 성체 줄기세포의 self-renewal 능력을 유지하는데 도움이 될 수 있다.
대조적으로, 활성화된 성체 줄기세포에서 관찰된 바와 같이 상승된 OXPHOS는 일반적으로 a-KG 수준을 증가시키고, succinate 또는 L-2-HG 수준을 감소시켜 히스톤 및 DNA 탈메틸화를 유발함으로써, 줄기세포 활성화, 증식 및 분화를 가능하게 한다. 이 분야에서 충분히 해결되지 않은 핵심적인 질문은 이러한 대사산물(acetyl-CoA, a-KG, succinate, fumarate, and L- or D-2-HG)의 변화가 특정 유전자좌에서 특정 히스톤 아세틸화 및 메틸화 지표 및 DNA 메틸화 지표를 수정하여, 줄기세포 운명을 결정하는데 필요한 유전자 발현을 조절하는 방법이 무엇인지이다.
6. NAD+/ NADH 비율은 줄기세포의 운명과 기능을 조절한다.
TCA 사이클은 OXPHOS에 연료를 공급하기 위해 각각 전자전달계 복합체 I 및 II에 의해 NAD+ 및 FAD로 순차적으로 산화되는 환원 등가물 NADH 및 FADH2를 생성한다. 따라서, 미토콘드리아는 줄기세포를 포함한 다양한 세포 유형의 운명과 기능을 조절할 수 있는 세포 NAD+/ NADH 비율의 중요한 조절자 역할을 할 수 있다.
PSC 및 성체 줄기세포의 운명과 기능은 다른 단백질에서 다양한 acyl groups (e.g., acetyl, succinyl, malonyl, glutaryl, or long-chain acyl groups)을 제거하는 NAD+-dependent deacylases의 부류인 sirtuins에 의해 조절될 수 있다. 포유류에는 7개의 sirtuins (SIRT1-SIRT7)이 있으며 특정 세포 위치에 존재한다. SIRT1 및 SIRT2는 핵 또는 세포질에 위치하는 반면 SIRT6 및 SIRT7은 핵 단백질이다. SIRT3, SIRT4 및 SIRT5는 미토콘드리아 매트릭스에서 발견된다.
mESC와 hPSC는 모두 증가된 SIRT1 단백질 수준을 갖고, 분화 중에 감소하며, SIRT1은 naïve mESC 만능성을 유지한다. SIRT2와 SIRT6 모두 PSC의 적절한 lineage commitment에 필요하다. 그러나 현재까지, 미토콘드리아 NAD+/ NADH 비율의 변화가 줄기세포 운명을 조절하기 위해 이러한 핵 SIRT를 제어하는지 여부는 명확하지 않다.
미토콘드리아 복합체 I는 NAD+를 재생하는 능력을 가지고 있어 미토콘드리아 기질에서 단백질의 SIRT3 의존성 아세틸화를 조절한다. 조혈모줄기세포는 SIRT3가 풍부하다. 나이가 들어감에 따라 SIRT3 발현이 감소하고, 노화된 쥐의 SIRT3 손실은 조혈모줄기세포 pool을 감소시키며, 연속 적인 이식 스트레스(serial transplantation stress) 시 조혈모줄기세포 self-renewal를 손상시킨다. 또한 SIRT3 과발현은 산화 스트레스를 줄이고, 노화된 조혈모줄기세포의 기능적 결함을 완화시킨다.
유사하게, 노화된 쥐의 골격근 줄기세포는 미토콘드리아 기능 장애와 낮은 NAD+ 수준을 나타낸다. NAD+의 전구체인 nicotinamide riboside (NR)를 사용한 치료는 골격근 줄기세포의 미토콘드리아 기능 개선과 함께 노화로부터 보호하고, 골격근 줄기세포의 수를 증가 시키며, 근육 재생 능력을 향상시킨다. 또한 NR 치료는 신경줄기세포와 멜라닌 줄기세포(melanocyte stem cells)를 노화로부터 보호한다. 그러나, NR 치료의 유익한 효과는 골격근 줄기세포에서 SIRT1이 없는 쥐에서 사라져 이 과정에 SIRT1이 필요함을 나타낸다.
휴면 상태의 골격근 줄기세포의 활성화는 FAO에서 해당 과정으로의 전환을 수반하여 세포 NAD+ 수준과 SIRT1 활성을 감소시킨다. 쥐에서 SIRT1의 deacetylase domain의 결실은 조기 골격근 줄기세포 분화를 유도하고 근육 재생을 손상시킨다. 전체 NAD+ 수준은 부분적으로 NAD+ 인양 경로의 속도 제한 효소인 NAMPT (nicotinamide phosphoribosyltransferase)에 의해 제어되며, 이는 쥐 해마를 포함한 여러 조직에서 나이에 따라 감소한다.
성체 신경 줄기 및 전구 세포에서 NAMPT의 결실은 nicotinamide mononucleotide (NMN; a precursor of NAD+) 보충에 의해 완화될 수 있는 oligodendrocytes의 self-renewal, 증식 및 생성 능력을 감소시킨다. 이러한 연구는 NAD+가 정상적인 노화 과정에서 줄기세포 운명의 주요 조절자임을 강조한다.
미토콘드리아 NAD+/ NADH 비율이 줄기세포 기능에 영향을 미칠 수 있는 직접적인 방법 중 하나는 L-2-HG를 생성하는 것이다. 미토콘드리아 전자전달계 손상, 산도(acidity) 또는 저산소증은 NAD+ 재발생을 저해하여 NAD+/NADH 비율을 감소시키고 L-2-HG 수준을 증가시킨다. D-2-HG와 달리 돌연변이 isocitrate dehydrogenases (IDH1 / 2), lactate dehydrogenases (LDHA 및 LDHC), 세포질 및 미토콘드리아 malate dehydrogenases (각각 MDH1 및 MDH2)에 의해 생성된 암 대사산물은 a-KG를 무차별 기질로 사용하고 NADH를 조효소로 사용하여 L-2-HG를 생성할 수 있다.
α-KG와 구조적으로 유사하기 때문에 L-2-HG는 JHDM 및 TET를 포함한 α-KG 의존성 dioxygenases를 경쟁적으로 억제할 수 있다. a-KG는 히스톤과 DNA 메틸화를 조절하여 줄기세포의 운명과 기능을 조절할 수 있기 때문에 L-2-HG는 줄기세포 생물학의 주요 조절자일 수도 있다. 태아 쥐 조혈모줄기세포에서 미토콘드리아 전자전달계 복합체 III 소단위 Rieske iron-sulfur protein (RISP)의 손실은 NADH/ NAD+ 비율을 증가시키고, 재생 능력에 영향을 주지 않으며, MPP로의 분화를 손상시키는 수준의 L-2-HG를 유발하여, 결과적으로 배아 치사(embryonic lethality)를 초래한다.
성체 쥐 조혈모줄기세포에서 RISP의 손실은 휴면 상태를 방해하고, 심각한 범혈구감소증(pancytopenia)과 치사를 유발한다. RISP가 결핍된 조혈모줄기세포는 DNA와 히스톤 과메틸화(hypermethylation)뿐만 아니라, 히스톤 저아세틸화(hypoacetylation)를 보여준다. 흥미롭게도, 암 유전적으로 형질전환된 조혈모줄기세포에서 미토콘드리아 복합체 III 기능의 손실은 증식과 종양 진행을 감소 시켜, 정상 조혈모줄기세포와 암 유전적으로 형질전환된 조혈모줄기세포 사이의 미토콘드리아 의존적 증식 경로를 강조한다.
종합적으로, 이러한 연구는 미토콘드리아 복합체 III이 조혈모줄기세포의 증식에 없어서는 안되지만, HSC 분화 및 휴면 상태의 지배적인 조절자임을 나타낸다. 증가된 L-2-HG가 후성유전학적 변형을 통해 분화 또는 휴면 상태의 소실을 손상시키는지는 알려져 있지 않다.
...................(계속)
☞ 자세한 내용은 내용바로가기 또는 첨부파일을 이용하시기 바랍니다.
관련정보
지식
동향


 pdf_0003842.pdf
pdf_0003842.pdf