줄기세포
줄기세포의 분화 및 운명 결정 등에 대한 우리의 이해가 높아짐에 따라 생명과학의 기초연구에서부터 질병 모델링, 약물 스크리닝 및 조직공학·장기 개발까지 다양한 응용분야의 in vitro 및 in vivo에서 줄기세포를 사용할 수 있게 되었습니다.Collection
줄기세포
개념
줄기세포의 분화 및 운명 결정 등에 대한 우리의 이해가 높아짐에 따라 생명과학의 기초연구에서부터 질병 모델링, 약물 스크리닝 및 조직공학·장기 개발까지 다양한 응용분야의 in vitro 및 in vivo에서 줄기세포를 사용할 수 있게 되었다.
줄기세포를 이용한 치료는 기존의 치료법으로 치료가 불가능했던 여러 난치 질환에 근본적인 치료법을 제시할 것으로 기대되고 있으나, 아직 기술적으로 해결해야 할 과제들이 많이 남아있고 윤리적인 문제도 남아있다.
바이오인(BioIN)에서는 줄기세포에 관련된 다양한 자료들을 종합적으로 살펴볼 수 있다.
|
줄기세포 연구 중요성 및 연구개발 동향
|
|
|||||||||||||||||||||||||||||||||
|
주요국 및 국내 규제 동향, 윤리·안전성 이슈
|
|
|||||||||||||||||||||||||||||||||
|
줄기세포 관련 시장동향 및 전망
|
|
|||||||||||||||||||||||||||||||||
|
내용 출처 |
|
지식
더보기-
BioINwatch정교하고 안전한 방식으로 진화하는 줄기세포 치료
정교하고 안전한 방식으로 진화하는 줄기세포 치료 BioINwatch(BioIN+Issue+Watch): 25-5 ◇︎줄기세포 치료는 과거의 기술적·윤리적 한계를 극복하고, 대량생산, 맞춤형 치료, 안전성 개선 등 실질적 진전을 이루는 중. 특히 초기 임상시험의 성공적인 결과가 쌓이면서 줄기세포 치료가 실용적인 치료 옵션으로 부상하면서 향후 5∼10년 내 일부 줄기세포 치료가 의료 현장에 도입될 가능성이 높아지는 추세 ▸주요 출처 : Nature, Stem cells head to the clinic: treatments for cancer, diabetes and Parkinson’s disease could soon be here, 2024.12.20.; Nature News, Stem cells reverse woman’s diabetes - a world first, 2024.11.26 ◆︎ 줄기세포 치료는 과거의 한계와 실패를 극복하며 더 정교하고 안전한 방식으로
2025-01-16

-
BioINpro[줄기세포 연구동향] 줄기세포를 활용한 인공자궁 개발 동향
줄기세포를 활용한 인공자궁 개발 동향 줄기세포 연구동향 홍인선 / 가천대학교 의과대학 ◈ 목차 서론 1.저출산 문제와 인공자궁 개발의 중요성 2.자궁내막 재생에 활용 가능한 다양한 종류의 자궁 줄기세포 및 특징 2-1. 상피 유사 자궁내막 줄기세포 2-2. 자궁내막의 간질 유사 줄기세포 2-3. 혈관 주위 자궁내막 줄기세포 3.자궁줄기세포를 이용한 자궁내막의 재생 4.조직공학적 접근 5.결론 및 향후 전망 ◈본문 서론 (abstract) 저출산 문제와 난임 치료에 대한 요구가 증가함에 따라 자궁내막 재생을 목표로 한 재생 의학 기술, 특히 줄기세포를 활용한 인공 자궁 개발의 필요성이 대두되고 있음. 자궁내막은 임신과 월경 주기에서 중요한 역할을 하며, 손상된 자궁내막은 불임, 유산 및 자궁내 유착 등의 생식 문제를 유발할 수 있음. 자궁내막 줄기세포는 자가 재생 및 다양한 세포로 분화할 수 있는 능력을 갖추고 있으며, 이를 활용한 자궁내막 재생 기술은 다양한 임상
2024-10-04

-
BioINpro[줄기세포 연구동향] off-the-shelf용 저면역원성 유도만능 줄기세포주 확립
off-the-shelf용 저면역원성 유도만능 줄기세포주 확립 줄기세포 연구동향 주지현 교수/ 가톨릭대학교 유도만능 줄기세포 연구소 ◈ 목차 1.개요 가. 유도만능줄기세포(Induced Pluripotent Stem Cell iPSC) 유래 치료제 나. 유도만능줄기세포 유래 세포치료제 개발 현황 다. 면역거부반응에 따른 만능유도줄기세포를 이용한 세포치료제 개발의 한계 라. off-the-shelf용 저면역원성 유도만능줄기세포주 제작(Universal iPSC) 기술을 통한 한계 극복 2.‘CRISPR-Cas9’을 이용한 off-the-shelf용 저면역원성 유도만능 줄기세포치료제 가. ‘CRISPR-Cas9’을 이용한 임상 허가 사례 나. off-the-shelf용 저면역원성 유도만능줄기세포주(Universal iPSC)의 제작 전략 3.유전자편집 기술을 이용한 유전자 치료제의 규제학적 업데이트 가. 식품의약품 안전처의 ‘유전자편집 기술을 이용한 첨단바이오의약품 품질 평가
2024-09-24

-
BioINpro[줄기세포 연구동향] 세포 전달용 마이크로/나노로봇
세포 전달용 말이크로/나노로봇 줄기세포 연구동향 최홍수 / DGIST 로봇및기계전자공학과 교수 ◈ 목차 1.서론 2.세포 전달 또는 세포 기반 마이크로/나노로봇 가. IN Vitro 세포 전달 마이크로/나노로봇 나. 세포 기반 마이크로/나노로봇 3.마이크로/나노로봇 정밀 제어 기술 가.자기장 기반 마이크로/나노로봇 제어 나. 자기장 기반 마이크로로봇 제어를 위한 자기장 제어 시스템 다. 자기장 제어시스템을 이용한 마이크로/나노로봇 제어 기술 4.향후 과제와 연구개발 방향 5.참고문헌 ◈본문 1. 서론 마이크로/나노로봇은 인간이 하기 어렵거나 불가능한 작업을 수행하기 위해 개발되고 있는 첨단로봇으로서, 일반적으로 크기는 수 밀리미터(mm: 1×10-3m)에서 수 나노미터(nm: 1×10-9m)에 이른다. 그러나 이러한 크기로만 마이크로/나노로봇을 정의하기보다는 이러한 크기의 첨단로봇을 활용하기 위한 다양한 학문적 분야를 의미한다. 넓은 의미에서 마이크로/나노로봇은 이러한
2024-09-19

-
BioINwatch종양 형성 과정에서의 줄기세포 상태 변화를 활용한 새로운 암 치료 전략
종양 형성 과정에서의 줄기세포 상태 변화를 활용한 새로운 암 치료 전략 BioINwatch(BioIN+Issue+Watch): 24-41 ◇ 최근 ‘세포기반 차단의학(cell-based interceptive medicine)’ 개념과 연관된 연구결과가 발표. 종양 형성 과정에서 줄기세포의 상태 변화를 분석한 연구팀은 빠른 세포 주기(상위 스파이크, low-가소성)와 느린 세포 주기(하위 스파이크, high-가소성)를 나타내는 2가지 세포 상태를 알게 되었고, 이러한 세포 상태의 전환을 조작함으로써 암 치료의 새로운 전략을 개발할 수 있다는 가능성을 제시 ▸주요 출처 : Science, Stem-cell states converge in multistage cutaneous squamous cell carcinoma development, 2024.1 ■ EU의 LifeTime 이니셔티브*에서는 ‘세포기반 차단의학(cell-based interceptive medicine)’
2024-06-25

-
BioINwatch특정 줄기세포에 대한 항체로 노화된 면역체계의 회춘 가능성 제시
특정 줄기세포에 대한 항체로 노화된 면역체계의 회춘 가능성 제시 BioINwatch(BioIN+Issue+Watch): 24-30 ◇ 노화에 따른 면역력 저하로 감염에 취약해지고 만성 염증 질환이 증가하는데, 이런 면역노화의 주요 원인이 비정상적인 조혈줄기세포군의 증가 때문임을 발견. 연구팀은 마우스 모델에서 비정상적인 조혈줄기세포를 표적으로 제거하는 항체를 이용하여 노화된 면역시스템을 젊게 되돌릴 수 있다는 가능성을 확인. 향후 항체 치료로 노화된 면역체계를 젊게 유지할 수 있을지 기대 ▸주요 출처: Naure News, How to make an old immune system young again, 2024.3.27., Nature, depleting myeloid-biased haematopoietic stem cells rejuvenates aged immunity, 2024.3.27 ■노령(Aged) 쥐에서 증가된 비정상 조혈줄기세포를 표적으로 공격하는
2024-05-09

-
BioINdustry글로벌 줄기세포 시장 현황 및 전망
[BioINdustry No.189] 글로벌 줄기세포 시장 현황 및 전망 국가생명공학정책연구센터 연구원 서순원 ※ 본 보고서는 FORTUNE BUSINESS INSIGHTS에서 발간한 ‘Stem Cells Global Market Analysis, Insights and Forecast, 2023-2030 (2023.9)’ 보고서를 참고로 국가생명공학정책연구센터에서 재구성한 것임 ◈ 목차 ●요약 ●본문 1.줄기세포 정의 및 시장 분석 범위 2.줄기세포 시장 영향 요인 1.시장 성장 요인 2.시장 저해 요인 3.줄기세포 시장 분석 1.세포 유형별 분석 2.응용 분야별 3.최종 사용자별 4.지역별 분서 4.줄기세포 시장의 주요 기업 [요약] □︎글로벌 줄기세포 시장 규모는 2022년 137억 840만 달러에서 연평균 14.9%로 성장하여 2030년 399억 3,560만 달러로 확대 전망 ○세포 유형별로는 중간엽줄기세포, 응용 분야별로는 연구 부문, 최종 사용자별로는 제약 및 생명공학 기
2024-02-05

-
BioINwatch암 전이와 관련된 새로운 유형의 줄기세포 발견
암 전이와 관련된 새로운 유형의 줄기세포 발견 BioINwatch(BioIN+Issue+Watch): 23-69 ◇ 지금까지 알려지지 않았던 척추골격줄기세포(vertebral skeletal stem cells, vSSCs)가 새롭게 발견. 새로운 유형의 줄기세포는 척추 형성에 기여할 뿐 만 아니라 종양이 척추로 이동하여 성장하는 데에도 역할을 한다는 사실이 규명. vSSCs에 대한 추가 연구를 통해 암을 넘어서 척추측만증, 관절염과 같은 질환 극복에도 영향을 미칠 것으로 기대 ▸주요 출처 : Nature News, Breast cancer often spreads to the spine - newfound stem cell can explain why, 2023.9.13.; Nature, A vertebral skeletal stem cell lineage driving metastasis, 2023.9.13 ■ 유방암, 전립선암, 폐암이 척추로 전이되는 것을 촉진하는 새로
2023-10-05

발간
더보기-
 정책/기획보고서2015년도 생명공학육성시행계획, 2015년도 줄기세포연구시행계획
정책/기획보고서2015년도 생명공학육성시행계획, 2015년도 줄기세포연구시행계획
2015년도 생명공학육성시행계획 (2015년도 줄기세포연구시행계획 포함) (생명공학육성시행계획) 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부, 보건복지부, 환경부, 해양수산부, 식품의약품안전처 (줄기세포연구시행계획) 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부, 보건복지부, 식품의약품안전처 미래창조과학부 등 관계 부처는 ‘제2차 2단계 생명공학육성기본계획(Bio-Vision 2016)’의 체계적 추진과 및 산업화 촉진을 위해 각 관계부처의 이행실적 및 2015년도 세부 추진계획을 종합, 조사·분석한 ‘2015년도 생명공학육성시행계획’과 ‘줄기세포연구종합추진계획(’07~’15)’에 따른 ‘2015년도 줄기세포연구시행계획’을 수립(2015. 9.)하였습니다. 특히, 2015년 생명공학육성시행계획은 ‘제2차 2단계 생명공학육성기본계획’의 4대 전략에 따른 15대 실천과제의 효율적 이행 및 추진을 위해, 금년부터 4대 전략에 따른 세부추진과제를 설정하고
2015-11-17
-
 정책/기획보고서2014년도 생명공학육성시행계획(줄기세포연구시행계획 포함)
정책/기획보고서2014년도 생명공학육성시행계획(줄기세포연구시행계획 포함)
(생명공학육성시행계획) 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부, 보건복지부, 환경부, 해양수산부, 식품의약품안전처 (줄기세포연구시행계획) 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부, 보건복지부, 식품의약품안전처 미래창조과학부 등 관계 부처는 ‘제2차 2단계 생명공학육성기본계획(Bio-Vision 2016)’의 효과적 추진을 위해 2013년 부처/관계기관별 실적을 점검하고, 대내외적 환경변화를 반영하여 2014년도 추진계획을 수립한 ‘2014년도 생명공학육성시행계획’ 및 ‘줄기세포연구종합추진계획(’07~’15)’에 따른 ‘2014년도 줄기세포연구시행계획’을 수립(2014. 4.)하였습니다.
2014-07-04
-
 연구 보고서줄기세포 연구 및 활용기술
연구 보고서줄기세포 연구 및 활용기술
1. 줄기세포 연구 개요 가. 줄기세포란? 1) 줄기세포 정의 및 종류 □ 줄기세포(Stem cell)란 조직분화 과정에서 볼 수 있는 ‘미분화 세포’로, 인체를 구성하는 다양한 조직으로 분화 가능한 세포를 의미함 ○ 줄기세포는 분화능력(Differentiation), 자가복제능력(Self-Renewal), 호밍효과(Homing Effect) 등의 고유한 특성을 지님 - 줄기세포는 이론적으로 모든 종류의 기능세포로 분화 가능하며(분화능) 스스로 자기와 동일한 형태와 능력을 가진 세포를 만들어낼 수 있고 (자가복제능력) 정맥 내 투여 시 손상된 부위를 스스로 찾아가는 능력 (호밍 효과)을 가짐 ◆ 줄기세포 분화 기전을 이해하고 이러한 특성을 활용한다면, 손상된 각종 장기 기능의 근본적인 재생(regeneration)이 가능하며 난치병 치료에 대한 새로운 가능성을 모색할 수 있음 ○줄기세포는 분화 가능성을 기준으로 210여개의 모든 인체세포로 분화 가능한 ‘만능성(전분화능) 줄기세
2013-10-30
-
 정책/기획보고서2013년도 줄기세포연구시행계획
정책/기획보고서2013년도 줄기세포연구시행계획
Ⅰ 개 요 1. 계획수립의 근거 및 경위 □ 근 거 ◈ 舊과학기술부 주관으로 범정부 차원의「줄기세포연구 종합추진계획」수립 (생명공학종합정책심의회, ʼ06. 5. 29) - 관계부처는 종합추진계획에 따라 줄기세포연구의 연차별 시행계획을 수립하고 이를 시행 ※ 관계부처 : 미래창조과학부, 교육부, 농림축산식품부, 산업통상자원부, 보건복지부, 식품의약품안전처 □ 추진 경위 ○ 2006. 5월 줄기세포연구 종합추진계획(‘07~’15) 수립 - 2007. 3월 2007년도 줄기세포연구 시행계획 수립 - 2008. 6월 2008년도 줄기세포연구 시행계획 수립 - 2009. 7월 2009년도 줄기세포연구 시행계획 수립 - 2010. 6월 2010년도 줄기세포연구 시행계획 수립 - 2011. 6월 2011년도 줄기세포연구 시행계획 수립 - 2012. 5월 2012년도 줄기세포연구 시행계획 수립 - 2013. 6월 2013년도 줄기세포연구 시행계획 수립 ○ 2009. 7월 줄기세포연구 활성화 방
2013-08-08
-
 정책/기획보고서2012년 줄기세포연구시행계획
정책/기획보고서2012년 줄기세포연구시행계획
[계획수립의 근거 및 경위] ● 근거 舊과학기술부 주관으로 범정부 차원의 「줄기세포연구 종합추진계획」수립 (생명공학종합정책심의회, '06.5.29) -관계부처는 종합추진계획에 따라 줄기세포연구의 연차별 시행계획을 수립하고 이를 시행 ※ 관계부처 : 교육과학기술부, 농림수산식품부, 지식경제부, 보건복지부 ● 추진 경위 ○ 2006. 1월 범부처 종합계획 수립 계획 발표(국정현안조정회의) - 2006. 2~5월 종합추진계획 수립을 위한 기획연구 추진 ○ 2006. 5월 줄기세포연구 종합추진계획(‘07~’15) 수립 - 2007. 3월 2007년도 줄기세포연구 시행계획 수립 - 2008. 6월 2008년도 줄기세포연구 시행계획 수립 - 2009. 7월 2009년도 줄기세포연구 시행계획 수립 - 2010. 6월 2010년도 줄기세포연구 시행계획 수립 - 2011. 6월 2011년도 줄기세포연구 시행계획 수립 - 2012
2012-06-29
-
 정책/기획보고서2011년 줄기세포연구시행계획
정책/기획보고서2011년 줄기세포연구시행계획
2011년 줄기세포연구시행계획 교육과학기술부 등 4개 부처는 “줄기세포연구 종합추진계획(’06.5)"의 효율적 추진과 향후 줄기세포 연구분야 선진국 도약을 위해 연구개발, 인프라, 인력양성 등 분야별 2011년 계획을 마련하여 “2011년도 줄기세포연구시행계획”을 수립(2011.6) 하였습니다. 관심있는 분들의 많은 활용을 부탁드립니다.
2011-08-11
-
 정책/기획보고서2010년도 줄기세포연구시행계획
정책/기획보고서2010년도 줄기세포연구시행계획
1. 계획수립의 근거 및 경위 근 거 ◈ 과학기술부 주관으로 정부차원의 「줄기세포연구 종합추진계획」수립(생명공학종합정책심의회, ‘06. 5. 29) - 관계부처는 종합추진계획에 따라 줄기세포연구의 연차별 시행계획을 수립하고 이를 시행 ※ 관계부처 : 교육과학기술부, 농림수산식품부, 지식경제부, 보건복지부 추진 경위 ● 2006. 1월 범부처적 종합계획 수립 계획 발표 (국정현안조정회의) ‑ 2006. 2~5월 종합추진계획 수립을 위한 기획연구 추진 ● 2006. 5월 줄기세포연구 종합추진계획(ʼ07〜ʼ15) 수립 ‑ 2007. 3월 2007년도 줄기세포연구 시행계획 수립 ‑ 2008. 5월 2008년도 줄기세포연구 시행계획 수립 ‑ 2009. 5월 2009년도 줄기세포연구 시행계획 수립 ● 2009. 7월 줄기세포 연구 활성화 방안 수립 ‑ 2010. 5월 2010년도 줄기세포연구 시행계획 수립 2. 줄기세포연구 종합추진계획(ʼ06〜ʼ15) 요약 종합추진계획 중점
2010-08-24
-
 정책/기획보고서2009년도 줄기세포연구시행계획
정책/기획보고서2009년도 줄기세포연구시행계획
Ⅰ. 개 요 1. 계획수립의 근거 및 경위 □ 근 거 ◈ 과학기술부 주관으로 정부차원의 「줄기세포연구 종합추진계획」수립(생명공학종합정책심의회, ’06. 5. 29) - 관계부처는 종합추진계획에 따라 줄기세포연구의 연차별 시행계획을 수립하고 이를 시행 ※ 관계부처 : 교육과학기술부, 농림수산식품부, 지식경제부, 보건복지가족부 □ 추진 경위 ○ 2006. 1월 범부처적 종합계획 수립 계획 발표 (국정현안조정회의) - 2006. 2~5월 종합추진계획 수립을 위한 기획연구 추진 ○ 2006. 5월 줄기세포연구 종합추진계획(’06~’15) 수립 - 2007. 3월 2007년도 줄기세포연구 시행계획 수립 - 2008. 5월 2008년도 줄기세포연구 시행계획 수립 - 2009. 5월 2009년도 줄기세포연구 시행계획 수립 2. 줄기세포연구 종합추진계획(’06~’15) 개요 ○ 종합추진계획 중점추진 방향 - 체계적이고
2009-09-23
동향
더보기-
기술동향
노벨상 수상 이후, 유도만능줄기세포(iPS cell)의 임상적 응용2024.08.05
BRIC
-
기술동향
고순도 장 줄기세포 대량 배양 기술 개발2024.07.22
한국경제
-
기술동향
[NRF R&D Brief 2024-25호] 줄기세포의 근육분화를 통한 배양육 연구2024.07.12
한국연구재단
-
기술동향
인간배아줄기세포의 최근 연구동향 및 전망2024.01.03
BRIC
-
기술동향
중증 천식 환자에서의 자가 골수 줄기세포 치료술2023.09.13
NECA 신의료기술평가사업본부
-
기술동향
동물 실험 대체법으로서 인간 줄기세포를 이용한 약물 개발 현황 및 전망2022.06.29
BRIC
-
제도동향
줄기세포 유래 세포외소포치료제 품질, 비임상 평가정보집2022.03.30
식품의약품안전평가원
-
기술동향
[BIO ECONOMY REPORT] 줄기세포 유래 세포외소포를 활용한 뇌졸중치료제 개발2022.03.23
한국바이오협회
-
기술동향
줄기세포 유래 세포외소포 치료제 연구개발 및 규제동향2021.12.29
식품의약품안전평가원
-
정책동향
줄기세포 및 오가노이드_기초연구본부 선정 R&D 이슈 연구동향2021.11.22
한국연구재단
-
기술동향
신호전달 세포소기관으로서 미토콘드리아는 포유류 줄기세포 운명을 제어한다.2021.07.30
생물학연구정보센터(BRIC)
-
기술동향
-
기술동향
근육 줄기세포 지지 그룹: 근육 재생 과정 중 조직적인 세포 반응2020.08.21
생물학연구정보센터(BRIC)
-
기술동향
임상적용을 위한 생물공학적 기술을 이용한 줄기세포 배양법2020.08.03
생물학연구정보센터(BRIC)
-
기술동향
줄기세포 연구의 발전과 치료 개발2020.01.29
생물학연구정보센터(BRIC)
-
기술동향
메신저 RNA에 m6A를 쓰고, 지우고, 읽기를 통한 교모세포종 줄기세포에서의 유전자 발현 조절 연구 동향2019.12.02
생물학연구정보센터(BRIC)
-
기술동향
줄기세포 배양 관련 배양액, 성장인자, 소재 등의 국산 제품 개발 동향2019.07.10
생물학연구정보센터(BRIC)
-
기술동향
인공 난소 개발에 있어서 줄기세포의 활용2018.10.15
생물학연구정보센터(BRIC)
-
기술동향
KISTEP 기술동향브리프 줄기세포 (2018-07)2018.06.11
한국과학기술기획평가원(KISTEP)
-
기술동향
줄기세포의 역동적 상태: 설치류와 인간에서의 naive, primed 다능성 비교2018.01.09
생물학연구정보센터(BRIC)
차트+
더보기뉴스
더보기-
R&D
日 줄기세포 20년 투자, 결실 임박했나2025.04.18
조선비즈
-
R&D
파킨슨병 줄기세포 치료 잇따라 성공…안전·효능 확인2025.04.17
조선비즈
-
R&D
미국에서 세계 첫 정자 생성 줄기세포 치료법 임상시험, 남성 불임 치료 목표2025.04.09
조선비즈
-
R&D
유도만능줄기세포로 만든 3D심장, 세계 최초로 전시2025.04.08
동아사이언스
-
R&D
기증 태아서 '망막 줄기세포' 발견…실명 치료길 열리나2025.03.31
동아사이언스
-
R&D
日 연구진, 유도만능줄기세포로 마비환자 스스로 서게 해2025.03.26
동아사이언스
-
R&D
돌이킬 수 없는 '각막 손상 실명' 복구하는 줄기세포 치료법2025.03.06
동아사이언스
-
R&D
줄기세포로 기억력 향상…혈관성 치매 치료 단서 발견2025.02.27
동아사이언스
-
R&D
주형환 "치매 등 노인성 질환 줄기세포 치료 가능토록 규제 개선"2025.02.27
뉴스1
-
R&D
질병청, 지난해 연구용 줄기세포 133건 제공…전년比 2배 증가2025.02.21
연합뉴스
-
R&D
이젠 우리나라에서도··· '줄기세포 치료' 등 재생의료 받을 길 열린다2025.01.10
서울경제
-
R&D
소의 '메탄 트림' 줄이고… 줄기세포로 당뇨도 고친다2025.01.09
조선일보
-
R&D
줄기세포 조절 시스템, 수학적 알고리즘으로 규명2024.12.26
이데일리
-
R&D
인간 유래 줄기세포로 소뇌실조증 치료 돌파구 열려2024.12.23
메디포뉴스
-
R&D
KAIST-생명연, 세계 첫 완전 무이종 인간 장 줄기세포 대량 배양 성공…"기술이전 가능"2024.12.12
뉴스1코리아
-
R&D
서울대-한양대, 뇌경색 후유증 줄기세포 치료제 첫 개발2024.12.11
지디넷코리아
-
R&D
"100세 이상 산 사람은 특별하다"...줄기세포로 장수 비결 찾는다2024.12.02
동아사이언스
-
R&D
시술 수준인데 한국선 안된대요…줄기세포 치료 대못규제에 수천억씩 日에 퍼줘2024.11.26
매일경제
-
R&D
첨단재생의료심위, 폐섬유증·직장염 환자 줄기세포 치료 연구 ‘승인’2024.11.25
메디포뉴스
-
R&D
줄기세포 치료에 생기는 독성 억제하는 '나노 입자' 개발2024.11.19
동아사이언스
부처보도자료
더보기-
국가줄기세포은행, 질환자 유래 줄기세포 분양으로 희귀·난치 질환 맞춤형 치료법 개발 활용 기대
질병관리청
2025-02-20
-
국립줄기세포재생센터에서 공급한 줄기치료제, 처음으로 임상시험 승인
질병관리청
2024-10-02
-
국립줄기세포재생센터 제조시설 활용절차는 어떻게 되나요?
질병관리청
2024-01-23
-
줄기세포 기술 특허출원, 한국 성장률 2위
특허청
2023-06-05
-
줄기세포, 유전자치료 등 첨단재생의료 치료 기반 마련하다!
보건복지부
2020-11-19
-
줄기세포, 유전자치료 등 첨단재생의료 치료 기반 마련하다!
보건복지부
2020-11-19
-
줄기세포, 유전자치료 등 첨단재생의료 치료 기반 마련하다!
보건복지부
2020-11-19
-
황우석 박사 배아줄기세포주 등록
보건복지부
2016-11-15
-
줄기세포 연구에서 실용화까지 지원하는 국립줄기세포재생센터 문 연다
보건복지부
2016-10-19
-
2015「실용화형 융합연구단」선정, ‘3D 프린팅’, ‘스마트팜’, ‘줄기세포’ 분야
미래창조과학부
2015-09-16
-
말 ‘줄기세포’ 치료로 경주마 치료 성적도 올리고, 동물줄기세포 치료 실용화에 박차
농림축산식품부
2015-07-24
-
식약처, 국내·외‘줄기세포치료제 개발 및 규제동향 2014’발간
식품의약품안전처
2015-04-07
-
줄기세포치료제 개발 및 규제동향 2013
식품의약품안전처
2014-03-28
-
국가 줄기세포 관리 분양 체계 구축
보건복지부
2014-03-04
-
국가 줄기세포 관리 분양 체계 구축
보건복지부
2014-03-04
-
식약처,‘차세대 줄기세포기반제제 평가 연구 사업단’운영
식품의약품안전처
2014-02-28
-
식약처,‘차세대 줄기세포기반제제 평가 연구 사업단’운영
식품의약품안전처
2014-02-28
-
줄기세포치료제 최신 연구동향 한 눈에 조망
식품의약품안전처
2012-08-29
-
줄기세포 R&D 투자 재점화
교육과학기술부
2010-07-20
-
새해부터 줄기세포주 등록제 시행
보건복지부
2010-01-06
성과
더보기-
오가노이드에서 고순도 줄기세포를 대량 배양하는 기술 개발
2024-03-07
-
영양상태가 줄기세포의 효율을 좌우한다
2012-05-18
-
기존 줄기세포의 한계를 극복한 새로운 세포치료 성공
2012-03-21
-
체세포로부터 신경줄기세포 형성을 통한 새로운 역분화 유도만능줄기세포 제조기술 개발
2011-12-16
-
국내연구진 성체줄기세포의 성장과 분화 조절기전 규명
2011-11-10
-
세계 표준화 줄기세포 분화기술, 상용화된다
2011-11-08
-
물리적 환경 조절만으로도 배아줄기세포의 대량 배양이 가능한 배양 플랫폼 개발
2011-11-01
-
줄기세포 증식․분화 효율 높이는 신개념 세포배양 기판 대량생산기술 개발
2011-10-11
-
환자유래 역분화 줄기세포로 부신백질이영양증의 원인확인 및 신약개발의 플랫폼 제공
2011-07-01
-
역분화 줄기세포를 이용 파킨슨병 치료 가능성 높였다
2011-05-20
-
배아줄기세포와 역분화줄기세포에서 직접 기능성 혈관전구세포로 분화 성공
2010-12-27
-
지방 흡인술로 버려지는 지방 줄기세포를 이용한 골격 재생기술 개발
2010-10-22
-
국내 배아줄기세포 분화 방법, 세계 줄기세포 표준화 프로토콜로 채택
2010-10-21
-
척수 손상 후 발생하는 만성적 신경병증 통증,줄기세포를 이용한 치료가능성 발견
2010-10-08
-
국내서 개발된 배아줄기세포 한국인의 최대 25%에게 이식가능
2010-08-03
-
새로운 혈액줄기세포 공급원으로 “지방조직” 이용가능성 규명
2010-02-05
-
줄기세포 분화 및 역분화의 새로운 기작 발견
2010-01-25
-
사람 지방줄기세포를 이용한 혈관세포 분화기술개발
2008-08-07
-
뇌종양 줄기세포 발생기전 규명
2008-08-01
-
인간 배아줄기세포로부터 세계 최고 수율의 도파민 신경세포 대량 분화 성공
2008-02-26
연계정보BICS는 바이오 R&D에서 산업화까지 다양한 정보 자료를 수집하여
이용자들이 쉽게 접근하고 활용할 수 있는 플랫폼입니다.
더보기
-
Bio지표글로벌 줄기세포 시장 현황 및 전망(2022~2030)
○ 글로벌 줄기세포 시장 규모는 2022년 137억 840만 달러에서 연평균 14.9%로 성장하여 2030년 399억 3,560만 달러로 확대 전망
2024-11-12
-
Bio지표아시아/태평양 국가별 줄기세포 시장 현황 및 전망(2022~2030)
○ 한국은 아시아/태평양 시장의 12.5%를 차지하며 중국(35.5%), 일본(21.5%)에 이어 시장을 점유 - 시장 규모는 2022년 3억 8,810만 달러에서 연평균 17.5%로 성장하여 2030년 13억 3,910만 달러에 이를 것으로 전망
2024-11-12
-
Bio지표지역별 줄기세포 시장 현황 및 전망(2022~2030)
○ 북미(전체 시장의 53%), 아시아/태평양(23%), 유럽(18%) 순으로 시장을 점유하고 있으며, 아시아/태평양 지역의 연평균 성장률은 16.8%로 가장 높은 성장세 전망
2024-11-12
-
Bio지표최종 사용자별 글로벌 줄기세포 시장 현황 및 전망(2022~2030)
○ 제약 및 생명공학 기업(전체 시장의 35.8%), 학술 및 연구 기관(30.4%), 병원(21.2%), 기타(12.6%) 순으로 시장을 점유
2024-11-12
-
Bio지표응용 분야별 글로벌 줄기세포 시장 현황 및 전망(2022~2030)
○ 연구 부문은 전체 시장의 65.6%, 임상 부문은 34.4%를 차지하며 시장을 점유
2024-11-12
-
Bio지표세포 유형별 글로벌 줄기세포 시장 현황 및 전망(2022~2030)
○ 중간엽줄기세포(전체 시장의 36.1%), 유도만능줄기세포(28.8%), 성체줄기세포(22.4%) 배아줄기세포(12.7%) 순으로 시장을 점유
2024-11-12
연계정보
-
연구보고서
더보기
-
ntis줄기세포 유래 치아형성 세포원 확보 및 분화 고도화 기술 개발
닫기
연계정보(NTIS)
연구보고서줄기세포 유래 치아형성 세포원 확보 및 분화 고도화 기술 개발/Development of technique for generation of stem cell-derived tooth-forming cells and further differentiation
사업 : 2021 과학기술정보통신부 바이오.의료기술개발(R&D)과제 : 1711128097 경북대학 줄기세포 유래 치아형성 세포원 확보 및 분화 고도화 기술 개발등록번호,발행년월,발행기관명, 발행국가/사용언어,키워드 등록번호 발행년월 202205 발행기관명 경북대학교 발행국가 대한민국 초록 연구개발 목표치아형성 세포원 확보 및 배양 기술 플랫폼 확립 다양한 치계줄기세포 및 배아줄기세포의 고도분화 유도를 통한 치아형성 세포원 확보 치아줄기세포의 조직형성 기술 확립을 위한 치아 오가노이드 제작 및 배양기술 확립 치아 오가노이드 응용기술 개발 및 차세대 치아 재생치료 기반 기술 확립 연구개발 내용1단계치아줄기세포 생산 및 치아 오가노이드 제작 다양한 치계줄기세포의 확보 및 배양기술 최적화를 통한 치아형성 세포원 확보 다양한 치아형성 줄기세포의 특성 및 분화양상 비교 치계줄기세포의 분화기전 조절을 통한 고도 분화 유도 기술 확립 치배 유래 치아 오가노이드 제작 및 치아형성 유도 기술 개발 배아줄기세포의 치아형성 세포 분화 기술 개발 SOX10 발현 신경능선세포의 치수 및 치주인대줄기세포 분화 유도 배아줄기세포 유래 치수 및 치주인대줄기세포 복합체를 이용한 치아 오가노이드 제작 및 치아형성 세포원 추출 기술 개발 배아줄기세포 및 오가노이드 유래 치아형성 세포원 공급2단계치아 오가노이드 유효성 검증 동물 모델을 이용한 치아 오가노이드 생착력 평가 생체 내 치아 오가노이드 통합성 및 기능개선점 분석 치아 오가노이드의 구획별 고도분화 기술 개발 및 기능성 강화 치아 오가노이드의 안정성 검증 및 유효성 최적화 활용계획 및 기대효과 줄기세포 유래 치아형성세포 생산 및 바이오치아 제작을 위한 치계 세포원 공급 치아 오가노이드 생체 이식을 통한 치아 및 치주조직 재생 기법 개발 및 차세대 재생의학 기반 확립 치아 오가노이드의 신약 개발 플랫폼 활용 및 치아주위조직 재생의 실용화 토대 확립 첨단 치계줄기세포 제품의 개발 및 수출을 통한 차세대 바이오 성장 동력 개발출처 요약문 2p -
ntis손상된 자궁의 상처 회복에 관여하는 인자 및 월경혈 유래 줄기세포의 효능 분석
닫기
연계정보(NTIS)
연구보고서손상된 자궁의 상처 회복에 관여하는 인자 및 월경혈 유래 줄기세포의 효능 분석/Evaluation of healing process and the Effect of Adipose-derived Stem Cells(ADSC) on Injured Uterus
사업 : 2022 과학기술정보통신부 개인기초연구(과기정통부)과제 : 1711166667 가톨릭대학교(성의교정) 손상된 자궁의 상처회복에 관여하는 인자 및 지방 유래 줄기세포의 효능분석등록번호,발행년월,발행기관명, 발행국가/사용언어,키워드 등록번호 발행년월 202403 발행기관명 가톨릭대학교 발행국가 대한민국 초록 연구개요 손상된 자궁근층의 회복에 영향을 미치는 인자를 파악하고 줄기세포연구를 통해 손상된 자궁의 재건을 촉진할 수 있는 방법을 찾아서 자궁근종 및 자궁선근증 수술로 인한 난임 극복을 위한 기술 개발 연구 목표대비 연구결과손상된 자궁 회복에 있어 지방유래줄기세포의 긍정적인 효과를 기대하여 연구를 진행함 Rat 의 자궁 손상 후 시간경과에 따라 세포 재생에 다른 결과가 나타날 것으로 예상하였으며 실험군과 대조군의 차이가 명확히 보이는 회복시기를 결정하기 위하여 자궁 손상 후3일 5일 7일째의 rat을 구분하여 uterus 조직을 얻어 슬라이드 제작기본 HE 염색 및 RFP Sirus red MT IHC 의 염색법을 통해 대조군과의 차이를 확인하였을 때 손상부위 회복시 실험군에서 구조적으로 정상 자궁에 가깝에 회복되는 것을 확인하였음기대결과와 부합되는 결과를 확인하였으며 세포재생 관련 인자들을 파악하기 위한 후속연구를 계획 중에 있음 연구개발성과의 활용 계획 및 기대효과연구개발결과의 중요성동물실험을 통해 비교적 획득하기 쉬운 지방유래줄기세포를 이용하여 손상된 자궁의 회복력을 보는 실험으로 본 연구 결과에서는 줄기세포의 주입으로 자궁의 구조적 변형을 최소화할 수 있는 가능성을 확인하였음본 연구를 바탕으로 회복에 관여하는 사이토카인 등을 좀 더 연구한다면 이를 기반으로 자궁선근증이나 근종으로 수술하는 여성들에게 자궁을 보존하면서 가임력을 최대화시킬 수 있는 기초실험연구가 될 것이라고 확신함출처 연구결과 요약문 2p -
ntis난치성 류마티스관절염 특이 면역조절 기능성 줄기세포치료제 개발 및 최적 공여유전자 마커 발굴
닫기
연계정보(NTIS)
연구보고서난치성 류마티스관절염 특이 면역조절 기능성 줄기세포치료제 개발 및 최적 공여유전자 마커 발굴/Development of rheumatoid arthritis-specific immune modulatory functional stem cell therapy and the optimal biomarker discovery for donor selection
사업 : 2022 과학기술정보통신부 바이오의료기술개발과제 : 1711158017 가톨릭대학교(성의교정) 난치성 류마티스관절염 특이 면역조절 기능성 줄기세포치료제 개발 및 최적 공여유전자 마커 발굴등록번호,발행년월,발행기관명, 발행국가/사용언어,키워드 등록번호 발행년월 202306 발행기관명 가톨릭대학교 발행국가 대한민국 초록 연구개발 목표난치성 류마티스관절염 치료의 한계를 극복하기 위하여 새로운 성체 줄기세포의 공급원으로서 사람 코 유래 면역조절 기능성 줄기세포 human nasal turbinatederived stem cells hNTSCs를 이용해 생물정보학 기반 류마티스관절염 치료에 최적화된 줄기세포 치료제를 개발하고 임상시험용 세포치료제 GMP 생산 공정 표준화 및 GLP 인증기관 비임상시험을 통한 안전성을 확보하여 난치성 류마티스관절염 특이 면역 기능성 줄기세포치료제 IND 신청을 목표함 연구개발 내용1단계1 류마티스관절염 전임상모델에서 hNTSCs 치료효과 및 생물학적 안전성 규명 고순도 hNTSCs 분리 및 대량생산 기술확립 전임상모델에서 hNTSCs 효과 및 약리작용 in vivo modeofaction 규명 hNTSCs 체내 동태 in vivo trafficking 및 안전성독성 조사 전임상 연구를 통해 치료에 유효한 면역조절 기능성 hNTSCs 도출2 생물정보학 기반 류마티스관절염 치료용 줄기세포치료제 생산 인프라 구축 차세대 염기서열분석NGS을 적용하여 치료효능이 우수한 줄기세포치료제와 비우수 세포 간에 공통적으로 발현 차이를 보이는 유전자 발굴 우수치료 특이 유전자마커의 검증 및 우수치료제 예측 유전자검사법 개발 류마티스관절염 치료에 유효한 hNTSCs 확보 및 대량생산 기술 최적화2단계3 GMP 생산을 통한 임상시험용 hNTSCs 생산공정 수립 및 GLP 비임상 안전성 평가 GMP 수준에서 임상 연구를 위한 류마티스관절염 특이 면역조절 기능성 hNTSCs 생산공정 수립 GMP 수준 임상시험용 줄기세포치료제 전임상 유효성 평가 기관 GMP 시설에서 임상시험용 줄기세포치료제 생산 및 세포은행 확보 GLP 기관 비임상시험효력 분포 독성시험 완료 종양원성 시험 진행4 임상시험용 류마티스관절염 줄기세포치료제 GMP 생산공정 기술 표준화 및 임상시험계획서IND 신청 질환동물모델에서 임상시험용 줄기세포치료제의 생물학적 활성 검증 임상시험용 줄기세포치료제 GMP 생산 공정기술 최적화 표준화 및 생산 공정서 SOP 수립 임상시험 준비를 위한 CRO 임상시험 수탁기관 선정 및 임상개발계획 수립 IND 신청 활용계획 및 기대효과응용분야 및 활용범위 포함 고품질 고효율의 줄기세포 치료제 생산에 대한 충분한 원천기술을 기반으로 류마티스관절염 줄기세포치료제에서 우수한 치료효능의 줄기세포치료제를 선별할 수 있는 유전자마커를 발굴하고 이를 바탕으로 치료효과를 혁신적으로 높일 수 있는 최적의 줄기세포치료제를 생산함으로서 줄기세포치료가 보편적으로 활용될 수 있는 대안을 제시할 수 있음출처 요약문 3p -
ntis치주인대줄기세포 치근 국소부 밀집화 및 분화모델을 이용한 치주조직재생 기전 규명 및 최적화
닫기
연계정보(NTIS)
연구보고서치주인대줄기세포 치근 국소부 밀집화 및 분화모델을 이용한 치주조직재생 기전 규명 및 최적화/Evaluation and optimization of periodontal tissue regeneration mechanism using local re-population and differentiation of periodontal ligament stem cells on root surface
사업 : 2021 과학기술정보통신부 개인기초연구(과기정통부)(R&D)과제 : 1711142684 전북대학 치주인대줄기세포 치근 국소부 밀집화 및 분화 모델을 이용한 치주조직재생 기전 규명 및 최적화등록번호,발행년월,발행기관명, 발행국가/사용언어,키워드 등록번호 발행년월 202309 발행기관명 전북대학교 발행국가 대한민국 초록 연구개요본 연구는 이상적인 치주조직 재생 유도시에 발생하는 생체현상을 모방하기 위해 치주조직재생 전구세포인 치주인대줄기세포의 치근부 밀집화 및 분화를 위한 새로운 전달 방식을 도입하고자 함 이를 통해 치주 결손부 및 치주염 국소환경의 치유 및 재생에서 나타나는 다양한 발현인자와 관련 기전을 규명하고 치주인대 줄기세포의 안정적이고 효율적인 국소전달을 통한 치주조직 재생 증진을 위한 최적화된 방법을 찾고자 함 이를 기반으로 기존의 치주조직재생유도의 개념을 실질적으로 구현할 수 있는 치주조직 재생 세포치료제 개발을 위한 기초지식을 확보하는 것을 목표로 함 연구 목표대비 연구결과 고순도 치주인대줄기세포주 확보 및 치근 타겟 나노파이버nanofiber 제작 표준화된 고순도 치주인대줄기세포주 확립 및 세포 특성 확인 하이드록시아파타이트Hydroxyapatite HA 결합성 펩타이드 함유 양친매성 화합물amphiphile을 활용한 나노파이버nanofiber 제작 조건 평가 치근 타겟 골형성 나노파이버 하이드로겔 전달체 최적화 나노파이버 하이드로겔 전달체 기능 및 치주인대줄기세포 친화성 평가 골형성 펩타이드 함유 양친매성 화합물amphiphile을 이용한 나노파이버 제작 조건 확립 및 효능 평가 치주염 국소환경 발현 인자 분석 줄기세포 밀집화 및 분화 모델 검증 치주염 국소환경에서 특이적으로 나타나는 발현 인자 분석 치주인대줄기세포 치근면 밀집화 및 분화 촉진을 통한 조직재생 효과 분석 치주염 국소환경에서 치주인대줄기세포 밀집화 및 분화모델 적용에 의한 치주조직재생 효과와 관련 기전 규명 치주염 동물모델 및 줄기세포 적용 평가 방법 확립 백서 ligatureinduced periodontitis 모델 검증 및 치주조직재생 평가 방법 확립 치주염 유발 염증성 치조골 결손 중대형 동물모델 구축 치주염 모델에서의 치주인대줄기세포의 치주조직 재생 효능 및 관련 기전 규명 연구개발성과의 활용 계획 및 기대효과연구개발결과의 중요성 학문적 활용 및 기대효과 치주조직 재생 연구 활성화의 기초 연구기반 마련 및 파생 연구과제 도출 치주조직 재생 활용기술 개발의 기반 마련 줄기세포 응용 치주조직재생 연구 및 치료제 개발을 위한 국내외 공동 연구개발 네트워크 구축 기술적 활용 및 기대효과 치주조직 결손부 재생 및 기능 회복을 위한 가장 효과적인 치료법 기반 제시 중간엽 줄기세포 성장인자를 기반으로 다양한 조직공학 기술 시도 및 치료법 개발로 임상 치료 기술 혁신 및 선진화 경제적산업적 활용 및 기대호과 조직재생 분야 원천기술 및 지적재산권 확보로 고부가가치 산업의 국가 경쟁력 향상 후속연구를 통해 치주조직 재생치료제 개발 및 상품화의 토대 마련 재생적 치주질환 치료를 통한 치아보존 가능성 증대로 치과치료 비용 절감 및 국민 의료비 절감출처 연구결과 요약문 2p
-
ntis줄기세포 유래 치아형성 세포원 확보 및 분화 고도화 기술 개발
-
과제
더보기
-
ntis사람 시상하부 줄기세포 및 엑소좀을 이용한 항노화 기술 개발
닫기
연계정보(NTIS)
과제사람 시상하부 줄기세포 및 엑소좀을 이용한 항노화 기술 개발
한양대학교 정부투자연구비 225,000,000원 총연구비 225,000,000원 뇌과학 뇌신경생물 신경발생 및 분화- 본 과제에 참여한 연구자
- 연구책임자이상훈
- 참여연구자장미윤;강지희;고승환;이나경;SULISTIO YANUAR ALAN;김수현;황영란;김주미;PIEKNELL KELVIN;석민종;켈빈;우예찬
연구목표연계정보 과제고유번호 2710074656 기준년도 2024 연구책임자 이상훈 과제수행기관 한양대학교 정부투자연구비 225,000,000 총연구비 225,000,000 - 6T관련효과
- 뇌신경과학 연구
-
ntis전분화능 줄기세포 유래 혈소판 대량생산 기술개발
닫기
연계정보(NTIS)
과제전분화능 줄기세포 유래 혈소판 대량생산 기술개발
차의과학대학교 분당차병원 정부투자연구비 550,000,000원 총연구비 550,000,000원 보건의료 신약·의약품개발 세포/조직치료제- 본 과제에 참여한 연구자
- 연구책임자강은주
- 참여연구자강순숙;김상미;송지환;최유빈;이연미;김용희;황새벽;김재은;한종석;이동규;이상진;나송은;홍채윤;박경서;황현욱
연구목표연계정보 과제고유번호 2460003541 기준년도 2024 연구책임자 강은주 과제수행기관 차의과학대학교 분당차병원 정부투자연구비 550,000,000 총연구비 550,000,000 - 6T관련효과
- 바이오신약 개발기술
-
ntis인공 적혈구 생산용 무혈청 화학조성 기반 유도만능줄기세포 증식 및 적혈구 분화배지 개발
닫기
연계정보(NTIS)
과제인공 적혈구 생산용 무혈청 화학조성 기반 유도만능줄기세포 증식 및 적혈구 분화배지 개발
주식회사셀라토즈테라퓨틱스 정부투자연구비 499,999,000원 총연구비 667,083,000원 생명과학 산업바이오 달리 분류되지 않는 산업바이오- 본 과제에 참여한 연구자
- 연구책임자임재승
- 참여연구자김혜선;이현주
연구목표연계정보 과제고유번호 2460003544 기준년도 2024 연구책임자 임재승 과제수행기관 주식회사셀라토즈테라퓨틱스 정부투자연구비 499,999,000 총연구비 667,083,000 - 6T관련효과
- 기타기초·기반기술
-
ntis인간 줄기세포 기반 인공혈소판 대량생산공정 기술 개발 및 고도화
닫기
연계정보(NTIS)
과제인간 줄기세포 기반 인공혈소판 대량생산공정 기술 개발 및 고도화
주식회사 듀셀바이오테라퓨틱스 정부투자연구비 1,000,000,000원 총연구비 1,250,000,000원 보건의료 신약·의약품개발 세포/조직치료제- 본 과제에 참여한 연구자
- 연구책임자김치화
- 참여연구자김정희;오선환;박인화;이민우;신응균;정현욱;전효진;이미현;조연희;김예니;김동영;함형석;황치연;김다정
연구목표연계정보 과제고유번호 2460003543 기준년도 2024 연구책임자 김치화 과제수행기관 주식회사 듀셀바이오테라퓨틱스 정부투자연구비 1,000,000,000 총연구비 1,250,000,000 - 6T관련효과
- 생물공정 기술
-
ntis사람 시상하부 줄기세포 및 엑소좀을 이용한 항노화 기술 개발
- 논문 더보기
- 특허 더보기


 개념
개념 지식
지식 발간
발간 동향
동향 차트 +
차트 + 뉴스
뉴스 부처보도자료
부처보도자료 성과
성과 연계정보
연계정보 연계정보
연계정보 영상 +
영상 +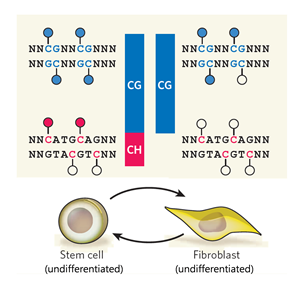 미분화 줄기세포와 분화 체세포에서의 시토신 메틸화 모식도
미분화 줄기세포와 분화 체세포에서의 시토신 메틸화 모식도
 두가지 종류의 맞춤형 줄기세포 획득과정 비교
두가지 종류의 맞춤형 줄기세포 획득과정 비교
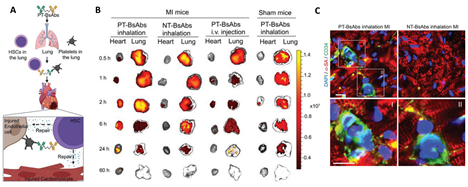 이중항체의 심근경색 손상부위 표적 및 줄기세포 모집 효능 검증(문헌 내 Figures 재구성)
이중항체의 심근경색 손상부위 표적 및 줄기세포 모집 효능 검증(문헌 내 Figures 재구성)
 인간 줄기세포로 만든 0.5mm 미니 심장 제작 성공
인간 줄기세포로 만든 0.5mm 미니 심장 제작 성공
 유도만능줄기세포(iPSC)를 이용한 파킨슨병 치료 개념도
유도만능줄기세포(iPSC)를 이용한 파킨슨병 치료 개념도
 기간별 자가 및 동종유래 줄기세포 임상연구 비율
기간별 자가 및 동종유래 줄기세포 임상연구 비율
 자가 및 동종유리 줄기세포 임상시험 추이
자가 및 동종유리 줄기세포 임상시험 추이
 줄기세포의 분류
줄기세포의 분류
 인간 줄기세포기반 원천기술 개발과 기대효과
인간 줄기세포기반 원천기술 개발과 기대효과
 인간 줄기세포기반 신약 스크리닝 기술개발의 기대효과
인간 줄기세포기반 신약 스크리닝 기술개발의 기대효과
 글로벌 제약회사 줄기세포 연구동향
글로벌 제약회사 줄기세포 연구동향
 퇴행성 뇌질환과 줄기세포에 관한 논문 발표 증가
퇴행성 뇌질환과 줄기세포에 관한 논문 발표 증가
 전분화능 줄기세포 유래 피부상피 오가노이드 모델 구축
전분화능 줄기세포 유래 피부상피 오가노이드 모델 구축
 전분화능줄기세포 유래 고성능 장 오가노이드 재생치료제 개발
전분화능줄기세포 유래 고성능 장 오가노이드 재생치료제 개발
 장 줄기세포 집합체의 무이종 배양법 및 활용 연구
장 줄기세포 집합체의 무이종 배양법 및 활용 연구
 3차원 장 오가노이드 유래 장 줄기세포 농축 배양 기술 개발
3차원 장 오가노이드 유래 장 줄기세포 농축 배양 기술 개발
 < 줄기세포 관련 Nature Outlook 컬렉션의 주요 내용 >
< 줄기세포 관련 Nature Outlook 컬렉션의 주요 내용 >
 줄기세포치료제의 질환 분야별 제품화 시기 예측
줄기세포치료제의 질환 분야별 제품화 시기 예측
 만능성 줄기세포의 초기 분화형태
만능성 줄기세포의 초기 분화형태
 줄기세포 연구개발 패러다임 변화
줄기세포 연구개발 패러다임 변화
 줄기세포 관련 Nature Outlook 컬렉션의 주요 내용
줄기세포 관련 Nature Outlook 컬렉션의 주요 내용
 인간 줄기세포로 만든 합성배아 사진
인간 줄기세포로 만든 합성배아 사진
 글로벌 유도만능 줄기세포 기반 치료제 회사
글로벌 유도만능 줄기세포 기반 치료제 회사
 유도만능 줄기세포의 분화능
유도만능 줄기세포의 분화능
 줄기세포 기반 세포봇의 비강 경로를 통한 in vivo 세포 전달
줄기세포 기반 세포봇의 비강 경로를 통한 in vivo 세포 전달
 줄기세포 기반 세포봇의 비강 경로를 통한 세포 전달
줄기세포 기반 세포봇의 비강 경로를 통한 세포 전달
 줄기세포시장 관련 주요 이벤트 타임라인
줄기세포시장 관련 주요 이벤트 타임라인
 줄기세포 시장 변화 트렌드
줄기세포 시장 변화 트렌드
 질환별 US 줄기세포시장 매출 전망('08년)
질환별 US 줄기세포시장 매출 전망('08년)
 인간 줄기세포로 만든 합성배아 사진
인간 줄기세포로 만든 합성배아 사진
 인간 줄기세포 기반 배아 모델(Blastoids)
인간 줄기세포 기반 배아 모델(Blastoids)
 [2013 생명공학백서 | 그림 4-1-5] 국내 줄기세포치료제별 환자 집단 전망
[2013 생명공학백서 | 그림 4-1-5] 국내 줄기세포치료제별 환자 집단 전망
 [2013 생명공학백서 | 그림 4-1-4] 글로벌 줄기세포 시장 현황 및 전망
[2013 생명공학백서 | 그림 4-1-4] 글로벌 줄기세포 시장 현황 및 전망
 줄기세포 기술로드맵(TRM) (2011-12)
줄기세포 기술로드맵(TRM) (2011-12)
 줄기세포 기업의 펀드유형 분포
줄기세포 기업의 펀드유형 분포
 유럽 국가(영국, 스웨덴, 덴마크)의 줄기세포 연구 지원 현황
유럽 국가(영국, 스웨덴, 덴마크)의 줄기세포 연구 지원 현황
 미국 주(州)정부의 줄기세포 연구 지원 현황
미국 주(州)정부의 줄기세포 연구 지원 현황
 줄기세포연구 자금지원기관
줄기세포연구 자금지원기관
 인간배아줄기세포의 유럽시장 규제수준
인간배아줄기세포의 유럽시장 규제수준
 유럽특허청에 등록되어 있는 줄기세포 관련 특허 출원국
유럽특허청에 등록되어 있는 줄기세포 관련 특허 출원국
 유럽 국가별 줄기세포 관련 임상시험 비중(2010년)
유럽 국가별 줄기세포 관련 임상시험 비중(2010년)
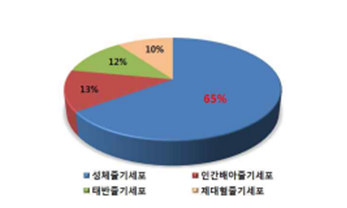 줄기세포 종류에 따른 치료제 선호도 비중(2010년)
줄기세포 종류에 따른 치료제 선호도 비중(2010년)
 세계 줄기세포 치료의 잠재적 시장(2010년)
세계 줄기세포 치료의 잠재적 시장(2010년)
 줄기세포 3R 전략
줄기세포 3R 전략
 SWOT 분석
SWOT 분석
 유럽의 줄기세포 시장 성장요인 및 억제요인
유럽의 줄기세포 시장 성장요인 및 억제요인
 유럽의 줄기세포 연구 기법 시장 성숙도
유럽의 줄기세포 연구 기법 시장 성숙도
 유럽의 줄기세포 시장 수익 전망
유럽의 줄기세포 시장 수익 전망
 줄기세포 연구 기법 중요도
줄기세포 연구 기법 중요도
 유럽줄기세포 연구의 목적, 분야 및 대상줄기세포(2010)
유럽줄기세포 연구의 목적, 분야 및 대상줄기세포(2010)
 줄기세포 시장의 핵심 영향 요소
줄기세포 시장의 핵심 영향 요소
 줄기세포 연구개발 SWOT 분석
줄기세포 연구개발 SWOT 분석
 미국 NIH의 줄기세포치료제 분야별 투자(’09~’10)
미국 NIH의 줄기세포치료제 분야별 투자(’09~’10)
 줄기세포 세계시장 전망(’08~’14)
줄기세포 세계시장 전망(’08~’14)
 줄기세포 치료제의 니즈와 시장출시
줄기세포 치료제의 니즈와 시장출시
 질병별 줄기세포 치료제 임상시험 현황(미국, 2011)
질병별 줄기세포 치료제 임상시험 현황(미국, 2011)
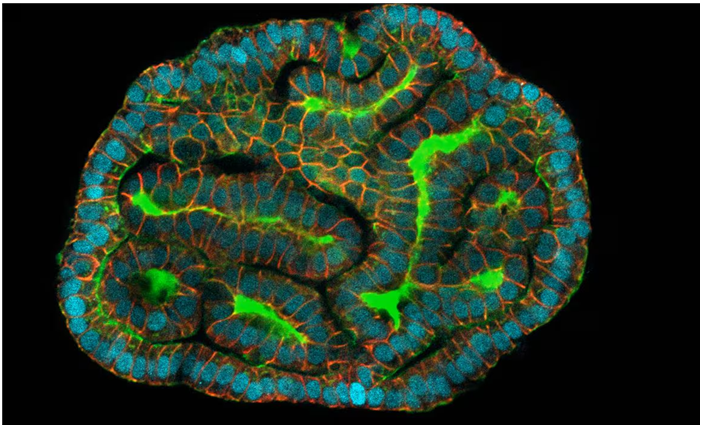 양수 유래 태아 상피 줄기세포로부터 형성된 신장 오가노이드
양수 유래 태아 상피 줄기세포로부터 형성된 신장 오가노이드
 항체를 이용한 골수편향 줄기세포(my-HSCs) 제거로 면역체계의 균형을 회복
항체를 이용한 골수편향 줄기세포(my-HSCs) 제거로 면역체계의 균형을 회복
 골수 내 조혈줄기세포의 분화
골수 내 조혈줄기세포의 분화
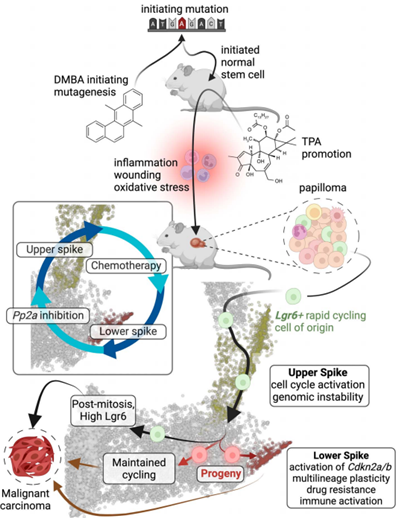 화학적 발암 모델에서 단일세포 수준에서 관찰한 줄기세포의 경로
화학적 발암 모델에서 단일세포 수준에서 관찰한 줄기세포의 경로
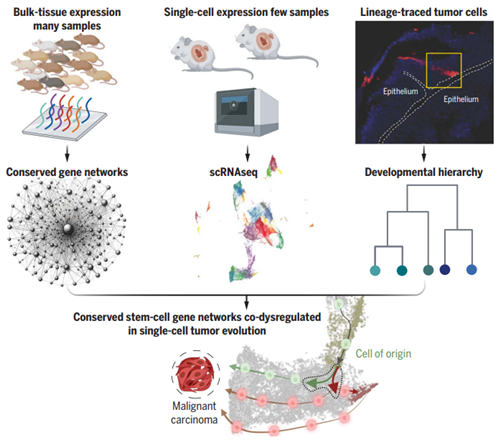 다양한 분석 방법을 결합한 암 발생 과정에서의 줄기세포 경로 분석
다양한 분석 방법을 결합한 암 발생 과정에서의 줄기세포 경로 분석
 최종 사용자별 글로벌 줄기세포 시장 수익 현황 및 전망
최종 사용자별 글로벌 줄기세포 시장 수익 현황 및 전망
 지역별 줄기세포 시장 수익 현황 및 전망
지역별 줄기세포 시장 수익 현황 및 전망
 응용 분야별 글로벌 줄기세포 시장 수익 현황 및 전망
응용 분야별 글로벌 줄기세포 시장 수익 현황 및 전망
 아시아 태평양 국가별 줄기세포 시장 수익 현황 및 전망
아시아 태평양 국가별 줄기세포 시장 수익 현황 및 전망
 세포 유형별 글로벌 줄기세포 시장 수익 현황 및 전망
세포 유형별 글로벌 줄기세포 시장 수익 현황 및 전망
 글로벌 줄기세포 시장 현황 및 전망 (2022년~2030년)
글로벌 줄기세포 시장 현황 및 전망 (2022년~2030년)
 부유 배양을 통한 인간 배아줄기세포 유래 신경전구세포 유도
부유 배양을 통한 인간 배아줄기세포 유래 신경전구세포 유도
 전분화능줄기세포 유래 고성능 장오가노이드 재생치료제
전분화능줄기세포 유래 고성능 장오가노이드 재생치료제
 3차원 장 오가노이드 유래 장 줄기세포 농축 배양 기술 개발
3차원 장 오가노이드 유래 장 줄기세포 농축 배양 기술 개발
 인간 전분화능줄기세포 유래 2차원 장 상피세포 모델 분화 기술 개발
인간 전분화능줄기세포 유래 2차원 장 상피세포 모델 분화 기술 개발
 인간 전분화능줄기세포 유래 오가노이드 및 활용
인간 전분화능줄기세포 유래 오가노이드 및 활용
 전분화능 줄기세포 유래 장 오가노이드 체외 성숙화 분자 기전 규명
전분화능 줄기세포 유래 장 오가노이드 체외 성숙화 분자 기전 규명
 전분화능 줄기세포 유래 리포터 장 오가노이드 개발
전분화능 줄기세포 유래 리포터 장 오가노이드 개발
 [2015 생명공학백서 | 그림 4-1-7] 줄기세포 개발국별 임상건수 및 점유율 (ʼ14.12 기준)
[2015 생명공학백서 | 그림 4-1-7] 줄기세포 개발국별 임상건수 및 점유율 (ʼ14.12 기준)
 [2015 생명공학백서 | 그림 4-1-6] 글로벌 줄기세포 기술 분야별 시장 현황 및 전망 (단위: 억 달러)
[2015 생명공학백서 | 그림 4-1-6] 글로벌 줄기세포 기술 분야별 시장 현황 및 전망 (단위: 억 달러)
 [2021 생명공학백서 | 그림 3-11] 세계 각국의 줄기세포/재생의료 논문지수
[2021 생명공학백서 | 그림 3-11] 세계 각국의 줄기세포/재생의료 논문지수
 세 부모 아기의 탄생 과정
세 부모 아기의 탄생 과정
 만능 유도 줄기세포 제작 혹은 역노화를 위한 세포 리프로그래밍 과정
만능 유도 줄기세포 제작 혹은 역노화를 위한 세포 리프로그래밍 과정
 [2017 생명공학백서 | 그림 3-10] 세포기반 치료제 중 중간엽줄기세포(MSC;Blue)를 이용한 국가별 임상승인 현황
[2017 생명공학백서 | 그림 3-10] 세포기반 치료제 중 중간엽줄기세포(MSC;Blue)를 이용한 국가별 임상승인 현황
 [2017 생명공학백서 | 그림 3-8] 질환별, 세포별 치료제 임상시험 현황
[2017 생명공학백서 | 그림 3-8] 질환별, 세포별 치료제 임상시험 현황
 [2017 생명공학백서 | 그림 3-6] 세계 줄기세포 치료제 상용화 현황
[2017 생명공학백서 | 그림 3-6] 세계 줄기세포 치료제 상용화 현황
 [2017 생명공학백서 | 그림 1-10] 중국과학원(CAS)의 줄기세포 연구논문과 특허 추이
[2017 생명공학백서 | 그림 1-10] 중국과학원(CAS)의 줄기세포 연구논문과 특허 추이
 면역결핍 미니돼지 및 인간 조혈줄기세포 활용 이종간 목적조직 보완법 기반 인공혈액 연구개발 개념도
면역결핍 미니돼지 및 인간 조혈줄기세포 활용 이종간 목적조직 보완법 기반 인공혈액 연구개발 개념도
 생쥐 배아줄기세포-배반포 키메라 기법 이용 유전자적중 생쥐 제작 방법 및 노벨상 수상자
생쥐 배아줄기세포-배반포 키메라 기법 이용 유전자적중 생쥐 제작 방법 및 노벨상 수상자
 특정장기 발생 결손 배아 및 유도만능줄기세포 기반 배반포 보완법 이용 인간-중대동물 이종간 키메라 장기 제작
특정장기 발생 결손 배아 및 유도만능줄기세포 기반 배반포 보완법 이용 인간-중대동물 이종간 키메라 장기 제작
 성체줄기세포-유래 및 전분화능줄기세포-유래 오가노이드 제작 현황
성체줄기세포-유래 및 전분화능줄기세포-유래 오가노이드 제작 현황
 [2019 생명공학백서 | 그림 3-9] 세계 각국의 줄기세포/재생의료 특허지수
[2019 생명공학백서 | 그림 3-9] 세계 각국의 줄기세포/재생의료 특허지수
 [2019 생명공학백서 | 그림 3-8] 세계 각국의 줄기세포/재생의료 논문지수
[2019 생명공학백서 | 그림 3-8] 세계 각국의 줄기세포/재생의료 논문지수
 [2019 생명공학백서 | 그림 3-3] 세계 줄기세포 및 주요 재생의료 치료제 개발 현황(2011~2017)
[2019 생명공학백서 | 그림 3-3] 세계 줄기세포 및 주요 재생의료 치료제 개발 현황(2011~2017)
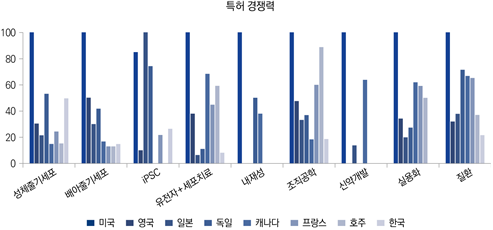 [2021 생명공학백서 | 그림 3-12] 세계 각국의 줄기세포/재생의료 특허지수
[2021 생명공학백서 | 그림 3-12] 세계 각국의 줄기세포/재생의료 특허지수
 [2021 생명공학백서 | 그림 3-5] 눈물샘 오가노이드 개발
[2021 생명공학백서 | 그림 3-5] 눈물샘 오가노이드 개발
 [2021 생명공학백서 | 그림 3-3]세계 줄기세포 및 주요 재생의료 치료제 개발 현황
[2021 생명공학백서 | 그림 3-3]세계 줄기세포 및 주요 재생의료 치료제 개발 현황
 [2021 생명공학백서 | 그림 1-5] 글로벌 재생의료 시장규모(2017~2028)
[2021 생명공학백서 | 그림 1-5] 글로벌 재생의료 시장규모(2017~2028)
 차세대 줄기세포치료제 임상개발 현황
차세대 줄기세포치료제 임상개발 현황
 줄기세포 국외 시장 동향
줄기세포 국외 시장 동향
 2013년도 정부 줄기세포 시행계획
2013년도 정부 줄기세포 시행계획
 줄기 세포 예산현황 및 NIT 줄기세포 예산현황
줄기 세포 예산현황 및 NIT 줄기세포 예산현황
 환자와 유전자 일치하는 줄기세포 획득과정 비교
환자와 유전자 일치하는 줄기세포 획득과정 비교
 줄기세포의 종류
줄기세포의 종류
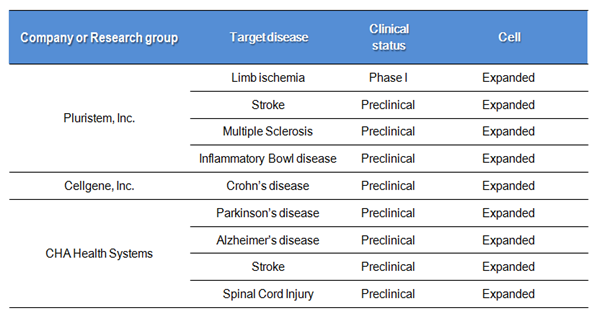 지방줄기세포를 이용한 세포치료제 개발현황
지방줄기세포를 이용한 세포치료제 개발현황
 태반줄기세포를 이용한 세포치료제 개발현황
태반줄기세포를 이용한 세포치료제 개발현황
 제대혈 줄기세포를 이용한 세포치료제 개발현황
제대혈 줄기세포를 이용한 세포치료제 개발현황
 태아 뇌줄기세포를 이용한 세포치료제 개발현황
태아 뇌줄기세포를 이용한 세포치료제 개발현황
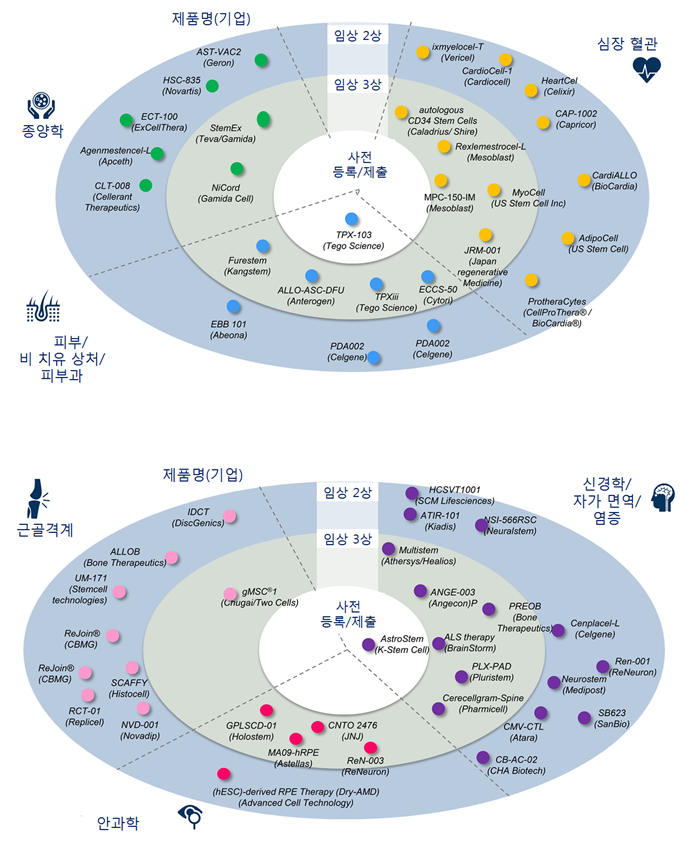
 간엽줄기세포의 다양한 분비성분 및 역할
간엽줄기세포의 다양한 분비성분 및 역할
 간엽줄기세포의 다양한 분비성분 및 역할
간엽줄기세포의 다양한 분비성분 및 역할
 인간배아줄기세포 유래 인공적혈구(좌측)와 혈소판 (우측) 생산기술 개발
인간배아줄기세포 유래 인공적혈구(좌측)와 혈소판 (우측) 생산기술 개발
 인간배아줄기세포 유래 망막색소상피세포 이식 스타가르트 환자의 시력회복
인간배아줄기세포 유래 망막색소상피세포 이식 스타가르트 환자의 시력회복
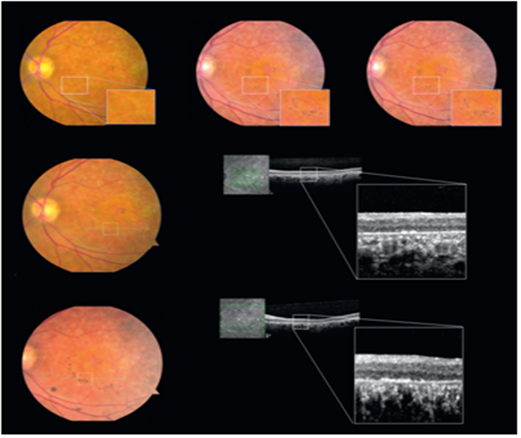 질환모델동물에 이식된 인간배아줄기세포 유래 망막색소상피세포의 생착
질환모델동물에 이식된 인간배아줄기세포 유래 망막색소상피세포의 생착
 인간배아줄기세포 유래 망막색소상피세포 전임상 효력시험 결과
인간배아줄기세포 유래 망막색소상피세포 전임상 효력시험 결과
 인간배아줄기세포 유래 망막색소상피세포
인간배아줄기세포 유래 망막색소상피세포
 줄기세포의 특성 및 종류
줄기세포의 특성 및 종류
 유도 만능줄기세포 생성 및 직접교차분화의 모식도
유도 만능줄기세포 생성 및 직접교차분화의 모식도
 한국 줄기세포시장 전망
한국 줄기세포시장 전망
 질환별 US 줄기세포 시장 및 매출규모 (2007년)
질환별 US 줄기세포 시장 및 매출규모 (2007년)
 줄기세포 질환별 세계시장 현황 및 전망
줄기세포 질환별 세계시장 현황 및 전망
 줄기세포 기술별 세계시장 현황 및 전망
줄기세포 기술별 세계시장 현황 및 전망
 줄기세포 분야별 세계시장 현황 및 전망
줄기세포 분야별 세계시장 현황 및 전망
 줄기세포 예산 연도별 현황 (2010 ~ 2012)
줄기세포 예산 연도별 현황 (2010 ~ 2012)
 줄기세포 관련 논문 발표 주요 국가 (2001.1.1. ~ 2010.11.9)
줄기세포 관련 논문 발표 주요 국가 (2001.1.1. ~ 2010.11.9)
 국내 성체줄기세포 치료제 임상 현황
국내 성체줄기세포 치료제 임상 현황
 세계 줄기세포 임상시험 점유율
세계 줄기세포 임상시험 점유율
 줄기세포의 종류
줄기세포의 종류
 줄기세포 치료
줄기세포 치료
 제대혈 유래 중간엽 줄기세포의 다양한 분비 단백질들을 통한 동시다발적 알츠하이머병 치료 기전
제대혈 유래 중간엽 줄기세포의 다양한 분비 단백질들을 통한 동시다발적 알츠하이머병 치료 기전
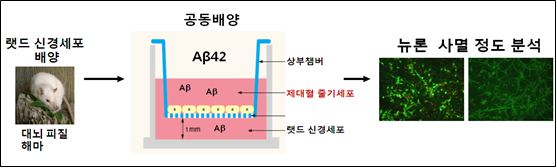 공동배양 챔버를 이용한 제대혈 중간엽줄기세포의 Paracrine 능력 분석
공동배양 챔버를 이용한 제대혈 중간엽줄기세포의 Paracrine 능력 분석
 소분자 화합물을 활용하여 유도한 신경줄기세포의 in vivo 분화능 검증
소분자 화합물을 활용하여 유도한 신경줄기세포의 in vivo 분화능 검증
 인간배아 생성을 모방하는 체외 줄기세포 기반의 배아모델
인간배아 생성을 모방하는 체외 줄기세포 기반의 배아모델
 만능성 줄기세포의 초기 분화형태
만능성 줄기세포의 초기 분화형태
 노화 뇌에서 니치세포 분비인자를 통한 신경줄기세포 휴지기 조절
노화 뇌에서 니치세포 분비인자를 통한 신경줄기세포 휴지기 조절
 유도만능줄기세포(iPSC)를 이용한 파킨슨병 치료 개념도
유도만능줄기세포(iPSC)를 이용한 파킨슨병 치료 개념도
 타인 유래 유도만능줄기세포(iPSC, induced pluripotent stem cell)의 임상시험
타인 유래 유도만능줄기세포(iPSC, induced pluripotent stem cell)의 임상시험
 최근 주요 줄기세포 기업의 경영 전략
최근 주요 줄기세포 기업의 경영 전략
 주요 기업별 줄기세포 시장 점유율(2016년)
주요 기업별 줄기세포 시장 점유율(2016년)
 아시아 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
아시아 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
 유럽 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
유럽 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
 북미 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
북미 지역 줄기세포 시장 현황 및 전망(단위: 억달러)
 글로벌 줄기세포 시장 현황 및 전망(2016-2025년)
글로벌 줄기세포 시장 현황 및 전망(2016-2025년)
 국가별 줄기세포치료제 신규 임상시험 건수(2016)
국가별 줄기세포치료제 신규 임상시험 건수(2016)
 응용별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
응용별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
 기술별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
기술별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
 제품(Product)별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
제품(Product)별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
 줄기세포 분야 성장과 수익 기회 매트릭스
줄기세포 분야 성장과 수익 기회 매트릭스
 지역별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
지역별 글로벌 줄기세포 시장 현황 및 전망(단위: 십억달러)
 글로벌 줄기세포 시장 현황 및 전망(2016-2025년)
글로벌 줄기세포 시장 현황 및 전망(2016-2025년)
 글로벌 줄기세포 시장현황 및 전망(2019-2025년, 단위: 백만달러)
글로벌 줄기세포 시장현황 및 전망(2019-2025년, 단위: 백만달러)
 줄기세포와 재생의료의 범위와 영역
줄기세포와 재생의료의 범위와 영역
 줄기세포 분류 및 생성 과정
줄기세포 분류 및 생성 과정
 글로벌 줄기세포 분야 단일세포 분석 시장현황 및 전망(2014-2025년, 단위: 백만달러)
글로벌 줄기세포 분야 단일세포 분석 시장현황 및 전망(2014-2025년, 단위: 백만달러)
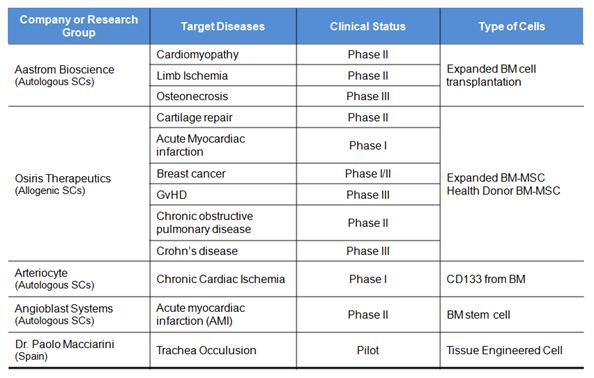
 글로벌 줄기세포치료제 주요 파이프라인 현황
글로벌 줄기세포치료제 주요 파이프라인 현황
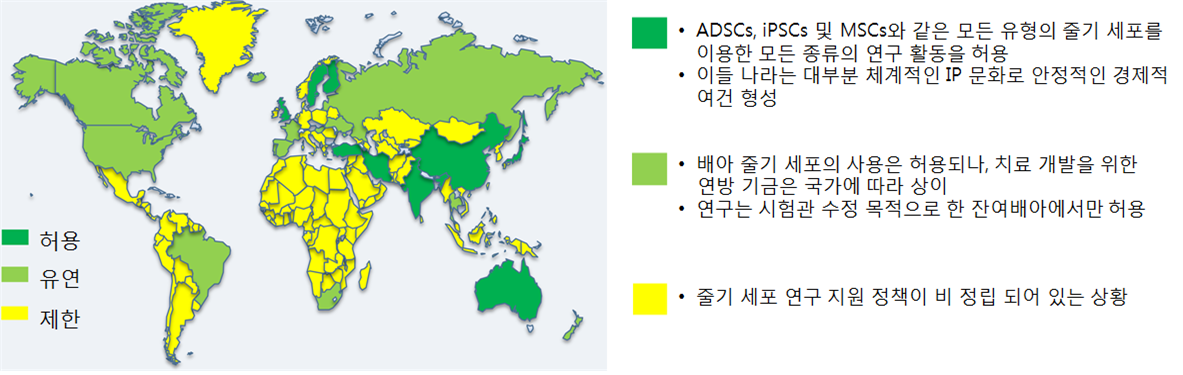 글로벌 줄기세포치료제 규제 및 정책 현황
글로벌 줄기세포치료제 규제 및 정책 현황
 글로벌 줄기세포치료제 시장 현황 및 전망(2017-2023년, 단위: 십억달러)
글로벌 줄기세포치료제 시장 현황 및 전망(2017-2023년, 단위: 십억달러)
 재생의약과 줄기세포치료제의 범위
재생의약과 줄기세포치료제의 범위
 줄기세포 분류 및 생성 과정
줄기세포 분류 및 생성 과정
 줄기세포를 이용한 신약 스크리닝 모식도
줄기세포를 이용한 신약 스크리닝 모식도
 유도만능줄기세포 관련 주요 서비스 제품업체(2013년)
유도만능줄기세포 관련 주요 서비스 제품업체(2013년)
 유도만능줄기세포 관련 세품 주요 공급업체 및 제조업체, 2013년
유도만능줄기세포 관련 세품 주요 공급업체 및 제조업체, 2013년
 유도만능줄기세포 관련 제품기능별 시장 비중, 2012–2018
유도만능줄기세포 관련 제품기능별 시장 비중, 2012–2018
 유도만능줄기세포 응용영역별 시장 현황 및 전망(2012–2018, 단위 : 백만달러)
유도만능줄기세포 응용영역별 시장 현황 및 전망(2012–2018, 단위 : 백만달러)
 유도만능줄기세포 연구목적별 시장 비중, 2012–2018
유도만능줄기세포 연구목적별 시장 비중, 2012–2018
 유도만능줄기세포 분화세포별 시장 비중(2012–2018, 단위 : 백만달러)
유도만능줄기세포 분화세포별 시장 비중(2012–2018, 단위 : 백만달러)
 유도만능줄기세포 제작방법별 시장 비중(2012–2018, 단위 : 백만달러)
유도만능줄기세포 제작방법별 시장 비중(2012–2018, 단위 : 백만달러)
 유도만능줄기세포 지역별 시장 비중, 2012–2018
유도만능줄기세포 지역별 시장 비중, 2012–2018
 글로벌 유도만능줄기세포 시장 현황 및 전망(2012–2018, 단위 : 백만달러)
글로벌 유도만능줄기세포 시장 현황 및 전망(2012–2018, 단위 : 백만달러)
 유도만능줄기세포 관련 시장 분류
유도만능줄기세포 관련 시장 분류
 유도만능줄기세포 분야 NIH 투자 현황(2007–2013, 단위 : 백만달러)
유도만능줄기세포 분야 NIH 투자 현황(2007–2013, 단위 : 백만달러)
 유도만능줄기세포 분야 정부투자 현황(2007–2013, 단위 : 백만달러)
유도만능줄기세포 분야 정부투자 현황(2007–2013, 단위 : 백만달러)
 줄기세포 활용영역 전망
줄기세포 활용영역 전망
 줄기세포 종류별 장단점 비교
줄기세포 종류별 장단점 비교
 줄기세포치료제의 상용화 단계 진입에 성공하는 성과
줄기세포치료제의 상용화 단계 진입에 성공하는 성과
 줄기세포 종류별 제작방법 비교
줄기세포 종류별 제작방법 비교
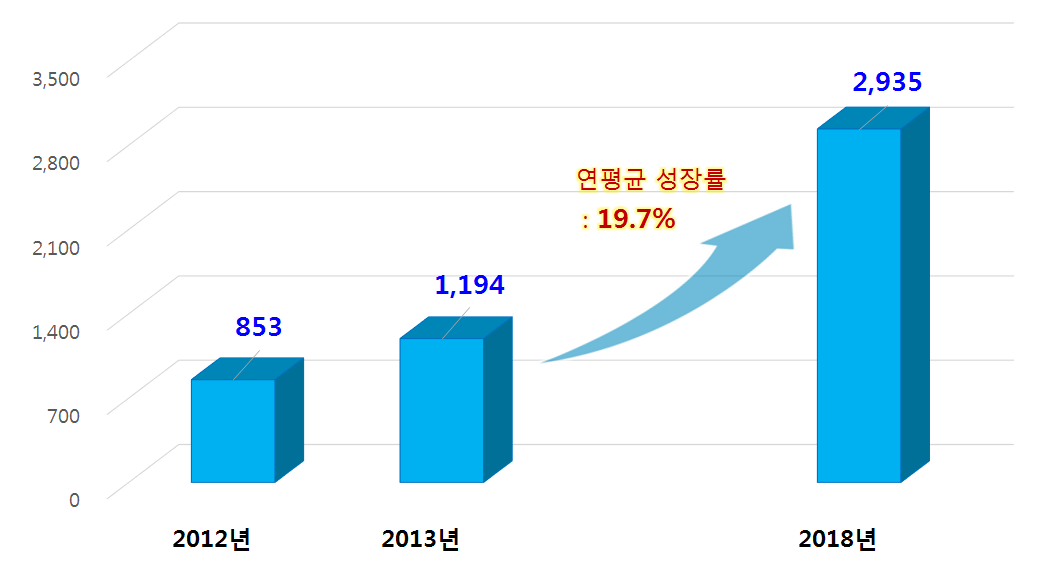 글로벌 유도만능줄기세포 시장 현황 및 전망, 2012–2018
글로벌 유도만능줄기세포 시장 현황 및 전망, 2012–2018
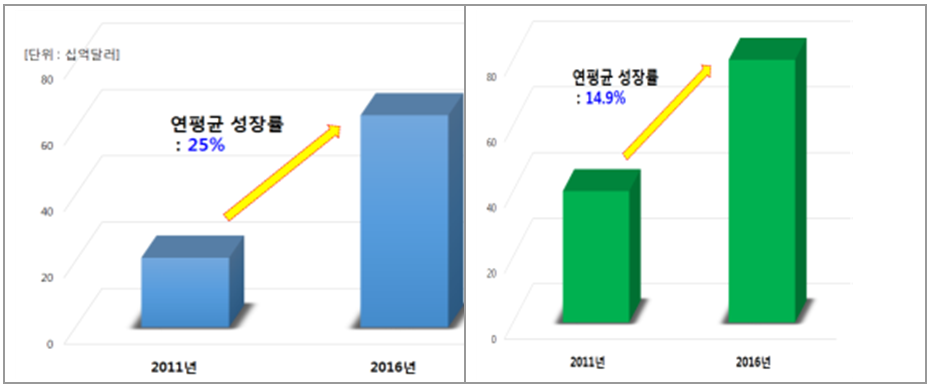 글로벌 줄기세포 및 생체재료 분야 시장 현황 및 전망(2011-2016)
글로벌 줄기세포 및 생체재료 분야 시장 현황 및 전망(2011-2016)
 국내 줄기세포 시장 영향요인 분석
국내 줄기세포 시장 영향요인 분석
 재생의약/줄기세포 시장의 기회
재생의약/줄기세포 시장의 기회
 글로벌 줄기세포 시장현황 및 전망(2013~2018)
글로벌 줄기세포 시장현황 및 전망(2013~2018)
 임상단계별 줄기세포치료제 개발 관련 임상시험 현황
임상단계별 줄기세포치료제 개발 관련 임상시험 현황
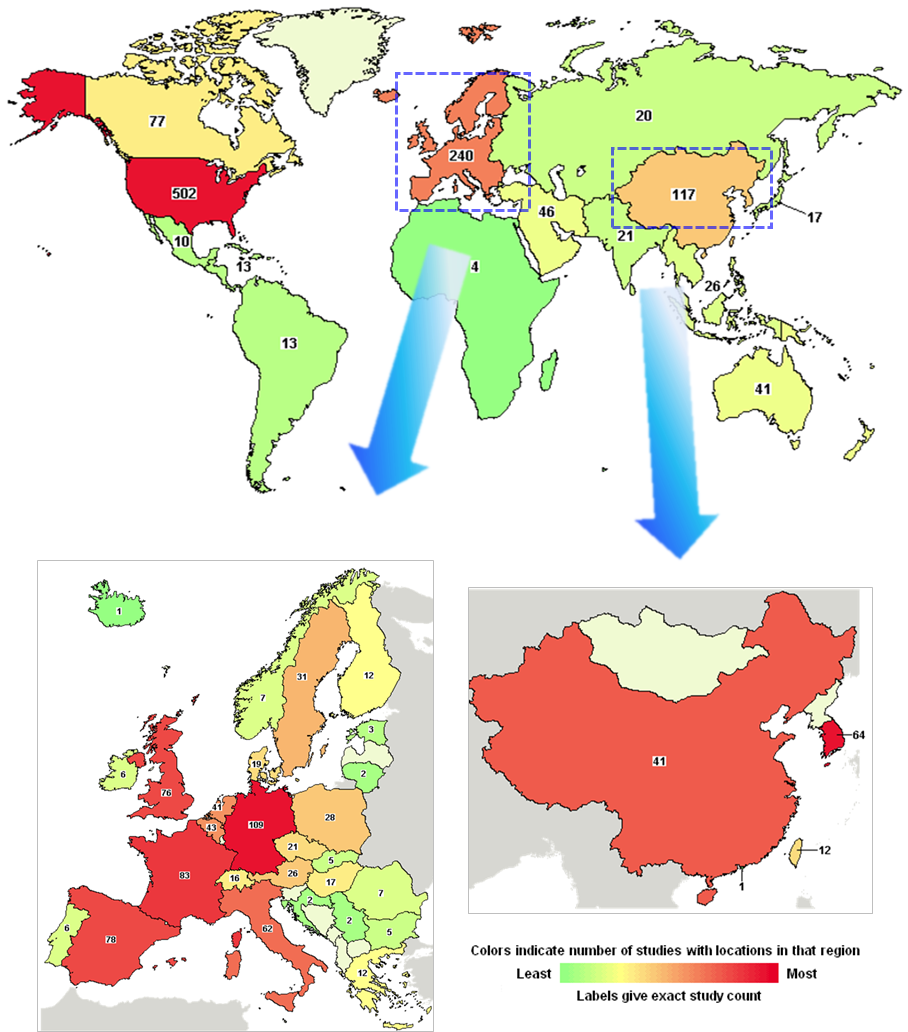 지역별 줄기세포치료제 개발 관련 임상시험 현황
지역별 줄기세포치료제 개발 관련 임상시험 현황
 글로벌 줄기세포치료제 승인 현황
글로벌 줄기세포치료제 승인 현황
 국내 줄기세포 분야 주요기업 현황
국내 줄기세포 분야 주요기업 현황
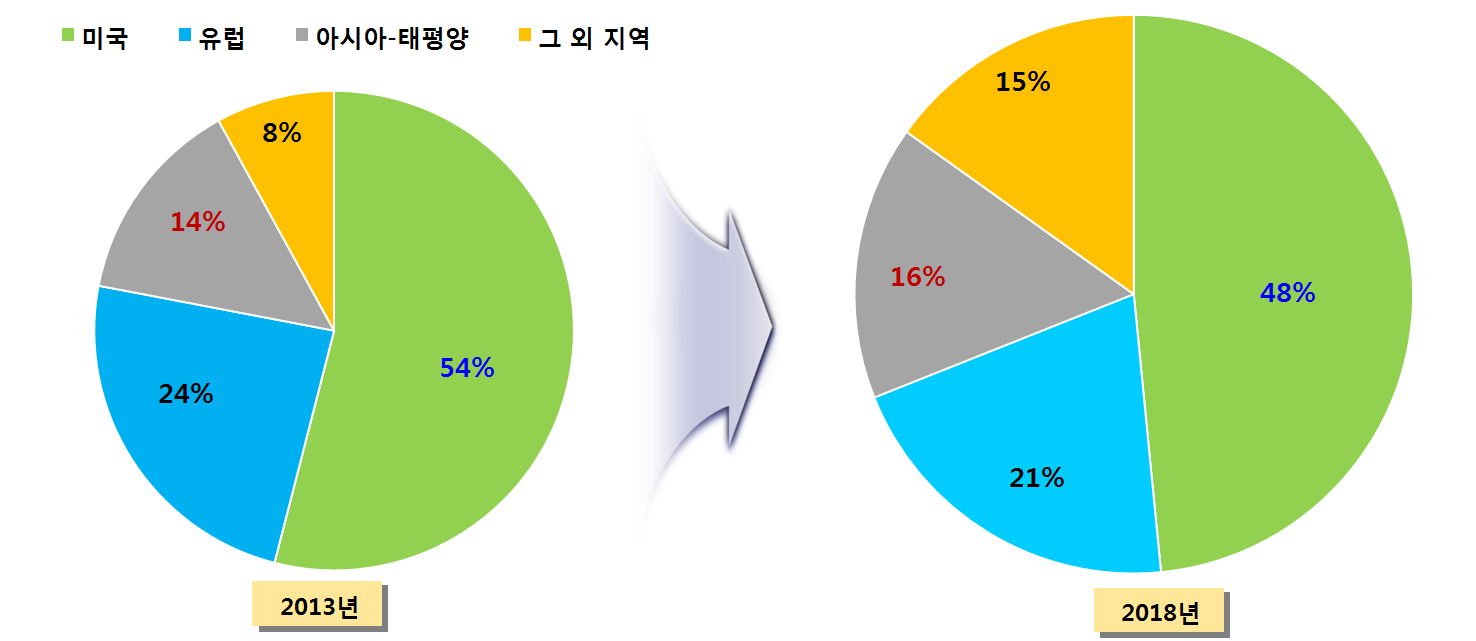 지역별 줄기세포 시장현황 및 전망
지역별 줄기세포 시장현황 및 전망
 세포원별 줄기세포 시장현황 및 전망(단위 : 십억달러)
세포원별 줄기세포 시장현황 및 전망(단위 : 십억달러)
 줄기세포 분류 및 생성 과정
줄기세포 분류 및 생성 과정




![[사이언스포럼] 줄기세포 연구로 여는 생명과학의 미래](/InnoDS/data/upload/bt_youtube/CDE4CE0A-E6C9-D5A2-EBCE-E56C92B7DEBC.jpg)